- Nickelsulfat
-
Strukturformel 
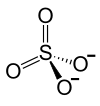
Allgemeines Name Nickel(II)-sulfat Andere Namen Nickelsulfat
Summenformel NiSO4 CAS-Nummer wasserfrei: 7786-81-4
Hexahydrat: 10101-97-0Kurzbeschreibung Hexahydrat: geruchlose, smaragdgrüne bis blaue Kristalle
wasserfrei: gelbe KristalleEigenschaften Molare Masse Hexahydrat: 262,85 g·mol−1
wasserfrei: 154,75 g·mol−1Aggregatzustand fest
Dichte Hexahydrat: 2,07 g·cm−3
wasserfrei: 3,68 g·cm−3 [1]Schmelzpunkt Hexahydrat: 53 °C [1]
Siedepunkt thermische Zersetzung: 840 °C [1]
Löslichkeit 650 g·l−1 in Wasser (20 °C)[2]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Gesundheits-
schädlichUmwelt-
gefährlich(Xn) (N) R- und S-Sätze R: 22-40-42/43-50/53 S: (2)-22-36/37-60-61 LD50 264 mg·kg−1[2]
WGK 2 – wassergefährdend [2] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Nickel(II)-sulfat ist das Nickelsalz der Schwefelsäure. Es besteht aus je einem Nickel-Kation (Ni2+) und einem Sulfat-Anion (SO42−). Beim Erhitzen über 840 °C tritt Zersetzung unter Bildung von giftigen Dämpfen (Nickelmonoxid, Schwefeltrioxid) auf. In wässriger Lösung bildet Nickel(II)-sulfat schwache Säuren.
Inhaltsverzeichnis
Darstellung
Nickel(II)-sulfat kann dargestellt werden durch Reaktion von Nickel mit verdünnter Schwefelsäure und anschließender Kristallisation.
Hydrate
Nickel(II)-sulfat existiert neben der wasserfreien Form auch als Hepta- und Hexahydrat. Das Heptahydrat liegt in Form von dunkelgrünen Kristallen vor. Bei 31,5 °C wird aus dem Heptahydrat Hexahydrat, das smaragdgrün bis blau ist. Die wasserfreie, gelbe Form tritt bei Temperaturen über 103 °C auf.[4]
Verwendung
Nickel(II)-sulfat ist die technisch wichtigste Nickelverbindung. Es dient zur Herstellung von anderen Nickelverbindung und Katalysatoren.[4] Die wässrigen Lösungen von Nickel(II)-sulfat und Nickel(II)-chlorid NiCl2 werden zur galvanischen Abscheidung von metallischen Nickelschichten verwendet. Weiterhin wird es in der Färberei als Beizmittel und bei der Herstellung von Gasmasken verwendet.
Sicherheitshinweise
Nickel(II)-sulfat wurde als beim Mensch bekanntermaßen krebserzeugenden Stoff (Kategorie 1) eingestuft (TRGS 905).[1] Der Stoff kann zu Kontaktallergien führen. Nach dem Verschlucken treten Reizungen des Magen-Darm-Trakts auf.
Quellen
- ↑ a b c d Eintrag zu Nickel(II)-sulfat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 04. November 2008 (JavaScript erforderlich)
- ↑ a b c Sicherheitsdatenblatt (Merck)
- ↑ Eintrag zu CAS-Nr. 7786-81-4 im European chemical Substances Information System ESIS
- ↑ a b CD Römpp Chemie Lexikon – Version 1.0, Stuttgart/New York: Georg Thieme Verlag 1995
Wikimedia Foundation.

-sulfate-hexahydrate-sample.jpg)