- P53
-
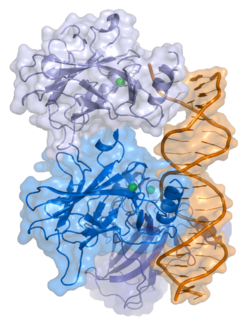
P53 Bänder-/Oberflächenmodell vpn p53 an DNA nach PDB 1TUP Vorhandene Strukturdaten: 1a1u, 1aie, 1c26, 1gzh, 1hs5, 1kzy, 1olg, 1olh, 1pes, 1pet, 1sae, 1saf, 1sag, 1sah, 1sai, 1saj, 1sak, 1sal, 1tsr, 1tup, 1uol, 1ycs, 2ac0, 2ady, 2ahi, 2ata, 2b3g, 2bim, 2bin, 2bio, 2bip, 2biq, 2fej, 2gs0, 2h1l, 2j1w, 2j1x, 2j1y, 2j1z, 2j20, 2j21, 2ocj, 3sak Größe 393 Aminosäuren Kofaktor Zn2+ Isoformen 2 Bezeichner Gen-Namen TP53; LFS1; TRP53; p53 Externe IDs OMIM: 191170 UniProt: P04637 MGI: 98834 Vorkommen Homologie-Familie TP53 Übergeordnetes Taxon Chordatiere Das Protein p53 ist in vielen Typen von entarteten Zellen in erhöhter Menge messbar. Es ist auch vorhanden in normal sprossenden Zellen, aber in ruhenden Zellen kaum oder gar nicht zu finden. In vielen Tumortypen ist p53 mutiert. In manchen, aber nicht allen Tumoren scheint das Protein als Tumorsuppressor zu wirken. p53 spielt wahrscheinlich eine Rolle bei der Regulation des Zellzyklus, wo es die Aktivität einer Anzahl von Genen bremst. p53 ist in allen Chordatieren zu finden.[1]
P53 wurde 1979 unabhängig voneinander von Albert B. DeLeo, David Lane und Arnold Levine entdeckt (DeLeo, 1979; Lane und Crawford, 1979; Linzer und Levine, 1979). Der humane Tumorsuppressor p53 reguliert als Transkriptionsfaktor nach DNA-Schädigung die Expression von Genen, die an der Kontrolle des Zellzyklus, an der Induktion der Apoptose (des programmierten Zelltods) oder an der DNA-Reparatur beteiligt sind. Aufgrund dieser Eigenschaft wird p53 in der Literatur als „Wächter des Genoms“ bezeichnet (Lane, 1992). Die besondere medizinische Bedeutung erklärt sich aus dem Befund, dass p53 in 50 % aller menschlichen Tumoren mutiert ist. Der Verlust der p53-Funktion spielt daher eine kritische Rolle bei der Entstehung von Krebs, ist jedoch nicht der ursächliche Auslöser für das unkontrollierte Wachstum von Zellen. p53 wurde aufgrund seiner Bedeutung 1993 zum „Molekül des Jahres“ gewählt.
Inhaltsverzeichnis
Funktion von p53
p53 erhielt seinen Namen aufgrund der scheinbaren Molekularmasse von 53 kDa auf einem SDS-PAGE Gel. Das dazugehörige Gen, das TP53-Tumorsuppressor-Gen, liegt auf dem Chromosom 17p13.1. Um es von dem Protein zu unterscheiden wird es kursiv geschrieben (TP53 war früher ein Synonym für menschliches p53). Das p53 Protein ist von Natur aus instabil, wird aber regelmäßig „nachgebildet“. Kommt es in der DNA jedoch zu Schäden, etwa einem Doppelstrangbruch, die eine Replikation oder eine Mitose fehlerhaft ablaufen lassen würden, so wird p53 innerhalb von 30 Minuten posttranslational stabilisiert, wodurch sich p53 in der Zelle akkumuliert.
Die Akkumulation von p53 hat viele Folgen. So werden einerseits DNA-Reparatur-Mechanismen in Gang gesetzt, andererseits wird der Zellzyklus gestoppt. Letzteres geschieht dadurch, dass p53 als Transkriptionsfaktor die Produktion des Proteins p21 induziert. p21 wiederum hemmt sowohl den Cyclin D/CDK4/6-Komplex als auch den Cyclin E/CDK2-Komplex. Diese werden eigentlich benötigt, um einen vom Protein pRB gebundenen weiteren Transkriptionsfaktor (E2F) freizusetzen, der den Zellzyklus weiterführen würde. Die Zelle bekommt also durch p53 Zeit, sich selbst zu reparieren, bevor sie sich teilt. Ist die DNA wieder in Ordnung, so sinkt der p53-Spiegel wieder, p21 wird nicht mehr transkribiert und nach einer Weile geht der Zellzyklus weiter.
Wird p53 jedoch zu stark angehäuft und kommen weitere Faktoren hinzu, so aktiviert p53 Gene der Bcl2-Familie (insbesondere den Apoptose-Regulator BAX), die wiederum in Form einer Signalkaskade Caspasen auslösen und so zu Apoptose (programmierter Zelltod) führen. Demnach ist p53 wie eine Art Bremse, die nötig ist, um Zellen vom unkontrollierten Wachstum und weiterer Schädigung abzuhalten, und deren Mutation zu verstärkter Zellteilung führt.
Schädigung von p53
p53 ist ein Schlüsselprotein mit enormer Bedeutung, ein Defekt hat demnach große Schadwirkung. Nach heutigem Kenntnisstand sind es im Allgemeinen Punktmutationen, die zu einem Funktionsverlust führen. Als Folge dieses Verlustes ist weder ein Anhalten des Zellzyklus zur DNA-Reparatur, noch die Einleitung der Apoptose möglich. Die Zellen beginnen sich auch mit Schäden in der DNA unkontrolliert zu teilen, es kommt zur Tumorbildung.
Im Folgenden eine Liste der Krankheiten, die ausschließlich oder hauptsächlich auf Mutationen in TP53 (dem p53-Gen) zurückzuführen sind.
Krankheit Häufigkeit der p53-Mutation OMIM Bemerkungen Li-Fraumeni-Syndrom Typ 1 70 Prozent aller Fälle angeboren 151623 Nebennierenrindenkarzinom 88 Prozent aller Fälle angeboren 202300 Folge des Li-Fraumeni-Syndroms Speiseröhrenkrebs 20 von 26 (1 Allel)[2] 133239 gehäuft in Nordchina Nasopharynxkarzinom 4 von 41 aus Hongkong und Guangxi[3] 161550 100fach gehäuft in Südchina
Patienten, die mit dem Li-Fraumeni-Syndrom geboren werden, haben eine angeborene Mutation in p53. So kommt es bei Menschen mit dieser Mutation schon in frühester Kindheit zu diversen Tumoren, wie Brustkrebs, Leukämie, Hirntumore und vieles mehr. Ursache für den Krebs ist jedoch nicht die Mutation von p53 selbst, sondern die hohe Zellteilungsrate während des embryonalen Wachstums, trotz Defekten in der DNA, sodass Schäden sich akkumulieren und weitere Gene für die Regulierung des Zellwachstums geschädigt werden können. Da jede Röntgenuntersuchung oder Chemotherapie die Mutationsrate erhöht, ist sowohl die Diagnose, als auch die Behandlung dieser Patienten besonders schwierig.Neben spontan auftretenden Mutationen gibt es auch andere Ursachen für Schäden an p53 bzw. seiner Funktionen. So gibt es tumorinduzierende Viren (sogenannte Oncoviren), die p53 hemmen, abbauen oder dessen natürlichen Abbau beschleunigen. Diese Strategie nutzen die Viren, da auch virale Erkrankungen eine Apoptose auslösen können und somit die Viren an ihrer Weiterverbreitung hindern würde.
Weiterhin kann p53 durch chemische Stoffe geschädigt werden, zum Beispiel durch das im Tabakrauch enthaltene Benzo(a)pyren oder durch Aflatoxin. Diese Stoffe hinterlassen charakteristische Merkmale in der geschädigten DNA und können dadurch als Verursacher identifiziert werden.
Zusammenhang zwischen p53 und Lebenserwartung
Versuche an Fruchtfliegen deuten darauf hin, dass eine künstlich reduzierte Aktivität des Anti-Tumor-Proteins sich bei den Versuchstieren auf die Lebensdauer positiv auswirkt[4]. Verhält sich das Protein jedoch aktiver als normal (überaktiv), so alterten behandelte Mäuse wesentlich schneller als gewöhnlich [5] Der Mechanismus selbst ist jedoch bislang ungeklärt.
Quellen
- ↑ PROSITE PS00348
- ↑ R. F. Boynton et al.: Loss of heterozygosity involving the APC and MCC genetic loci occurs in the majority of human esophageal cancers. Proc. Nat. Acad. Sci. 89/-/1992. S. 3385-3388. PMID 1565631
- ↑ F. Chakrani et al.: Mutations clustered in exon 5 of the p53 gene in primary nasopharyngeal carcinomas from southeastern Asia. Int. J. Cancer 61/-/1995. S. 316-320. PMID 7729941
- ↑ J. Bauer u.a. in Current Biology
- ↑ Ferbeyre G, Lowe SW: "Aging: The price of tumour suppression?" Nature 415, 26-27 (2002).
Literatur
- Hainaut, Pierre; Wiman, Klas (Eds.): 25 Years of P53 Research, Kluwer Academic Publishers (2005), ISBN 1-4020-2920-9
- Stiewe T (2007): "The p53 family in differentiation and tumorigenesis", Nature Reviews Cancer 7, 165-168 Artikel online
- Ferbeyre G, Lowe SW: "Aging: The price of tumour suppression?" Nature 415, 26-27 (2002) Artikel online
- Lacroix M, Toillon RA, and Leclercq G (2006): p53 and breast cancer, an update.; Endocrine-Related Cancer 13, 293-325
- Lane DP and Crawford LV (1979): T antigen is bound to a host protein in SV40-transformed cells.; Nature 278, 261-263
- Linzer DI and Levine AJ (1979): Characterization of a 54K dalton cellular SV40 tumor antigen present in SV40-transformed cells and uninfected embryonal carcinoma cells.; Cell 17, 43-52
- Lane DP (1992): Cancer. p53, guardian of the genome.; Nature 358, 15-16
- DeLeo AB (1979) Detection of a transformation-related antigen in chemically induced sarcomas and other transformed cells of the mouse. Proc Natl Acad Sci U S A. 1979 May;76(5):2420-4
Siehe auch
Weblinks
Wikimedia Foundation.