- Phenylpropanoid
-
Phenylpropanoide sind organisch-chemische Verbindungen mit einem typischen Kohlenstoffgrundgerüst, die aus einem Benzolaromaten und einer Kette aus drei Kohlenstoffatomen aufgebaut sind und häufig sowohl Hydroxy- als auch Methoxy-Gruppen am Aromaten tragen. Viele Phenylpropanoide sind Naturstoffe, die in Pflanzen und Mikroorganismen über den Shikimat-Biosyntheseweg[1] mit Phenylalanin als Zwischenprodukt[2] gebildet werden. Phenylpropanoide sind, neben den Terpenen, ein häufiger Bestandteil von ätherischen Ölen und stellen die Mehrzahl der natürlich vorkommenden phenolischen Naturstoffe bzw. deren Vorstufe dar. Zu den bekannten Vertretern aus der Gruppe der Phenylpropanoide gehören: Anethol, Apiol, Zimtaldehyd, Dillapiol und Estragol.
Inhaltsverzeichnis
Vorkommen
Phenylpropanoide sind eine sehr häufig vorkommende Klasse sekundärer Pflanzenstoffe, welche die Hauptmenge der natürlich vorkommenden Phenole und Aromaten darstellt bzw. deren biosynthetische Vorstufe sind. Das strukturelle Spektrum ist sehr breit gefächert und sie erfüllen vielfältige biologische Aufgaben.[3][4]
Als Beispiel für die biologische Funktion wären die Flavonoide zu nennen, welche für viele Arten einen Schutz gegen ultraviolette Strahlung und Blütenfarbstoffe darstellen.[5] oder aber das Biopolymer Lignin welches dem pflanzlichen Gewebe Stabilität gibt.[6]
Zimtsäuren
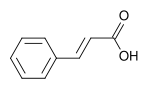
Eine zentrales Zwischenprodukt der meisten Phenylpropanoide stellen die Zimtsäure oder verschiedene Hydroxy- bzw. Methoxyzimtsäuren dar. In vielen Pflanzen stellen sie jedoch in Form von Konjugaten ein Endprodukt dar.[7] Das Vorkommen bestimmter Verbindungen ist dabei häufig auf eine bestimmte Anzahl Arten begrenzt.
Die Zimtsäuren werden biosynthetisch aus Phenylalanin mit Hilfe des Enzyms Phenylalanin-Ammoniak-Lyase (PAL) hergestellt. Eine Reihe von enzymatischen Hydroxylierungen und Methylierungen führt dann zu den Zimtsäurederivaten wie Cumarinsäure, Kaffeesäure, Ferulasäure, 5-Hydroxyferulasäure und 4-Hydroxy-3,5-dimethoxyzimtsäure. Die Ester dieser Zimtsäuren sind flüchtige Verbindungen mit herben oder blumigen Duft und dienen dem Anlocken von bestäubenden Insekten. Ein Beispiel hierfür ist der Zimtsäureethylester.
Zimtaldehyde and Monolignole
Die Reduktion der Carbonsäure-Gruppe in den Zimtsäuren führt zunächst zu den korrespondierenden Aldehyden wie Zimtaldehyd. Durch einen weiteren Reduktionschritt wird dann der entsprechende Alkohol wie Cumarylalkohol oder Coniferylalkohol hergestellt, welche Monolignole genannt werden. Diese Monolignole können zu Ligninen oder Suberinen polymerisieren welche als Zellwände von Pflanzen von Bedeutung sind.
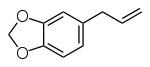
Die Phenylpropene wie Eugenol, Safrol und Estragol sind Derivate der Monolignole und sind Bestandteile von ätherischen Ölen.
Cumarine and Flavonoide
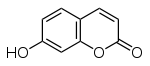
Die Hydroxylierung von Zimtsäure durch das Enzym Zimtsäure-4-Hydroxylase ergibt die p-Cumarinsäure welche durch eine weitere Hydroxylierung in 2-Stellung Umbelliferon ergibt. Die 2-hydroxylierten Verbindungen können nun über Cumaryl-CoA zu den Cumarinen cyclisiert werden. Flavonoide werden ebenfalls über die p-Cumarinsäure hergestellt. Zunächst wird aus Cumarinsäure das Cumaryl-CoA hergestellt. Mit Hilfe der Chalkonsynthase reagiert es mit drei Molekülen Malonyl-CoA zu Chalkon. Eine Isomerase überführt dieses dann in Flavon, aus welchem alle Flavonoide biosynthetisiert werden.
Stilbenoide
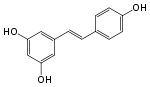
Stilbenoide wie etwa Resveratrol sind hydroxylierte Derivate von Stilben. Sie werden gebildet durch eine alternative Cyclisierung von Zimtsäure-CoA oder Cumaryl-CoA.
Einzelnachweise
- ↑ Phenylpropanoid biosynthesis – Reference pathway
- ↑ Overview of Phenylpropanoid Metabolism
- ↑ D. Strack: In: P.M. Dey, J.B. Harborne, editors. Plant Biochemistry; Academic Press San Diego California, USA 1997. p 387–416.
- ↑ G. Richter: In Stoffwechselphysiologie der Pflanzen. 6th ed.: Thieme Verlag, Stuttgart 1998, Chapter 8, Phenole; 365–90.
- ↑ L.G. Landry, C.C.S. Chapple, R. Last: In Arabidopsis mutants lacking phenolic sunscreens exhibit enhanced ultraviolet-B injury and oxidative damage. Plant Physiol 1995, 109, 1159–1166.
- ↑ C.F. Douglas: In Phenylpropanoid metabolism and lignin biosynthesis: from weeds to trees. Trends Plant Sci 1996,1 ,171–178.
- ↑ D. Strack, H.P. Mock: In P.M. Dey, J.B. Harborne, editors. Volume 9, methods in plant biochemistry: enzymes of secondary metabolism; Academic Press, San Diego California,USA 1993, 45–97.
Literatur
- G. Michal (Hrsg.): Biochemical Pathways – Biochemie-Atlas, 1. Auflage, Spektrum Akademischer Verlag, Heidelberg Berlin 1999, ISBN 3-86025-239-9.
- P. Nuhn: Naturstoffchemie: Mikrobielle, pflanzliche und tierische Naturstoffe, 2., neubearb. u. erw. A., Hirzel Verlag, Stuttgart 1997.
Wikimedia Foundation.