- Bowmansche Kapsel
-
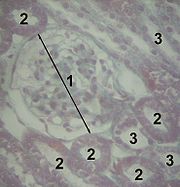
Das Nierenkörperchen (Corpusculum renale, Malpighi-Körperchen nach Marcellus Malpighi, 1628–1694) ist ein Teil des Nephrons. Es handelt sich um eine kugelige Struktur in der Rinde der Niere, die den Primärharn, ein Ultrafiltrat des Blutes, bildet. Es besteht aus einem kapillären Gefäßknäuel (Glomerulus oder Glomerulum), das von der Bowman-Kapsel (nach William Bowman, 1816–1892) umschlossen wird. Beide Strukturen bilden die Blut-Harn-Schranke.
Inhaltsverzeichnis
Gefäße
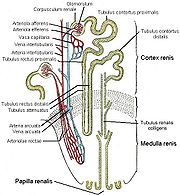
Man kann am Nierenkörperchen einen Gefäßpol mit genau einem zu- und wegführendem Blutgefäß und auf der anderen Seite einen Harnpol mit der Öffnung zum Tubulussystem unterscheiden. Das zuführende Gefäß für das Glomerulum ist die Arteriola glomerularis afferens (oder kurz das Vas afferens). Es entstammt der Nierenarterie (Arteria renalis) über eine Folge von Verzweigungen in Arteriae intralobulares, Arteriae arcuatae und Arteriae corticales radiatae, die schließlich das Vas afferens abgeben. Nach Passage des Kapillarbetts im Glomerulum fließt das Blut durch ein weiteres arterielles Gefäß, die Arteriola glomerularis efferens (oder kurz das Vas efferens) ab.
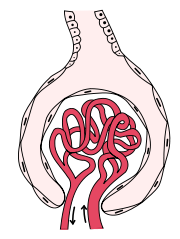
Das Vas afferens stülpt sich in die Bowman-Kapsel hinein, verzweigt sich und bildet dort ein Knäuel, das Glomerulum, welches bei genauerer Betrachtung aus ungefähr 30 verzweigten, anastomosierenden, aber parallelgeschalteten Kapillarschlingen besteht. Der Druckabfall bei der Passage des Blutes ist durch den parallelen Verlauf der Kapillaren nur gering.
An das Vas afferens ist der sogenannte juxtaglomeruläre Apparat angelagert. Es ist eine Kontaktstelle zum Tubulus desselben Nephrons, der zunächst zum Zentrum der Niere wegführt und dann schlaufenförmig in die Nähe seines Ausgangspunktes zurückkehrt. Hier spielen sich bedeutsame Regulationsvorgänge ab.
Das Vas efferens führt vom Glomerulum weg in Richtung Zentrum der Niere und bildet um das Tubulussystem des Nephrons, aus dem es entstammt, erneut ein Kapillargebiet.
Bowman-Kapsel
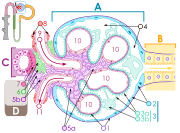
Die Bowman-Kapsel, auch Bowmansche Kapsel, besitzt zwei Schichten. Das äußere Blatt der Bowman-Kapsel umschließt das gesamte Nierenkörperchen. Es besteht aus einem dünnen, einschichtigen Plattenepithel. Das innere Blatt der Bowman-Kapsel liegt den Kapillaren direkt an. Die spezialisierten Zellen des inneren Blattes werden als Podozyten bezeichnet. Zwischen innerem und äußerem Blatt der Bowman-Kapsel entsteht ein schmales Lumen. Der filtrierte Anteil des Blutplasmas tritt durch die Blut-Harn-Schranke in dieses Lumen und fließt direkt durch die Öffnung der Kapsel in den sich anschließenden proximalen Tubulus.
Blut-Harn-Schranke
Die für die Funktion des Nierenkörperchens entscheidende Struktur ist die Blut-Harn-Schranke. Sie wird vom Kapillarendothel, den Podozyten und einer dazwischenliegenden, gemeinsamen Basalmembran gebildet. Die Schranke entscheidet darüber, welche Moleküle filtriert werden, und enthält hochspezialisierte Strukturen.
- Das Endothel ist vom diskontinuierlichen Typ. Die Fenster sind nicht (wie bei anderen gefensterten Endothelien) von einem Diaphragma verschlossen. Zudem besitzt es eine stark negativ geladene Glykokalix aus Sialoglykoproteinen.
- Die glomeruläre Basalmembran ist mit 300 Nanometern besonders dick und enthält zahlreiche negativ geladene Proteoglykane. Es handelt sich um die Basallaminae der Podozyten und des Kapillarendothels, die miteinander verschmolzen sind, so dass sich eine Lamina rara externa, Lamina densa und eine Lamina rara interna ausbildet. Der Lamina densa wird eine mechanische Barrierefunktion zugeschrieben.
- Die Podozyten besitzen primäre und sekundäre Verzweigungen. Zwischen diesen Fortsätzen ist eine Schlitzmembran ausgebildet. Die sehr feinen, außerordentlich zahlreichen, miteinander verzahnten Sekundärfortsätze bedecken von der Harnseite vollständig die Basalmembran. In den Schlitzen zwischen den verzahnten Füßchen befindet sich ein Schlitzdiaphragma (ähnlich den Adhärenskontakten, Protein Nephrin). Auch die Podozyten besitzen eine negativ geladene Glykokalix.
Die zahlreichen negativen Ladungen in allen Schichten der Blut-Harn-Schranke verhindert, dass zum Beispiel die bei pH 7,4 negativ geladenen Plasmaproteine filtriert werden (Ladungsselektivität). Außerdem sind Basalmembran, Podozyten und Schlitzmembran nur durchlässig für Moleküle bis zu einem Radius von acht Nanometern (ca. 70 kD) (Größenselektivität). Insgesamt ergibt sich eine Permselektivität des Filters nach Ladung und Größe, so dass zum Beispiel Albumin als wichtigstes Plasmaprotein mit 69 kD, negativer Gesamtladung und einem Molekülradius von 3,5 Nanometern nur in sehr geringem Ausmaß filtriert wird.
Abb. 5: Glomerulus im Rasterelektronenmikroskop (REM); die Bildbreite entspricht 115 µm.
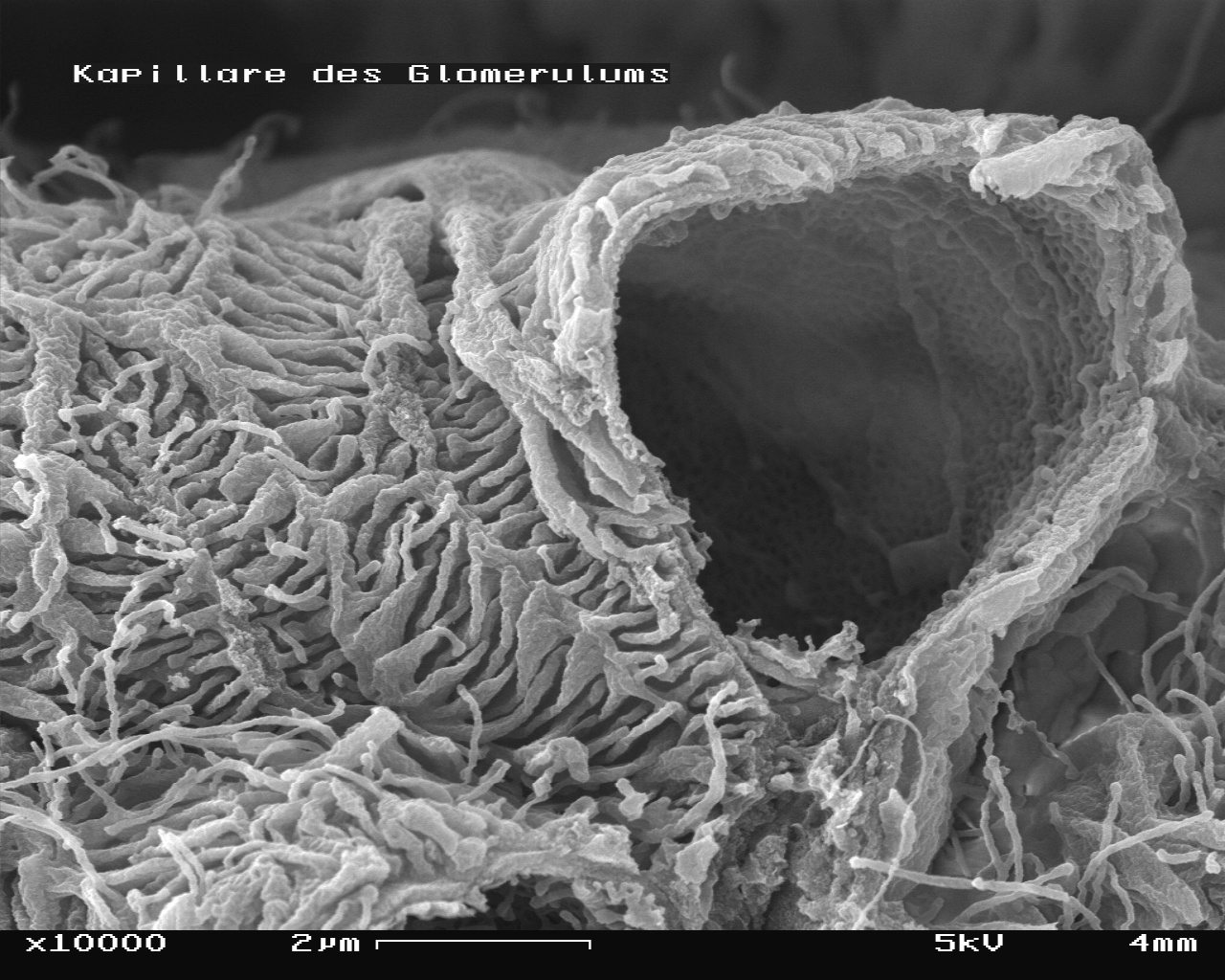
Abb. 7: Glomerulus mit gebrochener Kapillare im REM; die Bildbreite ist 11,5 µm groß.
Mesangium
Das Mesangium ist ein besonderes Bindegewebe innerhalb und außerhalb des Nierenkörperchens. Die so genannten Mesangiumzellen (Mesangiozyten) stützen die Kapillarwände, phagozytieren und sind auch an der Informationsweiterleitung bei Regulationsvorgängen (tubuloglomeruläres Feedback) beteiligt. Die extraglomerulären Mesangiumzellen sind Bestandteil des juxtaglomerulären Apparates.
Funktion
Pro Minute passieren 500 bis 800 Millilitern Blutplasma die Glomerula der Niere (Renaler Plasmafluss), wovon etwa 20 Prozent, also 90 bis 120 Milliliter pro Minute filtriert werden (Glomeruläre Filtrationsrate). Pro Tag werden so zwischen 180 und 200 Liter Primärharn gebildet. Davon werden 80 bis 90 Prozent in den proximalen Tubuli rückresorbiert. Die hormonregulierte Feinabstimmung erfolgt ADH-abhängig in den Hauptzellen der Sammelrohre, so dass insgesamt 99 Prozent des Wassers rückresorbiert werden.
Entscheidend für die Filtration ist die effektive Druckdifferenz zwischen Kapillaren und Bowman-Kapsel, die sich aus dem hydrostatischen und dem kolloidosmotischen Druck zusammensetzt. Während der Passage durch das Glomerulum nimmt der hydrostatische Druck praktisch nicht ab, denn durch den großen Gesamtquerschnitt der parallelgeschalteten Kapillaren ist der Widerstand gering. Da ein Ultrafiltrat abgepresst wird und die Plasmaproteine zurückbleiben, steigt während der Kapillarpassage kontinuierlich die Proteinkonzentration und somit der kolloidosmotische Druck, so dass der effektive Filtrationsdruck absinkt und am Ende Null erreicht, wenn das Filtrationsgleichgewicht erreicht wird.
Siehe auch
Weblinks
- Harnapparat – Blut-Harn-Schranke bei der Universität Freiburg, Abteilung für Anatomie
Wikimedia Foundation.