- Butan
-
Strukturformel 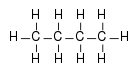
Allgemeines Name Butan Andere Namen - n-Butan
- R 600
Summenformel C4H10 CAS-Nummer 106-97-8 PubChem 7843 Kurzbeschreibung farbloses Gas Eigenschaften Molare Masse 58,12 g/mol Aggregatzustand gasförmig
Dichte 0,60 g·cm−3 (flüssig, am Siedepunkt)[1]
2,71 g·l−1 (gasförmig, 0 °C, 1013 hPa) [1]Schmelzpunkt −138,3 °C [1]
Siedepunkt −0,5 °C[1]
Dampfdruck Löslichkeit sehr schlecht in Wasser (61 mg/l bei 20 °C) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 
Hoch-
entzündlich(F+) R- und S-Sätze R: 12 S: (2)-9-16 MAK 2400 mg·m−3, 1000 ml/m3 [1]
WGK nicht wassergefährdend [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Butan ist die Bezeichnung für zwei gasförmige, farblose, gesättigte Kohlenwasserstoffe (Alkane), die in den zwei strukturisomeren Formen (n-)Butan CH3–CH2–CH2–CH3 und Methylpropan (Isobutan) CH(CH3)3 auftreten. Davon abgeleitet sind der Butyl- und Isobutyl-Rest (C4H9)–, die in vielen chemischen Verbindungen auftreten.
Inhaltsverzeichnis
Eigenschaften
Beide Butan-Isomere sind bei Raumtemperatur Gase, denn (n-)Butan hat einen Schmelzpunkt von −138 °C und einen Siedepunkt von −0,5 °C und Methylpropan (Isobutan) hat einen Schmelzpunkt von −160 °C und einen Siedepunkt von −12 °C. In Wasser ist Butan nahezu unlöslich (90 mg/l). Beide Isomere verhalten sich chemisch ähnlich: sie sind brennbar, entfärben Bromwasser und Kaliumpermanganatlösung nicht und werden von den Halogenen Chlor und Brom nur unter Lichteinfluss angegriffen. Der Explosionsbereich von n-Butan liegt in Luft zwischen der unteren Explosionsgrenze (UEG) von 1,4 Vol.-% (33 g/m3) und der oberen Explosionsgrenze (OEG) von 9,4 Vol.-% (231 g/m3).[1] Für Isobutan liegen diese Werte bei UEG mit 1,5 Vol.-% (37 g/m3 und OEG mit 9,4 Vol.-% (231 g/m3).[1]
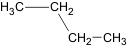
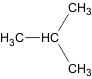
n-Butan i-Butan Verwendung und Herstellung
Butan und Methylpropan sind Flüssiggase, die bei der Erdöldestillation anfallen. Sie kommen im Erdöl und Erdgas vor.
Butan wird zur Herstellung von 1,3-Butadien und Maleinsäure und seit dem FCKW-Verbot als Treibgas in Sprays verwendet (Lebensmittelzusatzstoff E 943a[3]). . Beide Isomere werden als Brenngas in Tanks und Feuerzeugen, oft im Gemisch mit Propan, eingesetzt.
Butan wird trotz der Brennbarkeit wieder im Kühlschrank als Kältemittel eingesetzt (Kältemittelbezeichnung Butan R600 Methylpropan R600a), da die nicht brennbaren Fluorchlorkohlenwasserstoffe (FCKW) schädlich für die äußere Ozonschicht der Erdatmosphäre sind und die Ausbildung des Ozonlochs fördern. Als Kühlmittel im Gefrierbereich ist es wegen des Siedepunkts von −0,5 °C ungeeignet. Manche Solarkollektoren verwenden Methylpropan als Wärmeträger. Zur Verwendung in der Baubranche (Brenner) ist es ungeeignet, da bei niedrigen Temperaturen kein Gasdruck entsteht.
Auf Butylbasis werden Werkstoffe wie beispielsweise Alubutyl hergestellt.
Reaktionen
Unter idealen Bedingungen oxidiert Butan zu Kohlenstoffdioxid und Wasser.
Missbrauch als Droge
Butan wird als Rauschmittel wegen der hohen Verfügbarkeit und des geringen Preises verwendet. Die Wirkung ist mit ähnlichen Schnüffelstoffen zu vergleichen.[4]
Risiko
Beim Konsum kann es zu einer Sauerstoffunterversorgung kommen, die zu Übelkeit und Erbrechen, im schlimmsten Fall zu massiven Hirnschädigungen führt. Lebensgefahr bei Erhöhung des Gehirndrucks. Steigerung der Krampfanfälligkeit durch Senkung der Krampfschwelle. Psychische Abhängigkeit ist möglich. In geschlossenen kleinen Räumen (Auto) kann es zudem zu einem hochexplosivem Gas-Luftgemisch kommen.[5] Auch von Todesfällen wird berichtet.[6]
Einzelnachweise
- ↑ a b c d e f g h i j Eintrag zu Butan in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 22.12.2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 106-97-8 im European chemical Substances Information System ESIS
- ↑ ZZulV: Verordnung über die Zulassung von Zusatzstoffen zu Lebensmitteln zu technologischen Zwecken
- ↑ vgl. "Der plötzliche Schnüffeltod", in: die tageszeitung, 19. Juni 2008 [1]
- ↑ Jugendamt Nürnberg: Keine Flucht in die Sucht
- ↑ ad hoc news: 15-Jähriger kommt beim Schnüffeln ums Leben
Literatur
- Geert Oldenburg: Propan – Butan. Springer 1955, ASIN B0000BSW53
Weblinks
Wikimedia Foundation.

