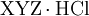- Chlorhydrat
-
Hydrochloride sind Salze von organischen Basen mit Salzsäure. Oft sind Hydrochloride Salze von primären, sekundären oder tertiären Aminen, die sich in einer Neutralisationsreaktion mit Salzsäure (HCl) bilden:
Die Reaktion verläuft analog der Reaktion von Ammoniak mit HCl, bei der sich Ammoniumchlorid (NH4Cl) bildet. Hydrochloride enthalten wie alle Chloride das Chlorid-Anion (Cl–) und sind daher Salze. Hydrochloride sind im Vergleich zu ihren Stammverbindungen (meist Amine) meist besser wasserlöslich und lassen sich leichter durch Umkristallisation reinigen. Die Hydrochloride von Aminen sind deutlich stabiler und resistenter gegenüber Alterung - erkennbar an Verfärbung - als die freien basischen Amine.
Bei komplizierten Molekülen mit mehreren basisch reagierenden funktionellen Gruppen (siehe Alkaloide, Lysin), bei denen sich die protonierte Gruppe nicht genau festlegen lässt, werden Hydrochloride oft so dargestellt:
Verwendung
Viele Arzneistoffe (Beispiele: Clenbuterol, Ethambutol, Fenoterol, Galantamin, Tramadol, Oxprenolol, Oxymetazolin, Oxytetracyclin, Pethidin, Phenylpropanolamin, Pilocarpin, Spectinomycin) werden als Hydrochloride eingesetzt, um im Magen-Darm-Trakt besser absorbiert werden zu können.
Analoge Salze
Die Hydrochloride zählen zur Stoffklasse der Hydrohalogenide. Dazu zählen weiterhin die Hydrofluoride, Hydrobromide und Hydroiodide.
Wikimedia Foundation.

![\mathrm{R-NH_2 +HCl \rightarrow \left[R-NH_3\right]^+ Cl^- }](/pictures/dewiki/51/31774aba6292403e88c03b71209b843a.png)