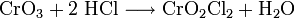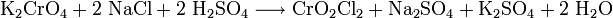- Chromyldichlorid
-
Strukturformel 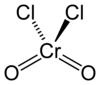
Allgemeines Name Chrom(VI)-oxiddichlorid Andere Namen - Chromyldichlorid
- Chromsäuredichlorid
- Chromoxychlorid
- Chromylchlorid
- Chromoxydichlorid
- Etards Reagenz
Summenformel Cl2CrO2 CAS-Nummer 14977-61-8 Kurzbeschreibung flüchtige, blutrote, an feuchter Luft rauchende Flüssigkeit Eigenschaften Molare Masse 154,90 g/mol Aggregatzustand flüssig
Dichte 1,912 g/cm3[1]
Schmelzpunkt -96,5 °C[1]
Siedepunkt 116,7 °C[1]
Dampfdruck 18,4 mbar bei 20°C [1]
Löslichkeit heftige Zersetzung in Wasser, löslich in anorganischen Säurechloriden und organischen Flüssigkeiten
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 



Brand-
förderndGiftig Ätzend Umwelt-
gefährlich(O) (T) (C) (N) R- und S-Sätze R: 8-35-43-46-49-50/53 S: 45-53-60-61 WGK 3[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Chrom(VI)-oxiddichlorid ist eine chemische Verbindung aus der Gruppe der Metalloxide bzw. Chlorverbindungen. Sie liegt in Form einer flüchtigen, blutroten, an feuchter Luft rauchenden Flüssigkeit vor.
Inhaltsverzeichnis
Gewinnung und Darstellung
Chrom(VI)-oxiddichlorid kann durch Reaktion von Chlorwasserstoff mit Chromsäure bzw. Chromtrioxid hergestellt werden.
Weiterhin kann es durch Reaktion von Kaliumchromat mit Natriumchlorid und Schwefelsäure hergestellt werden.[3]
Eigenschaften
Chrom(VI)-oxiddichlorid ist stark elektrophil und wirkt oxidierend. Es zersetzt sich in Wasser heftig, wobei Salzsäure- oder Chlordämpfe, sowie Chromsäure und Chromtrioxid entstehen. Die Dämpfe der Verbindung sind 5,35 mal schwerer als Luft.
Verwendung
Chrom(VI)-oxiddichlorid wird als Oxidationsmittel (z.B. bei der Umsetzung von Alkenen zu Aldehyden), in der Gerberei als Beizmittel und als Nachweismittel für Chlor verwendet.
Sicherheitshinweise
Chrom(VI)-oxiddichlorid ist als krebserzeugend und erbgutverändernd Kategorie 2 eingestuft. Sie selbst brennt nicht, ist jedoch stark brandfördernd.
Verwandte Verbindungen
- Chromylfluorid CrO2F2
Quellen
- ↑ a b c d e Eintrag zu CAS-Nr. 14977-61-8 in der GESTIS-Stoffdatenbank des BGIA (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 14977-61-8 im European chemical Substances Information System ESIS
- ↑ Georg Brauer, Handbuch der Präparativen Anorganischen Chemie, ISBN 3-432-02328-6
Wikimedia Foundation.