- E 650
-
Strukturformel 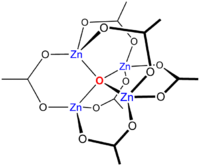
Allgemeines Name Zinkacetat Andere Namen - E650
Summenformel - C4H6O4Zn (wasserfrei)
CAS-Nummer - 557-34-6 (wasserfrei)
- 5970-45-6 (Dihydrat)
ATC-Code A16AX05
Kurzbeschreibung farbloser kristalliner Feststoff Eigenschaften Molare Masse - 183,48 g·mol−1 (wasserfrei)
- 219,50 g·mol−1 (Dihydrat)
Aggregatzustand fest
Dichte 1,74 g/cm3[1]
Schmelzpunkt Löslichkeit gut löslich in Wasser (430 g/l[1])
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Gesundheits-
schädlich(Xn) R- und S-Sätze R: 22 S: 24/25 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln WGK 3 (stark wassergefährdend)[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Zinkacetat ist das Zinksalz der Essigsäure, welches in Kaugummi als Geschmacksverstärker eingesetzt und dort mit der E-Nummer E650 gekennzeichnet wird. Bei Zinkacetat handelt es sich um eine Zinkverbindung, die gut vom Darm in die Blutbahn resorbiert wird. Somit dient dieser unter anderem als Zinklieferant für den Organismus.
Inhaltsverzeichnis
Chemische Eigenschaften
Basisches Zinkacetat
Beim Erhitzen von Zn(CH3CO2)2 im Vakuum wird Acetanhydrid abgespalten und es entsteht ein „basisches Zinkacetat“ der Formel Zn4O(CH3CO2)6. Es wird die unten abgebildete Clusterverbindung mit einer tetraedrischen Struktur gebildet, die dem analogen Berylliumsalz ähnelt.[2]
Verwendung
Zinkacetat ist ausschließlich in Kaugummi als Geschmacksverstärker zugelassen. Die Menge an Zinkacetat in der Kaugummimasse ist auf 1 g/kg beschränkt.[3]
Zinkacetat soll, ähnlich wie Zinkglukonat, in Hustenbonbons verabreicht durch eine lokale Wirkung im Hals die Dauer von Erkältungen verkürzen.[4]
Quellen
- ↑ a b c d e Eintrag zu Zinkacetat in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 11.11.2007 (JavaScript erforderlich)
- ↑ H. Koyama, Y. Saito: The Crystal Structure of Zinc Oxyacetate, Zn4O(CH3COO)6, in: Bull. Chem. Soc. Jpn. 1954, 27, 112–114.
- ↑ Lebensmittelzusatzstoffe
- ↑ G. Eby. Zinc Lozenges: Cold Cure or Candy? Solution Chemistry Determinations, Bioscience Reports, 2004, Volume 24, No.1, February 2004. Deutscher Bericht über die Veröffentlichung
Wikimedia Foundation.
