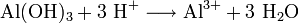- Al(OH)3
-
Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Aluminiumhydroxid Andere Namen - Hydrargillit
- Bayerit
- Böhmit
- Diaspor
- Nordstrandit
- Tonerdehydrat
Verhältnisformel Al(OH)3 · x H2O CAS-Nummer 21645-51-2 ATC-Code A02AB01
Kurzbeschreibung Weißer Feststoff Eigenschaften Molare Masse 78,00 g/mol Aggregatzustand fest
Dichte 2,42 g·cm−3[1]
Schmelzpunkt 300 °C (Kristallwasserabgabe)[1]
Dampfdruck < 0,1 hPa (20 °C)[1]
Löslichkeit schlecht (0,0015 g/l) in Wasser, unlöslich in Ethanol[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln MAK - 1,5 mg·m−3 (für Alveolengängigen Staubanteil)
- 4 mg·m−3 (für einatembaren Staubanteil)[1]
Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Das Aluminiumhydroxid, Summenformel Al(OH)3, wird nach seinen Erscheinungsformen unterschieden und hat amphoteren Charakter.
Inhaltsverzeichnis
Modifikationen
Vom Aluminiumorthohydroxid Al(OH)3 sind drei Modifikationen bekannt:
- monoklin, γ-Al(OH)3: Bekannt als Mineral Gibbsit (Hydrargillit)
- hexagonal, β-Al(OH)3: Bekannt als Mineral Bayerit
- triklin: Bekannt als Mineral Nordstrandit
Weiterhin existiert das wasserärmere Aluminiummetahydroxid (Aluminiumoxidhydroxid) AlO(OH) von dem folgende Variationen existieren:
- orthorhombisch, α-AlO(OH): Bekannt als Mineral Diaspor
- orthorhombisch, γ-AlO(OH): Bekannt als Mineral Böhmit
Vorkommen
Die Aluminiumhydroxid-Modifikationen Hydrargillit und Bayerit kommen in der Natur als Bestandteile des Bauxits vor.
Synthese
Durch Fällung von Aluminiumhydroxid mit Ammoniak in wässriger Aluminiumsalzlösung erhält man eine als Aluminiumoxidhydrat bezeichnete amorphe und voluminöse Form, die sich über die Zeit langsam über Bayerit und Böhmit in den thermodynamisch stabilen Hydrargillit wandelt. Durch Erhitzung von Hydrargillit auf 300 °C wird eine teilweise Entwässerung zu kristallisiertem Böhmit bewirkt. Diaspor wird dargestellt, indem Böhmit in wässriger Natronlauge unter Druck (50 MPa) auf 380 °C erhitzt wird.
Wird Kohlenstoffdioxid in eine Natriumaluminatlösung eingeleitet, bildet sich bei 80 °C kristallines α-Al(OH)3. Bei geringerer Temperatur würde zunächst Bayerit entstehen, der allmählich in α-Al(OH)3 übergeht.
Großtechnisch wird Aluminiumhydroxid aus Bauxit durch Aufschluss mit Natronlauge nach dem Bayer-Verfahren hergestellt. Größter Hersteller war in Deutschland die VAW (Vereinigte Aluminiumwerke AG). Heute wird Aluminiumhydroxid großtechnisch in Deutschland nur noch von der (AOS) Aluminium Oxid Stade GmbH produziert.
Werden die verschiedenen Aluminiumhydroxidformen durch starkes Erhitzen dehydriert (calciniert), erhält man Aluminiumoxid Al2O3.Reaktionsverhalten
Unter Einwirkung von Basen wird Aluminiumhydroxid in Aluminate überführt:
In Säuren reagiert es zu den entsprechenden Aluminiumsalzlösungen.
Die Reaktionsgeschwindigkeit ist dabei abhängig von der beteiligten Modifikation, so ist die Löslichkeit in Säuren bei amorpher Struktur wesentlich größer als bei kristalliner Form.
Verwendung
Aluminiumhydroxid tritt als Bayerit und Hydrargillit als Zwischenprodukte bei der Aluminiumgewinnung nach dem Bayer-Prozess in Erscheinung und wird dort als Nebenprodukt („Feuchthydrat“) gewonnen und als Rohstoff zur Herstellung diverser Al-Verbindungen in der Industrie verwendet, z. B. Herstellung von Natriumaluminat-Lösung oder Polyaluminiumchlorid.
Aluminiumhydroxid (Hydrargillit, auch ATH von Aluminiumtrihydrat genannt) ist das weltweit bedeutendste mineralische Flammschutzmittel. Es zeichnet sich besonders durch seine Umweltfreundlichkeit (halogenfrei) und Effizienz als Rauchgasunterdrückungsmittel aus.
In der Medizin wird Aluminiumhydroxid bei Dialysepatienten als Phosphatbinder eingesetzt. Dabei zeigte sich bei längerem Einsatz eine zerebrale Toxizität (Demenz), ebenso eine Knochentoxizität, weshalb ein Einsatz von höchstens vier Wochen empfohlen wird. Auch als Adjuvans bei Toxoidimpfstoffen wird Aluminiumhydroxid zur Wirkungsverstärkung angewendet.
Außerdem dienen Aluminiumhydroxidsteinchen einer Sexualpraktik in Afrika. Durch Einführen in die Vagina wird die Vaginalschleimhaut ausgetrocknet, was den Lustgewinn des Mannes steigern soll („Trockener Sex“).
Quellen
- ↑ a b c d e f Eintrag zu Aluminiumhydroxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 23.12.2007 (JavaScript erforderlich)
Literatur
- Martin Okrusch, Siegfried Matthes: Mineralogie. 7. Auflage. Springer Verlag, Berlin 2005, ISBN 3-540-23812-3
Wikimedia Foundation.


![\mathrm{Al(OH)_3 + OH^- \longrightarrow [Al(OH)_4]^-}](/pictures/dewiki/97/af0d3da0fb01afc653c446a5187038b4.png)