- Genmodifikation
-
 GloFish ist der Handelsname von gentechnisch veränderten Zebrabärblingen mit kräftigen rot, grün oder orange fluoreszierenden Farben. Obwohl sie ursprünglich nicht für kommerzielle Zwecke erzeugt wurden, sind sie die ersten gentechnisch veränderten Tiere, die als Haustiere erhältlich sind.
GloFish ist der Handelsname von gentechnisch veränderten Zebrabärblingen mit kräftigen rot, grün oder orange fluoreszierenden Farben. Obwohl sie ursprünglich nicht für kommerzielle Zwecke erzeugt wurden, sind sie die ersten gentechnisch veränderten Tiere, die als Haustiere erhältlich sind.Als Gentechnik bezeichnet man jene Methoden und Verfahren der Biotechnologie, welche auf den Kenntnissen der Molekularbiologie und Genetik aufbauen und gezielte Eingriffe in das Erbgut (Genom) und damit in die biochemischen Steuerungsvorgänge von Lebewesen bzw. viraler Genome ermöglichen. Als Produkt entsteht zunächst rekombinante DNA, mit der wiederum gentechnisch veränderte Organismen (GVO) hergestellt werden können. Der Begriff Gentechnik umfasst also die Veränderung und Neuzusammensetzung von DNA-Sequenzen im Reagenzglas oder in lebenden Organismen sowie das künstliche Einbringen von DNA in lebende Organismen.[1]
Gentechnik wird zur Herstellung neu kombinierter DNA innerhalb einer Art[2], vor allem aber auch über Art-Grenzen hinweg verwendet. Dies ist möglich, weil alle Lebewesen einen genetischen Code benutzen, von dem nur in wenigen Ausnahmefällen leicht abgewichen wird (siehe codon usage). Ziele gentechnischer Anwendungen sind beispielsweise die Verbesserung von Kulturpflanzen, die Herstellung von Medikamenten oder die Gentherapie.
Obwohl es große Gemeinsamkeiten zwischen den verwendeten Methoden gibt, wird häufig nach Anwendungsbereich differenziert:
- Grüne Gentechnik bzw. Agrogentechnik - Anwendung bei Pflanzen
- Rote Gentechnik - Anwendung bei Organismen mit rotem Blut (Wirbeltiere) oder Zellen aus diesen Organismen, in der Medizin und Pharmazeutik
- Weiße/Graue Gentechnik - Anwendung bei Industrieprozessen, grau speziell in der Abfallwirtschaft
Inhaltsverzeichnis
Bedeutung
Nutzpflanzen
Bei der Veränderung von Nutzpflanzen werden beispielsweise Resistenzen gegen Herbizide (z. B. Glyphosat oder Glufosinat) oder Resistenzen gegen Schädlinge eingebaut. Bei diesem Verfahren besteht das Risiko, dass die veränderten Gene ungewollt auf andere Wildtyp-Pflanzen derselben Art oder verwandte Arten übertragen werden.[3] In welchem Maße und unter welchen Bedingungen dieser Gendrift bzw. horizontale Gentransfer stattfindet, wird derzeit untersucht.[4][5] Problematisch ist dabei nicht nur, dass es zum Auskreuzen von Resistenzen kommen kann, insbesondere da Antibiotikaresistenz-Marker genutzt werden,[6] sondern auch dass Veränderungen auftreten können, die die Fruchtbarkeit der Wildtypen und damit die Biodiversität gefährden.[7] Die von GVO produzierten Proteine können außerdem, gewollt oder ungewollt,[8] Variationen bekannter Proteine sein, über deren Auswirkungen auf den Verbraucher keine Langzeitstudien existieren.[9] Neben Fragen über das geistige Eigentum an Genen, sind dies Hauptgründe für Kritik an der Gentechnik.
Medizin und Pharmazie
Etliche Produkte, die für den Menschen interessant sind (zum Beispiel Insulin, Vitamine), werden mit Hilfe gentechnisch veränderter Bakterien hergestellt. Auch für die Medizin hat die Gentechnik Bedeutung erlangt, die Zahl der gentechnisch hergestellten Medikamente auf dem Markt nimmt stetig zu. Mit Stand 2008 sind in Deutschland 134 Arzneimittel mit 98 verschiedenen gentechnisch erzeugten Wirkstoffen zugelassen.[10] Sie werden bei zahlreichen Krankheiten eingesetzt, etwa Zuckerkrankheit, Blutarmut, Herzinfarkt, Wachstumsstörungen bei Kindern, verschiedenen Krebsarten und der Bluterkrankheit. Weltweit befinden sich über 350 Gentech-Substanzen in klinischen Prüfungen mit Patienten.
Insulin ist das bekannteste Hormon, das mit Hilfe der Gentechnik gewonnen wurde. Das früher verwendete Insulin stammte von Rindern und Schweinen und war nicht hundertprozentig baugleich mit dem des Menschen. Mittels Gentechnik wurde es nun ersetzt und löste u.a. die Probleme von Diabetikern mit einer Unverträglichkeit gegenüber Tierinsulin.[11]
Auch in der Krebstherapie sind gentechnisch hergestellte Medikamente heute etabliert. Nach Meinung einiger Krebsexperten könnten durch den Einsatz von Interferon[12] und blutbildenden Wachstumsfaktoren[13] die Krebstherapien bei bestimmten Tumorarten verbessert, Krankenhausaufenthalte verkürzt oder gar vermieden sowie Lebensqualität gewonnen werden. Auch das Infektionsrisiko sei nachweislich gesunken.
Ansätze zur gentechnischen Veränderung von Zellen im menschlichen Körper zu Heilungszwecken werden im Artikel Gentherapie beschrieben.
Geschichte
Bereits vor 8000 Jahren wurde im heutigen Mexiko durch Züchtung das Erbgut von Teosinte-Getreide durch die Kombination von natürlich vorkommenden Mutationen so verbessert, dass die Vorläufer der heutigen Mais-Sorten entstanden. Dadurch wurde nicht nur der Ertrag erhöht, sondern auch eine Pilzresistenz entwickelt.[14]
Künstliche Mutationen für Züchtungszwecke wurden innerhalb der konventionellen Landwirtschaft erzeugt, in dem Keime stark ionisierender Strahlung oder anderen genverändernden Einflüssen (Mutagenen) ausgesetzt wurden, um Mutationen im Erbgut häufiger als unter natürlichen Bedingungen hervorzurufen.[15] Samen wurden ausgesät und jene Pflanzen, die die gewünschten Eigenschaften besaßen, wurden weiter gezüchtet. Ob dabei auch noch andere, unerwünschte, Eigenschaften entstanden, wurde nicht systematisch überprüft. Diese Technik wurde bei fast allen Nutzpflanzen und auch bei einigen Tierarten angewendet, jedoch lag der Erfolg der Mutationszüchtung bei Pflanzen nur zwischen 0,5 - 1% an züchterisch brauchbaren Mutanten, bei Tieren ist diese Methode überhaupt nicht zu gebrauchen.[16]
Bei diesen Vorläufern der Gentechnik enthielt der veränderte Organismus jedoch keine rekombinante DNA.
 Autoradiographie eines Sequenziergels. Die dargestellte DNA wurde mit 32P (Phosphor) radioaktiv markiert.
Autoradiographie eines Sequenziergels. Die dargestellte DNA wurde mit 32P (Phosphor) radioaktiv markiert.Die eigentliche Geschichte der Gentechnik begann, als es Ray Wu und Ellen Taylor 1971 gelang, mit Hilfe von 1970 entdeckten Restriktionsenzymen,[17] eine Sequenz von 12 Basenpaaren vom Ende des Genoms eines Lambda Virus abzutrennen.[18] Zwei Jahre später erzeugte man das erste genetisch veränderte rekombinante Bakterium, indem ein Plasmid mit vereinter viraler und bakterieller DNA in das Darmbakterium Escherichia coli eingeschleust wurde.[19] Angesichts dieser Fortschritte fand im Februar 1975 die Asilomar-Konferenz in Pacific Grove, Kalifornien, statt. Auf der Konferenz diskutierten 140 Molekularbiologen aus 16 Ländern Sicherheitsauflagen, unter denen die Forschung weiter stattfinden sollte.[20] Die Ergebnisse waren Grundlage für staatliche Regelungen in den Vereinigten Staaten und später in vielen anderen Staaten.[21] 1977 gelang erstmals die gentechnische Herstellung eines menschlichen Proteins in einem Bakterium.[22] Im selben Jahr entwickelten Walter Gilbert, Allan Maxam[23] und Frederick Sanger[24] unabhängig voneinander Methoden zur effizienten DNA-Sequenzierung, für die sie 1980 mit dem Nobelpreis für Chemie ausgezeichnet wurden. Ende der 1970er Jahre entdeckten die Belgier Marc Van Montagu und Jeff Schell die Möglichkeit, mittels Agrobacterium tumefaciens Gene in Pflanzen einzuschleusen und legten damit den Grundstein für die Grüne Gentechnik.[25]
1980 beantragte Ananda Chakrabarty in den USA das erste Patent auf einen GVO, dessen Zulassungsverfahren bis vor den Supreme Court getragen wurde. Dieser entschied 1981, dass der Fakt, dass Mikro-Organismen lebendig sind, keine gesetzliche Bedeutung für den Zweck des Patent-Rechtes habe und machte damit den Weg für die Patentierung von Lebewesen frei.[26] 1982 kam in den Vereinigten Staaten mit Insulin das erste gentechnisch hergestellte Medikament auf den Markt.[22] 1982 wurde mit dem Bakteriophagen Lambda das erste Virus in seiner vollständigen DNA-Sequenz veröffentlicht.[27] Im Jahr 1983 entwickelte Kary Mullis die Polymerase-Kettenreaktion, mit der DNA-Sequenzen vervielfältigt werden können und erhielt dafür 1993 den Chemie-Nobelpreis.[28] 1985 wurden genetisch manipulierte Pflanzen in den USA patentierbar und es erfolgte die erste Freisetzung genetisch manipulierter Bakterien (ice minus bacteria).[14] 1988 wurde das erste Patent für ein gentechnisch verändertes Säugetier, die sogenannte Krebsmaus, vergeben.[29]
Ab Herbst 1990 wurde im Humangenomprojekt damit begonnen, das gesamte Genom des Menschen zu sequenzieren. Im September desselben Jahres wurde die weltweit erste Gentherapie an einem Menschen durchgeführt. Im Jahr 1994 kamen im Vereinigten Königreich und den Vereinigten Staaten gentechnisch veränderte Flavr-Savr-Tomaten, auf den Markt.
1996 führte in Deutschland der Import von Sojabohnen, die einen nachweisbaren Anteil von gentechnisch veränderten Sojabohnen enthielten, zu ersten öffentlichen Kontroversen über die Verwendung von Gentechnologie in der Landwirtschaft.[30]
Die Firma Celera und International Genetics & Health Collaboratory behaupten 2001, das menschliche Genom, parallel zum Humangenomprojekt, vollständig entschlüsselt zu haben.[14] Jedoch war die Sequenzierung nicht vollständig. Ein Jahr später wurde der erste in seiner Keimbahn gentechnisch veränderte Primat geboren.
Techniken nach Anwendungsbereich
Grüne Gentechnik (Agrogentechnik)
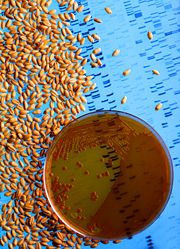 Elemente der Gentechnik: Bakterienkultur in einer Schale, Saatgut und durch Elektrophorese sichtbar gemachte DNA-Fragmente
Elemente der Gentechnik: Bakterienkultur in einer Schale, Saatgut und durch Elektrophorese sichtbar gemachte DNA-Fragmente→ Hauptartikel: Grüne Gentechnik, Grüne Biotechnologie
Da die Funktion der überwiegenden Gene in Pflanzen unbekannt ist, muss man, um sie zu erkennen, die Steuerung des Gens modifizieren. Dabei werden Effekte von Genen normalerweise durch einen Vergleich dreier Pflanzenpopulationen aufzuklären versucht (Wildtyp, Überexpressoren und „Knock out“-Population). Hierfür gibt es verschiedene Techniken, wie etwa RNAi. Allen Techniken ist gemein, dass sie doppelsträngige RNA produzieren, die der Pflanze den „Befehl“ gibt, „normale“ Ribonukleinsäure des zu untersuchenden Gens abzubauen.
Außerdem gehören auch deskriptive Techniken zur Standardausrüstung der gentechnischen Pflanzenforschung. Dabei werden Gene kloniert, dann bestimmt man die Häufigkeiten von Transkripten (Bauanleitungen für Proteine) oder mittels so genannter DNA-Chips gleich die meisten Gene einer Pflanze in ihrer Ablesehäufigkeit.
Der Agrobakterium-vermittelte Gentransfer ist ebenfalls eine wichtige Technik. Bei dieser gentechnischen Methode werden einzelne Erbfaktoren von Zellen eines Organismus in Zellen eines anderen Lebewesens übertragen.[25]
Die somatische Hybridisierung wiederum erlaubt es, gewünschte Merkmale verschiedener Elternpflanzen zu kombinieren. Im Vergleich zum Agrobakterium-vermittelten Gentransfer müssen hierbei keine spezifischen Gene identifiziert und isoliert werden. Außerdem wird damit die Einschränkung der Transformation (Gentransfer) überwunden, nur wenige Gene in einen vorgegebenes Erbgut einführen zu können. Auch kann bei der Zellfusion die Chromosomenzahl der Zellen multipliziert werden, also die Anzahl der Chromosomensätze (Ploidiegrad) erhöht werden. Dies kann die Ertragsfähigkeit von Pflanzen steigern (Heterosiseffekt). Molekulare Marker oder biochemische Analysen werden genutzt, um aus der somatischen Hybridisierung hervorgegangene Pflanzen zu charakterisieren und zu selektieren.
Rote Gentechnik
→ Hauptartikel: Rote Biotechnologie
Eine gentechnische Methode der roten Biotechnologie ist die Gentherapie. Hier wird davon ausgegangen, dass Krankheiten durch defekte Gene verursacht werden, welche man versucht zu ersetzen. Bei Ansätzen der in vitro Gentherapie werden dem Patienten Zellen entnommen, gentechnisch verändert und dann dem Patienten wieder zugeführt. Bei Ansätzen der in vivo Gentherapie wird der Patient direkt mit der Korrektur-DNA in einem Vektor (z.B. Retroviren) behandelt, die die DNA mit dem Genom der Zielzellen in Kontakt bringen soll.
Biotechnologische Medikamente werden durch transgene Organismen (Mikroorganismen, Nutztiere oder Pharmapflanzen) hergestellt. Dabei wird iterativ so lange verändert bis ein Wirkstoff entsteht, der die Krankheit heilen kann.
Weiße Gentechnik
→ Hauptartikel: Weiße Biotechnologie
Durch gelenkte Evolution (Molecular farming) werden hier Stämme von mutierten Mikroorganismen erzeugt und aufgrund ihrer Erträge der gewünschten Produkte, welche durch ein Screening festgestellt wurden, selektiert. Dieser Vorgang wird in iterativen Zyklen wiederholt, bis die angestrebten Veränderungen erreicht sind. Zur Identifizierung von nicht kultivierbaren Organismen untersucht man Metagenome, d. h. die Gesamtheit der Genome eines Lebensraums, Biotops oder einer Lebensgemeinschaft (Biozönose). In Metagenomen können beispielsweise Biokatalysatoren aufgefunden werden, die bisher noch nicht bekannte biochemische Reaktionen katalysieren und neue, interessante Stoffwechselprodukte bilden.
Zum Einschleusen von Plasmid-DNA in die Bakterie wird u. a. die Eigenschaft von Calciumchlorid genutzt, Zellmembranen durchlässig zu machen.[14]
Rechtliche Situation
Kennzeichnungspflicht für gentechnisch veränderte Produkte in der EU
Seit dem 18. April 2004 besteht innerhalb der EU eine Kennzeichnungspflicht für gentechnisch veränderte Produkte. Sie schließt ein, dass alle Produkte, die eine genetische Veränderung besitzen, gekennzeichnet werden müssen, auch dann, wenn die Veränderung im Endprodukt nicht mehr nachweisbar ist. Ausgenommen von der Kennzeichnungspflicht sind Fleisch, Eier und Milchprodukte von Tieren, die mit gentechnisch veränderten Pflanzen gefüttert wurden sowie Produktzusätze, die mithilfe genetisch veränderter Bakterien hergestellt wurden. Ebenso Enzyme, Zusatzstoffe und Aromen, da sie im rechtlichen Sinne nicht als Lebensmittel gelten.
Kritiker von gentechnisch veränderten Lebensmitteln verweisen in diesem Zusammenhang darauf, dass derzeit (Stand: 2005) etwa 80 Prozent der angebauten gentechnisch veränderten Pflanzen in die Futtermittelindustrie einfließen. Sie fordern deshalb die Kennzeichnungspflicht auch für diese tierischen Produkte.
Eine Kennzeichnung muss weiterhin nicht erfolgen, wenn die Verunreinigung mit genetisch verändertem Material unter 0,9 % (Stand: 2008) Gewichtsprozent liegt und zufällig oder technisch unvermeidbar ist. Dabei ist jede Einzelzutat eines Lebens- oder Futtermittels getrennt zu betrachten. 2007 wurde eine neue EU-Öko-Verordnung verabschiedet, die ab 2009 Gültigkeit erlangt. Mit ihr wird die Möglichkeit geschaffen, dass Zusatzstoffe für Lebens- oder Futtermittel, die A) grundsätzlich im Ökolandbau zugelassen sind und B) nachweislich nicht in GVO-freier Qualität verfügbar sind, auch dann eingesetzt werden dürfen, wenn sie durch gentechnisch veränderte Mikroorganismen hergestellt wurden. Die Interpretation der neuen Regel steht noch aus. Derzeit ist nach der neuen Regel kein Stoff zugelassen.
Situation in Deutschland
Gesetzlich werden Haftung, Strafvorschriften und Definitionen in Bezug auf die Gentechnik durch das 1990 erlassene deutsche Gentechnikgesetz geregelt. Der zweite Teil dieses Gesetzes definiert die Sicherheitsstufen und -maßnahmen an Arbeitsplätze für gentechnische Arbeiten.[31] Die Einstufung erfolgt dabei nach Risiko für die menschliche Gesundheit und Umwelt in 4 Sicherheitsstufen:
Stufe Beschreibung S1 Gentechnische Arbeiten, bei denen nach dem Stand der Wissenschaft nicht von einem Risiko für die menschliche Gesundheit und die Umwelt auszugehen ist S2 Gentechnische Arbeiten, bei denen nach dem Stand der Wissenschaft von einem geringen Risiko für die menschliche Gesundheit oder die Umwelt auszugehen ist S3 Gentechnische Arbeiten, bei denen nach dem Stand der Wissenschaft von einem mäßigen Risiko für die menschliche Gesundheit oder die Umwelt auszugehen ist S4 Gentechnische Arbeiten, bei denen nach dem Stand der Wissenschaft von einem hohen Risiko oder dem begründeten Verdacht eines solchen Risikos für die menschliche Gesundheit oder die Umwelt auszugehen ist Bei der Zuordnung wird nach Anhörung einer Kommission im Zweifel die höhere Sicherheitsstufe gewählt.
Den genauen Umgang mit gentechnisch veränderten Organismen, regelt die Gentechnik-Sicherheitsverordnung.[32] Ein Gesetz zur Neuordnung des Gentechnikrechts wurde im Juni 2004 erlassen, um die EU-Richtlinie zur Freisetzung von GVOs umzusetzen.
Die Möglichkeit der Kennzeichnung „ohne Gentechnik“ wird derzeit durch die „Neuartige-Lebensmittel-Verordnung“[33] geregelt. Die Große Koalition novelliert die Regelung im ersten Quartal 2008. Sie wird künftig nicht mehr in einer Verordnung sondern im EG-Gentechnik-Durchführungsgesetz festgeschrieben. Kern der Novelle sind Vereinfachungen bei der Auslobung von Fleisch, Milch und Eiern, die mit Futtermitteln erzeugt wurden, die nicht unter die EU-Kennzeichnungsregeln fallen. Damit wird eine Kennzeichnungslücke, die aufgrund der EU-Kennzeichnungsregeln besteht, geschlossen.
Während SPD, der ehemalige Bundeslandwirtschaftsminister Horst Seehofer, Verbraucherzentrale Bundesverband und etliche gentechnikkritische Verbände die neuen Regeln begrüßen, sprechen sich die Fraktion der CDU/CSU, Futtermittelverband, Bauernverband, Raiffeisen und andere dagegen aus. Sie kritisieren an der neuen Regel, dass nicht jegliche Berührung der Produkte mit GVO zum Verlust der Kennzeichnung führen.
Eine juristische Leerstelle besteht weiterhin in Bezug auf die Beeinflussung anderer Lebensmittel, mit schwerwiegenden Folgen. So verfügte das Augsburger Verwaltungsgericht am 4. Mai 2007, dass der Freistaat Bayern die Pollen einer auf einem seiner Versuchsfelder angebauten Bt-Maissorte MON 810 unschädlich zu machen habe, da sonst der Honig eines benachbarten Imkers verkehrs- und genußuntauglich und damit unverkäuflich geworden wäre.[34] Als Folge des Widerspruchs, durch den Freistaat Bayern, entschied das Gericht jedoch, dass mobile potentielle Geschädigte (Bienen/Imker) dem immobilen Risikoverursacher (Maisfeld) auszuweichen haben. [35] Jener Mais ist zwar von der Bundesregierung als unbedenklich eingestuft,[36] jedoch vom Bundesamt für Verbraucherschutz und Lebensmittelsicherheit für umweltgefährlich erklärt und darf deshalb nur unter Auflagen und nur für Tierfutter in Deutschland angebaut werden.[37]
Andere Länder
In Österreich wurde im April 1997 das Gentechnik-Volksbegehren[38] angenommen. Das bisher (April 2007) zweiterfolgreichste Volksbegehren der Zweiten Republik mit einer Beteiligung von über 21 % der Wahlberechtigten fordert ein gesetzlich verankertes Verbot der Produktion, des Imports und des Verkaufs gentechnisch veränderter Lebensmittel, ein ebensolches Verbot der Freisetzungen genetisch veränderter Pflanzen, Tiere und Mikroorganismen, sowie ein Verbot der Patentierung von Lebewesen. Der Beschluß wurde am 16. April 1998 nach 3. Lesung angenommen.[39][40] Der Verkauf von Saatgut mit einem Anteil von mehr als 0,1 % genmanipulierter Organismen ist seit Januar 2002 verboten. EU-Bestrebungen, höhere Toleranzwerte durchzusetzen, sind bisher gescheitert.
Die Schweizer stimmten mit der Volksinitiative vom 27. November 2005[41] mehrheitlich für ein Moratorium zur Nutzung von Gentechnik in der Landwirtschaft. Für vorerst fünf Jahre ist damit der Anbau von Pflanzen oder die Haltung von Tieren verboten, die gentechnisch verändert wurden.
In Großbritannien dürfen seit 2007 zu Forschungszwecken Embryonen mit Erbgut aus einer Kombination von menschlichen und tierischen Genen gezüchtet werden.[42]
In den USA gilt als Folge der dort angewandten Regelung der substanziellen Äquivalenz und daraus resultierenden Einstufung von GVOs als GRAS (generally recognized as save, dt: anerkanntermaßen sicher) ein Kennzeichnungsverbot, sowohl für gentechnisch veränderte als auch Gentechnik-freie Lebensmittel.[43]
Siehe auch
- Wikinews-Themenportal mit Nachrichten aus Genetik und Gentechnik
Weiterführende Literatur
Bücher
- Monika Jansohn (Hrsg.): Gentechnische Methoden – Eine Sammlung von Arbeitsanleitungen für das molekularbiologische Labor. 640 Seiten. Spektrum Akademischer Verlag 2007. 4. Aufl, ISBN 978-3-8274-1537-0
- Cornel Mülhard, Der Experimentator: Molekularbiologie/Genomics. 4. Aufl. Elsevier/Spektrum, 2003, ISBN 3-8274-1460-1
- Thilo Spahl, Thomas Deichmann: Das populäre Lexikon der Gentechnik. Eichborn, Frankfurt/Main 2001, ISBN 3-8218-1697-X
- T.A. Brown: Gentechnologie für Einsteiger. 3. Auflage. Spektrum, Heidelberg 2002, ISBN 3-8274-1302-8
- Hucho, F., Brockhoff, K., van den Daele, W., Köchy, K., Reich, J., Rheinberger, H.-J., Müller-Röber, B., Sperling, K., Wobus, A.M., Boysen, M., Kölsch, M.: Gentechnologiebericht. Analyse einer Hochtechnologie in Deutschland. München, 2005, ISBN 3-8274-1675-2
Aufsätze
- Uwe-Jürgen Ness: Gentechnische Methoden und Risiken in der Pharmakaerzeugung und -verwendung. In: Volker Haas [Hrsg.]: Gentechnik-Kritik am Scheideweg? Ist eine Teilakzeptanz der Gentechnik für Forschung, Medizin und Enzymproduktion notwendig? München 1997.
Einzelnachweise
- ↑ Brock Mikrobiologie: 11. Auflage, überarb. A. (April 2006), S. 1167, ISBN 3-8273-7187-2
- ↑ Fact Sheet: Cisgenetik und Smart Breeding
- ↑ David Quist, Ignacio Chapela: Transgenic DNA introgressed into traditional maize landraces in Oaxaca, Mexico. (Nature v.414, 541-543 29nov01)
- ↑ Andreas Lang, Heike Seitz, Frank Berhorn, Stefan Brunzel, Matthias Dolek, Sven Erlacher, Martin Felke, Patrick Leopold, Axel Schmidt, Bernhard Theißen: Standardisierte Erhebungsmethoden für Schmetterlinge (Lepidoptera) im Rahmen eines Monitorings für gentechnisch veränderte Organismen (GVO). Gefahrstoffe – Reinhaltung der Luft 66(7/8), S. 315–318 (2006), ISSN 0949-8036
- ↑ Wiebke Züghart, Frieder Graef: Monitoring der Umweltwirkungen gentechnisch veränderter Organismen. Gefahrstoffe – Reinhaltung der Luft 66(7/8), S. 319–322 (2006), ISSN 0949-8039
- ↑ BioSicherheit:Antibiotikaresistenz-Gene als Marker
- ↑ Elena R. Alvarez-Buylla, Berenice García-Ponce, Adriana Garay-Arroyo: Unique and redundant functional domains of APETALA1 and CAULIFLOWER, two recently duplicated Arabidopsis thaliana floral MADS-box genes (Journal of Experimental Botany 2006 57(12))
- ↑ Jeffrey M. Smith: Trojanische Saaten, Riemann 2004, ISBN 3-5705-0060-8. Kaptitel 4: Über das von Showa Denko auf gentechnischem Weg hergestellte L-Tryptophan, das das Eosinophilie-Myalgie-Syndrom auslöste, an dem 37 Menschen starben und über 1500 erkrankten.
- ↑ Stanley Ewen, Árpád Pusztai: Effect of diets containing genetically modified potatoes expressing Galanthus nivalis lectin on rat small intestine. The Lancet 1999; 354:1353-4
- ↑ Liste zugelassener gentechnische Arzneimittel in Deutschland beim „Verband forschender Arzneimittelhersteller“ (Stand 19. März 2008)
- ↑ Eva Fritzsche, Sabine Hancl (Hrsg.): Tierisches Insulin. trafo, Berlin 2006, ISBN 3-89626-616-0 (Patientenberichte zu Nebenwirkungen gentechnisch hergestellter Insuline)
- ↑ Krebsgesellschaft: Neues aus der Onkologie zum Thema rekombinante Interferone in der Hautkrebstherapie
- ↑ scinexx.de: EPO soll Krebstherapie unterstützen, Einsatz von Erythropoietin gegen Anämie nach einer Chemotherapie
- ↑ a b c d Gentechnologie I Skript bei biokurs.de
- ↑ Biologie-Online: Strahlengenetik
- ↑ Friedrich Leibenguth: Züchtungsgenetik S.30 und S207f, Thieme 1982, ISBN 3-1362-8601-4
- ↑ Smith HO, Wilcox KW.: A restriction enzyme from hemophilus influenzae: I. Purification and general properties., Journal of molecular biology 51 (1970) 379-91, PMID 5312500
- ↑ Wu R, Taylor E.: Nucleotide sequence analysis of DNA. II. Complete nucleotide sequence of the cohesive ends of bacteriophage lambda DNA, Journal of molecular biology 57 (1971) 491-511, PMID 4931680
- ↑ Stanley Norman Cohen, Annie Chang, Herbert W. Boyer, Robert B. Helling: Construction of Biologically Functional Bacterial Plasmids in vitro, Proceedings of the National Academy of Sciences of the United States of America 70 (1973), 3240-3244
- ↑ U. Tröhler: Asilomar-Konferenz zur Sicherheit in der Molekularbiologie von 1975 in der Schweizerischen Ärztezeitung, 28/2000
- ↑ Biolab Baden-Württemberg: Sicherheit & Recht
- ↑ a b Genentech Firmenchronologie: 1977 Genentech produced the first human protein (Somatostatin) in a microorganism (E. coli bacteria), 1982 First recombinant DNA drug marketed: human insulin
- ↑ Maxam, A. & Gilbert, W.: A new method of sequencing DNA. Proceedings of the National Academy of Sciences U.S.A., (1977) Bd. 74, S. 560-564. PMID 265521
- ↑ Sanger F, Air GM, Barrell BG, Brown NL, Coulson AR, Fiddes CA, Hutchison CA, Slocombe PM, Smith M.: Nucleotide sequence of bacteriophage phi X174 DNA. Nature, (1977) Bd. 265, S. 687-695. PMID 870828
- ↑ a b Jozef Schell, Van Montagu M., The Ti-plasmid of Agrobacterium tumefaciens, a natural vector for the introduction of nif genes in plants?. Basic Life Sci. 1977;9:159-79.
- ↑ Entscheidung des Supreme Court im Fall DIAMOND vs. CHAKRABARTY, 447 U.S. 303
- ↑ Sanger F, Coulson AR, Hong GF, Hill DF, Petersen GB: Nucleotide sequence of bacteriophage lambda DNA Journal of molecular biology 162(4) (1982) , 729-73, PMID 6221115
- ↑ Saiki RK, Gelfand DH, Stoffel S, Scharf SJ, Higuchi R, Horn GT, Mullis KB, Erlich HA: Primer-directed enzymatic amplification of DNA with a thermostable DNA polymerase, Science 239(4839) (1988), 487-91, PMID 2448875
- ↑ US Patent 4736866 - Transgenic non-human mammals (12. April 1988)
- ↑ Antje Lorch, Christoph Then: Agro-Gentechnik und die Rolle der Behörden, 2008 pdf
- ↑ BJM: Zweiter Teil GenTG
- ↑ Text der Gentechnik-Sicherheitsverordnung
- ↑ Bundesinstitut für Risikobewertung: Neuartige Lebensmittel Verordnung
- ↑ Imker hat Anspruch auf Schutz vor Pollen gentechnisch veränderten Maises
- ↑ Telepolis:Die Bienen und der Gen-Mais
- ↑ Regierung: Anbau von Genmais MON 810 stellt keine Gefahr für die Umwelt dar
- ↑ Telepolis:Der Streit um die grüne Gentechnik geht weiter
- ↑ Wortlaut des österreichischen Gentechnik-Volksbegehrens
- ↑ Parlamentarische Behandlung des Gentechnik-Volksbegehrens
- ↑ orf.at: Zehn Jahre Gentechnik-Volksbegehren: Bilanz
- ↑ admin.ch:Volksabstimmung vom 27. November 2005
- ↑ Großbritannien erlaubt Klonen von hybriden Mensch-Schwein-Embryonen heise.de vom 1. Juli 2008.
- ↑ Kommentar zur Kennzeichnungspolitik der FDA (englisch) (Dez. 2005)
Weblinks
- Telepolis Bio-Technik – tagesaktuelle Nachrichten aus der Wissenschaftsredaktion
- www.umweltinstitut.org – Gentechnik-Seiten des Umweltinstituts München
- Gen-ethisches Netzwerk e. V. – Kritischer Informationsdienst und Zeitschrift zur Gentechnologie
- Geopolitik und Gentechnik – von F. William Engdahl
- ETC Group: Biotechnology – Kritische wissenschaftliche Veröffentlichungen (engl./span.)
- Gentechnik in der EU-Politik – EU-Koordination des Deutschen Naturschutzrings
- Mailinglisten und News-Seiten zum Thema Gentechnik – Zusammenstellung von JANUN e. V. Hannover
Wikimedia Foundation.

