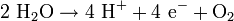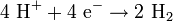- Alkalischer Elektrolyseur
-
Ein Elektrolyseur ist eine Vorrichtung, welche der Zerlegung von Wasser zu Wasserstoff und Sauerstoff dienlich ist. Den Prozess, Stoffe mithilfe des elektrischen Stroms zu zerlegen, nennt man Elektrolyse.
Der Vorgang geschieht nach folgender Reaktionsgleichung:
Der elektrische Energiebedarf zur Herstellung von 1 Nm3 Wasserstoff definiert den Wirkungsgrad einen Elektrolyseurs. In einem modernen Hochdruck-Elektrolyseur liegt dieser Energiebedarf bei etwa 4,8 kWh pro Nm3 bei einem Druck von 12 bar. Damit liegt der Wirkungsgrad bei 62,5 % (bezogen auf den unteren Heizwert von Wasserstoff).
Inhaltsverzeichnis
Man unterscheidet folgende Arten von Elektrolyseuren:
Alkalischer Elektrolyseur
Beim alkalischen Elektrolyseur wird bei einer Gleichspannung von mindestens 1,5 Volt an der Kathode Wasserstoff und an der Anode Sauerstoff gebildet. Als Elektrolyt dient Kalilauge (Kaliumhydroxid-Lösung, KOH) mit einer Konzentration von 20–40 %. Eine gasdichte Membran, das sogenannte Diaphragma, lässt zwar den Transport von OH−-Ionen zu, verhindert aber gleichzeitig die Vermischung der entstehenden Produktgase.
Als Elektroden werden sogenannte „DSA Elektroden“ (DimensionsStabile Anoden, meist Titanelektroden mit einer Rutheniumoxid-Beschichtung[1]) eingesetzt. Dies sind Streckmetalle, die mit einem Edelmetall-Katalysatoroxid - z.B. Ruthenium- oder Iridiumoxid - beschichtet werden. Es gibt aber auch Systeme mit Raney-Nickel-Katalysatoren in einer Gasdiffusionselektrode. Alkalische Elektrolyseure sind in großem Maßstab weltweit im Einsatz.
Saurer oder PEM-Elektrolyseur
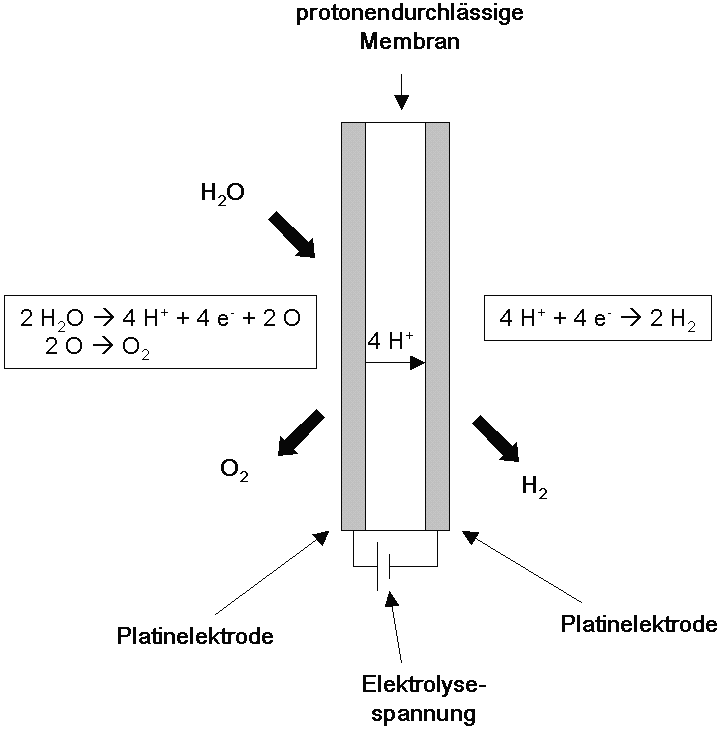
Im Protonen-Austausch-Membran-Elektrolyseur wird destilliertes Wasser durch elektrischen Strom in Wasserstoff und Sauerstoff gespalten. Er besteht aus einer protonendurchlässigen Polymermembran (en. „proton exchange membrane“ oder „polymer electrolyte membrane“, kurz „PEM“). Diese ist kathodenseitig mit einer porösen Elektrode aus auf Kohlenstoff geträgertem Platin und anodenseitig mit metallischen oder als Oxid vorliegenden Edelmetallen (meist Iridium und Ruthenium) beschichtet. An diese Elektroden wird eine äußere Spannung angelegt. Auf der Anodenseite des Elektrolyseurs wird Wasser zugeführt (Es können auch beide Halbzellen mit Wasser geflutet werden, oder auch nur die Kathodenseite, dies ist abhängig vom Verwendungszweck). Die katalytische Wirkung der Edelmetall-Elektroden führt zur Zersetzung des Wassers an der Anodenseite.
Es entstehen Sauerstoff, freie Elektronen und positiv geladene H+-Ionen. Die Wasserstoff-Ionen diffundieren durch die protonenleitende Membran auf die Kathodenseite, wo sie mit den Elektronen zu Wasserstoff kombinieren.
Reversible Brennstoffzellen auf PEM-Basis kombinieren eine Brennstoffzelle und einen Elektrolyseur und können damit als Energiespeicher (Akkumulator) dienen.[2]
Hochtemperatur-Elektrolyseur
Hochtemperaturelektrolyseure arbeiten bei Arbeitstemperaturen von etwa 900 °C. Dabei wird ein Teil der notwendigen Reaktionsenthalpie als Wärme eingekoppelt. Dies führt dazu, dass der Strombedarf sinkt und damit der primärenergetische Wirkungsgrad gegenüber der wässrigen, alkalischen Elektrolyse steigt.
Beispiele für Elektrolyseure
Einzelnachweise
- ↑ R. Holze: Leitfaden der Elektrochemie. S. 206, Vieweg+Teubner Verlag, 1998, ISBN 9783519035473
- ↑ Fraunhofer ISE: Reversible Brennstoffzellen - Langzeitspeicher für elektrische Energie.
Wikimedia Foundation.