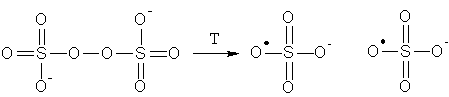- Ammoniumpersulfat
-
Strukturformel 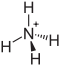

Allgemeines Name Ammoniumperoxodisulfat Andere Namen Ammoniumpersulfat
Summenformel H8N2O8S2 CAS-Nummer 7727-54-0 Kurzbeschreibung Farblose Kristalle Eigenschaften Molare Masse 228,20 g/mol Aggregatzustand fest
Dichte 1,98 g/cm3[1]
Schmelzpunkt Löslichkeit löslich in Wasser (620 g/l, 20 °C)[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 

Brand-
förderndGesundheits-
schädlich(O) (Xn) R- und S-Sätze R: 8-22-36/37/38-42/43 S: (2)-22-24-26-37 MAK keine Einstufung[1]
WGK 1[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Ammoniumperoxodisulfat ist eine salzartige Verbindung aus zwei Ammoniumionen und einem Peroxodisulfation.
Es besitzt die Formel (NH4)2S2O8Inhaltsverzeichnis
Darstellung
Ammoniumperoxodisulfat wird durch anodische Oxidation von Ammoniumsulfat hergestellt.[2]
Eigenschaften
Ammoniumperoxodisulfat ist das Salz der Peroxodischwefelsäure. Es bildet weiße Kristalle mit leichter grüner Fluoreszenz. Ammoniumperoxodisulfat ist wegen seines hohen Sauerstoffgehaltes ein starkes Bleich- und Oxidationsmittel sowie ein starker Radikalbildner. Es ist trocken zu lagern, da es sich in Gegenwart von Feuchtigkeit oder in warmen, wässrigen Lösungen unter Abgabe von Ozon zersetzt. Ammoniumperoxodisulfat zersetzt sich beim Erwärmen in je zwei Ammoniumionen und Sulfatradikale. Untenstehend die Zersetzung des Persulfations in zwei Sulfat-Radikale.
Anwendung
Ammoniumperoxodisulfat ist ein Polymerisationsinitiator beim Herstellen von Polyacrylamidgelen und wird auch bei der Herstellung von Superabsorbern als thermischer Radikalinitiator verwendet. Die bei der Zersetzung gebildeten Sulfatradikale können durch einen nucleophilen Angriff auf Kohlenstoffatome mit Doppelbindung dieselbe auflösen und so eine Kettenreaktion starten. Zudem kann es als Oxidationsmittel und zum Ätzen von gedruckten Schaltungen verwendet werden. In der chemischen Analyse wird es zur Trennung von Mangan und Chrom genutzt. In der Fotoentwicklung ist es ein Abschwächer.
Quellen
Wikimedia Foundation.