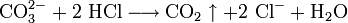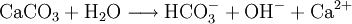- Karbonat
-
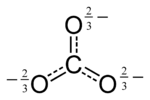
Als Carbonate werden die Salze der vollständig dissoziierten Kohlensäure bezeichnet. Das zugehörige zweifach negativ geladene Anion („Säurerest“) ist das Carbonat-Ion CO32−.
Das Carbonat-Anion ist vollkommen planar gebaut, mit 120°-Bindungswinkeln zwischen den einzelnen Sauerstoffatomen. Die Abstände aller drei O-Atome zum zentralen Kohlenstoffatom sind gleich und liegen mit etwa 130 pm zwischen der Länge von C-O-Einfachbindungen (143 pm) und C=O-Doppelbindungen (123 pm).[1]
Auch die Ester der Kohlensäure mit der allgemeinen Strukturformel R1-O-C(=O)-O-R2, wobei R1 und R2 kohlenstoffhaltige Alkyl- oder Aryl-Reste sind, werden Carbonate genannt. Gehören R1 und R2 zu demselben Molekül, so bildet sich eine ringförmige Verbindung wie beispielsweise Propylencarbonat.
Inhaltsverzeichnis
Vorkommen
 Der Edelstein Malachit im Planschliff, chemisch gesehen: basisches Kupfer(II)-carbonat
Der Edelstein Malachit im Planschliff, chemisch gesehen: basisches Kupfer(II)-carbonatCarbonat-Salze kommen ubiquitär in der Natur vor, vorwiegend als Minerale wie Calciumcarbonat (Kalk, Calcit, Kalkspat, Aragonit oder Marmor), Calciummagnesiumcarbonat (Dolomit), Magnesiumcarbonat (Magnesit), Eisencarbonat (Siderit oder Eisenspat), Mangancarbonat (Rhodochrosit oder Manganspat) und Zinkcarbonat (Smithsonit oder Zinkspat).[2] Die Gesamtmenge der in der Lithosphäre enthaltenen Carbonate beträgt etwa 2,9·1016 t.[1] Weiterhin enthält auch die Hydrosphäre der Meere, Seen und Flüsse große Mengen gelöster Carbonate und nahezu alle Lebewesen tragen sowohl gelöste Carbonate in sich oder benutzen unlösliche Carbonate als Gerüstsubstanz.
Eigenschaften von (anorganischen) Carbonaten
Carbonate sind ionische Salze und deshalb bei Raumtemperatur in der Regel kristalline Feststoffe. Das Carbonat-Anion bringt keine Eigenfarbe in die Verbindungen ein, so dass deren Farbe ggf. durch das betreffende Kation bestimmt wird. Carbonate sind geruchlos. Mit Ausnahme der Alkali-Carbonate sind sie nur wenig wasserlöslich, so dass die meisten Metalle bei Reaktion mit Alkalicarbonaten ausgefällt werden.
Reaktionen von Carbonaten
- Reaktion zwischen Kohlensäure und Carbonat:
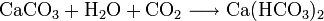
- Calciumcarbonat reagiert mit Wasser und Kohlenstoffdioxid zu Calciumhydrogencarbonat.
Diese Reaktion spielt sich bei der Lösung von Kalkstein in kohlensäurehaltigem Grundwasser ab. Sie ist der Ursprung der Wasserhärte.
- Dissoziation in Wasser:
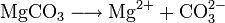
- Magnesiumcarbonat dissoziiert zu einem Magnesiumion und einem Carbonation.
- Zerfall beim Erhitzen:
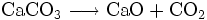
- Calciumcarbonat zerfällt zu Calciumoxid und Kohlenstoffdioxid.
Dies ist die Reaktion bei der Herstellung von Branntkalk.
Siehe auch: Carbonat-Silicat-Zyklus
Nachweis von Carbonaten
Carbonat-Ionen (CO32−) lassen sich durch Zugabe von Salzsäure nachweisen, bei der Kohlenstoffdioxid entsteht:
Kohlenstoffdioxidgas wird in die Nachweisreagenz Kalk- oder Barytwasser geleitet. Dort erzeugt es eine weiße Trübung von Calcium-- bzw. Bariumcarbonat:
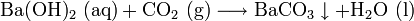
- Bariumhydroxid und Kohlenstoffdioxid reagieren zu Bariumcarbonat und Wasser
Der quantitative Nachweis geringer Carbonatkonzentrationen in Wässern erfolgt zusammen mit der Bestimmung von Hydrogencarbonaten oft durch eine Titration mit Salzsäure ("SBV"): weist das Messgut zu Beginn einen pH-Wert über 8,3 auf, so ist der Salzsäureverbrauch bis zum Erreichen von pH 8,3 äquivalent der Carbonatkonzentration. Der weitere Säureverbrauch bis zum Erreichen von pH 4,3 entspricht der Summe von Carbonat und Hydrogencarbonat. Bei Wässern mit pH-Werten unter 8,3 titriert man gleich nur bis 4,3 (nur noch Hydrogencarbonat) und errechnet den ursprünglichen, dann sehr geringen Anteil an Carbonat-Ionen aus dem Dissoziationsgleichgewicht der Kohlensäure.
Carbonate und Hydrogencarbonate können auch durch Ionen-HPLC oder durch Kapillarelektrophorese bestimmt werden. In beiden Fällen wird ein "Gesamtcarbonat" ermittelt und die Komponenten Carbonat, Hydrogencarbonat und "Freie Kohlensäure" unter Berücksichtigung von pH-Wert, Ionenstärke und Temperatur wiederum aus dem Dissoziationsgleichgewicht der Kohlensäure errechnet.
Basische Reaktion
Die Carbonationen reagieren mit Wasser zu Hydrogencarbonat- und Hydroxidionen. Es handelt sich dabei um eine basische Reaktion.
Wichtige Carbonate
 Strontianit aus dem Münsterland, chemisch gesehen: Strontiumcarbonat
Strontianit aus dem Münsterland, chemisch gesehen: Strontiumcarbonat- Bariumcarbonat (Witherit)
- Kaliumcarbonat (Pottasche)
- Natriumcarbonat (Soda)
- Magnesiumcarbonat (Magnesit)
- Calciumcarbonat (Kalkstein, Kreide, Kesselstein, Marmor)
- Calcium-Magnesium-Carbonat (Dolomit)
- Weitere Beispiele siehe unter: Kategorie:Carbonat
Organische Carbonate
Die kovalenten Carbonate, die sich formal von Alkoholen und Kohlensäure ableiten, kommen natürlich nicht vor. Der einfachste synthetisch hergestellte Kohlensäureester ist Dimethylcarbonat.
In den letzten Jahren haben organische Carbonate in polymerer Form als Polycarbonate besonders bei der Produktion von CDs und DVDs größere wirtschaftliche Bedeutung erlangt.
Einzelnachweise
- ↑ a b A.F. Holleman, E. Wiberg, N. Wiberg : Lehrbuch der anorganischen Chemie, 1995, Walter de Gruyter, ISBN 3-11-012641-9
- ↑ Wissenschaft-Online-Lexika: Eintrag zu Carbonate im Lexikon der Geographie
Weblinks
Wikimedia Foundation.