- Knoevenagel-Kondensation
-
Die Knoevenagel-Reaktion oder Knoevenagel-Kondensation ist eine wichtige Reaktion in der organischen Chemie. Es ist ein Spezialfall der Aldolreaktion, bei der Ketone oder Aldehyde mit besonders CH-aciden Verbindungen, z. B. Malonsäureester, Acetessigester oder Nitromethan, umgesetzt werden. Dabei entstehen ungesättigte Kondensationsprodukte.
Eine spezielle Reaktionsführung der Knoevenagel-Reaktion ist deren Doebner-Variante. Bei ihr wird der Aldehyd/das Keton mit freier Malonsäure in Pyridin und in Gegenwart eines Amins als Katalysator (häufig Pyrrolidin oder Piperidin) zur Reaktion gebracht. Die entstehende ungesättigte Dicarbonsäure decarboxyliert dabei. Auf diesem Wege sind z. B. Zimtsäuren sehr einfach zugänglich.
Benannt wurde die Reaktion nach ihrem Entdecker Emil Knoevenagel.
Reaktionsmechanismus
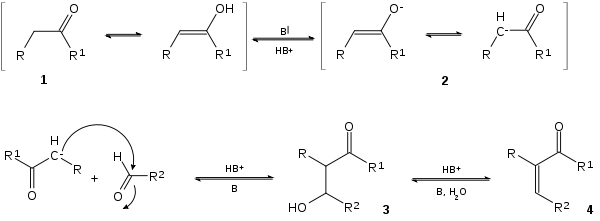
Nebenstehendes Reaktionsschema gibt einen allgemeinen Mechanismus der Knoevenagel-Kondensation an: Die CH-acide Verbindung 1 wird durch die als Katalysator zugegebene Base (meist ein Amin) deprotoniert. Das dadurch entstehende Anion 2 greift als Carbanion nukleophil den Carbonyl-Kohlenstoff der Carbonylverbindung an, während der Sauerstoff der Carbonylgruppe protoniert wird. Es entsteht der Alkohol 3, der als Intermediat auch isolierbar ist. Im darauf folgenden Eliminierungsschritt wird nach Protonierung der Hydroxy-Gruppe und deren Abgang als Wasser das ungesättigte Endprodukt 4 frei. Der Rest R der CH-acide Verbindung ist dabei vorzugsweise eine elektronenziehende Gruppe (z.B. -CN beim Cyanessigester oder -COCH3 bei Acetessigester). R'/R" sind zumeist Alkyl oder Arylreste.
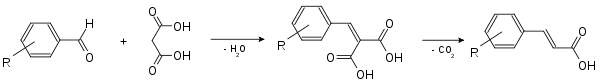
Die Doebner-Variante bietet einen einfachen Zugang zu α,β-ungesättigten Carbonsäuren, z. B. Zimtsäuren (R: div. Substituenten in verschiedenen Positionen, z. B. -OCH3):
Bekannte Produkte
Wikimedia Foundation.