- Anhydritspat
-
Anhydrit (Anhydritspat) Anhydrit aus Chihuahua, Mexiko Chemische Formel CaSO4 Mineralklasse Wasserfreie Sulfate
7.AD.30 (8. Auflage: VI/A.08-50) (nach Strunz)
28.3.2.1 (nach Dana)Kristallsystem orthorhombisch Kristallklasse dipyramidal 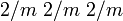
Farbe farblos, weiß, seltener rötlich, violett, bläulich, braun Strichfarbe weiß Mohshärte 3 bis 3,5 Dichte (g/cm³) 2,8 bis 3,0 Glanz Glasglanz, Perlmuttglanz Transparenz durchsichtig bis durchscheinend Bruch splitterig bis uneben Spaltbarkeit gut Habitus körnige, massige Aggregate; seltener prismatische Kristalle Häufige Kristallflächen Zwillingsbildung Kristalloptik Brechzahl α=1,569–1,573 β=1,574–1,579 γ=1,609–1,618 Doppelbrechung
(optische Orientierung)Δ=0,040-0,045 ; zweiachsig positiv Weitere Eigenschaften Schmelzpunkt 1450 °C Chemisches Verhalten schwer wasserlöslich (2 g/l bei 25 °C) Radioaktivität nicht radioaktiv Magnetismus nicht magnetisch Anhydrit (vom Griechischen anhydros: „wasserlos“; auch Anhydritspat oder Calciumsulfat, Gekrösstein oder Karstenit) ist ein häufig vorkommendes Mineral aus der Mineralklasse der wasserfreien Sulfate ohne fremde Anionen. Es kristallisiert im orthorhombischen Kristallsystem mit der chemischen Formel CaSO4 und entwickelt meist grobkörnige, massige Aggregate, manchmal aber auch prismatische Kristalle in den Farben weiß, violett, braun, rötlich oder bläulich. Es hat eine Mohssche Härte von 3 bis 3,5 und eine Dichte von 2,8 bis 3 g/cm3.
Die Anhydrit-Kristalle lassen sich an drei im rechten Winkel zueinander stehenden Flächen gut spalten und lassen sich dadurch von dem ansonsten äußerlich sehr ähnlichen Gips unterscheiden, in den das Anhydrit durch Wassereinlagerung übergeht.
Inhaltsverzeichnis
Modifikationen und Varietäten
- Angelit – Handelsbezeichnung für einen durchscheinenden, grau-blau-violetten Anhydrit-Kristall
- Vulpinit – körniges Aggregat
Bildung und Fundorte
Anhydrit ist ein Sediment-Mineral und bildet sich oft als Verdunstungsprodukt von Meerwasser, wobei die Temperatur über 35 °C betragen muss. Bei niedrigeren Temperaturen bildet sich Gips. Es kann sich, weil es schwer wasserlöslich ist, direkt aus überhitztem Meerwasser ablagern oder aber zusammen mit Gips und Halit bei Verdampfung desselbigen entstehen. Begleitminerale sind Gips(spat) und/oder Calcit.
Anhydrit nimmt bei kurzfristiger Feuchtigkeitseinwirkung kein Wasser auf. Steht er aber unter permanenter Feuchtigkeitseinwirkung, so verwandelt er sich langsam zu Gips. Dabei kommt es zu einer Volumenszunahme, die mitunter sprengend wirken kann. So können im Bergbau Anhyditschichten durch Grubenwasser "anwachsen", die Stollen verengen (Zwergenlöcher, Quellungshöhlen) oder Hebungen verursachen. Das ist beispielsweise auch im Straßen- und Tunnelbau zu beachten.
Wichtige Fundorte sind unter anderem Ellrich, Niedersachswerfen, Staßfurt und Wathlingen in Deutschland, Sardinien in Italien, Touissit in Marokko, Naica/Chihuahua in Mexiko, Tsumeb in Namibia, Wienern am Grundlsee (Steirisches Salzkammergut) in Österreich, Wieliczka in Polen, Simplon und das Gotthardmassiv in der Schweiz, Mežica in Slowenien sowie Idaho und Pennsylvania in den USA.
Anhydrit kann aber auch durch Brennen von Gips entstehen. Bei Temperaturen um 100 °C verbleibt im Gipsstein etwas Kristallwasser es entsteht Halbhydrat, bei höheren Temperaturen wird das gesamte Kristallwasser entzogen und es entsteht Anhydrit.
Verwendung
Anhydrit wird in Pulverform zu Klebstoff für Fliesen verarbeitet, allerdings muss ein "Anreger", meist Kaliumsulfat (K2SO4), oder auch Kalk (CaO), beigesetzt werden. Der Anreger, dessen Anteil 3-15% beträgt, beschleunigt die Wassereinlagerung, wodurch sich Anhydrit zu Gips umwandelt. Die Umwandlung von Anhydrit zu Gips erfolgt aber nur zu etwa 65%, wobei der Gips für die schnelle Trocknung sorgt und das Anhydrit als Gerüst für die hohe Festigkeit. Derartige Anhydritbinder sind lufthärtende, nicht hydraulische Bindemittel aus natürlichem oder synthetischem Anhydrit. Sie sind in ihren physikalischen und chemischen Eigenschaften mit Gips vergleichbar. Calciumsulfatbinder wird zum Beispiel im Wohnungsbau zur Herstellung von Calciumsulfatestrich oder Calciumsulfat-Fliessestrich verwendet.
Pulverisiertes Anhydrit ist Bestandteil von Zement und wird auch bei der Produktion von Schwefelsäure und Porenbeton eingesetzt.
Die Varietät Angelit wird darüber hinaus als Schmuckstein verwendet.
Sprengwirkung
Steht Anhydrit unter permanenter Feuchtigkeitseinwirkung, so nimmt er Wasser auf, wodurch sein Volumen um 50% zumimmt. Anhydrit verwandelt sich zu Gips, quillt dabei auf und kann sprengende Kräfte entwickeln. Dieser Prozess wird Salzsprengung genannt.
Im Bergbau können aufquellende Anhydritschichten die Stollen verengen und die anliegenden Gesteinsschichten sprengen. Im Extremfall kann dies auch zur Hebung des Bodens führen.
Anhydrit in Reinform ist daher als Baustoff ungeeignet.
Siehe auch
Literatur
- Petr Korbel, Milan Novák: Mineralien Enzyklopädie. Nebel Verlag GmbH, Eggolsheim 2002, ISBN 3-89555-076-0
Weblinks
- Mineralienatlas:Anhydrit (Wiki)
- Mineralien-Lexikon - Anhydrit
- Webmineral - Anhydrite (engl.)
- MinDat - Anhydrite (engl.)
- Verfahren zur Hydratisierung von Anhydrit
Wikimedia Foundation.

