- Lykopin
-
Strukturformel 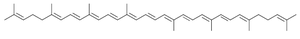
Allgemeines Name Lycopin Andere Namen - ψ,ψ-Carotin
- C.I. 75125
- C.I. Natural yellow 27
- E 160d
Summenformel C40H56 CAS-Nummer 502-65-8 Kurzbeschreibung dunkelrote Nadeln Eigenschaften Molare Masse 536,85 g/mol Aggregatzustand fest
Schmelzpunkt Löslichkeit In Wasser unlöslich, in Ethanol schwerlöslich und in pflanzlichen Ölen mäßig löslich.
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Lycopin (Lycopen) gehört zur Klasse der Carotinoide und wird in hohen Konzentrationen in Tomaten (von deren wissenschaftlichem Namen Solanum lycopersicum auch die Bezeichnung des Stoffes herrührt) und Hagebutten gefunden. Der Stoff besitzt aufgrund seiner Polyen-Struktur eine rote Farbe, welche auch den Tomaten ihre charakteristische Färbung verleiht. Es ist als Lebensmittelfarbstoff E 160d in der EU zugelassen. Lycopin zählt zu den Antioxidantien und gilt als Radikalfänger, d.h., es kann bestimmte reaktionsfreudige Moleküle im menschlichen Körper unschädlich machen.
Inhaltsverzeichnis
Vorkommen und Gewinnung
Reife Tomaten haben einen Lycopinanteil von ca. 3,9–5,6 mg pro 100 g Frucht. Auch Wassermelonen können etwa diese Konzentration an Lycopin (bis zu 1000 ppm der Trockenmasse) enthalten. Wesentlich mehr Lycopin enthalten Dosentomaten mit ca. 10 mg pro 100 Gramm. Dosentomaten werden meist erst in reifem Zustand geerntet und weisen deshalb mehr Lycopin auf. Konzentriertes Tomatenmark enthält sehr hohe Lycopinkonzentrationen (ca. 62 mg Lycopin pro 100 Gramm).
Die Verfügbarkeit von Lycopin ist bei verarbeiteten und erhitzten Produkten (z. B. Tomatensaft) höher als bei rohen, da beim Erhitzen die pflanzlichen Zellstrukturen aufgebrochen werden und das Lycopin herausgelöst wird. Eine deutliche Resorptionssteigerung wird durch die Kombination mit Fett erreicht.
Großtechnisch wird Lycopin mit organischen Lösungsmitteln (Hexan, Dichlormethan, Methanol) aus Tomatenkonzentraten extrahiert.
Verwendung
Lycopin wird als rote Lebensmittelfarbe als Carotinoid deklariert (siehe auch Carotine (E 160a–160f)) und zur Koloration von Lebensmitteln verwendet. Es wird vor allem zur Färbung von herzhaften Produkten, Suppen und Soßen, wo der Beigeschmack nach Tomate nicht stört, eingesetzt.
Biologische Wirkung
Carotinoide, insbesondere das Lycopin, zählen zu den wirksamsten natürlich vorkommenden Quenchern für Singulettsauerstoff 1O2. Dieser wird zum Beispiel durch photochemische Reaktionen bei der Lichtabsorption gebildet und ist hochreaktiv. Er kann verschiedene Aminosäuren in Proteinen, Nukleinsäuren sowie ungesättigte Fettsäuren oxidieren. Bei der Quenchingreaktion gehen die Carotinoide in einen angeregten Triplettzustand über ( 1O2 + 1Car → 3O2 + 3Car ). Anschließend erreichen die Carotinoide durch Abgabe von Wärme wieder ihren Grundzustand (3Car → 1Car + Wärme). Die Carotinoidmoleküle werden also bei dieser Reaktion nicht chemisch umgewandelt und stehen somit für weitere Quenchingprozesse zur Verfügung. Die Quenchingrate von Lycopin ist besonders hoch (ca. doppelt so groß wie bei β-Carotin und 100-mal so groß wie bei α-Tocopherol). Diese im Labor gefundene antioxidative Wirkung bedeutet jedoch nicht automatisch eine gesundheitsfördernde Wirkung des Lycopin.
Es gab Hinweise, dass der Konsum von Lycopin zu einem reduzierten Risiko führt, an Herz-Kreislauf-Erkrankung, Krebs (vor allem Prostatakrebs[2]), Diabetes mellitus, Osteoporose und Unfruchtbarkeit zu leiden.[3] Eine neuere, große Studie mit ca. 28.000 Probanden lässt jedoch vermuten, dass kein Zusammenhang zwischen Lycopin und Krebsrisiko besteht. Vielmehr zeigte sich, dass das verwandte Antioxidant β-Carotin das Risiko für Prostatakrebs erhöht.[4] Eine schützende Wirkung bei Belastungs-Asthma konnte nicht gezeigt werden.[5]
Im Menschen wird Lycopin mithilfe der β-Carotin-Dioxygenase 2 (BCDO2) abgebaut.[6] Die Abbauprodukte sind Pseudojonon, Geranial und 2-Methyl-2-hepten-6-on.[7]
Einzelnachweise
- ↑ a b Sicherheitsdatenblatt (Carl Roth)
- ↑ Giovannuci, E. et al. (2002): A Prospective Study of Tomato Products, Lycopene and Prostate Cancer Risk. In: J. Natl. Cancer. Inst. Bd. 94, S. 391-398. PMID 11880478
- ↑ Bowen P, Chen L, Stacewicz-Sapuntzakis M, Duncan C, Sharifi R, Ghosh L, Kim HS, Christov-Tzelkov K, van Breemen R: Tomato sauce supplementation and prostate cancer: lycopene accumulation and modulation of biomarkers of carcinogenesis. In: Experimental Biology and Medicine. 227, Nr. 10, 2002, S. 886–893. PMID 12424330
- ↑ American Association for Cancer Research. „No Magic Tomato? Study Breaks Link between Lycopene and Prostate Cancer Prevention “, Science Daily, May 17, 2007.
- ↑ B Falk et. al. Annals of Allergy, Asthma, & Immunology. 2005;94(4):480-5
- ↑ Kiefer et al.: Identification and characterization of a mammalian enzyme catalyzing the asymmetric oxidative cleavage of provitamin A. J. Biol. Chem. 276/-/2001: 14110-14116. PMID 11278918
- ↑ John Shi und Jerry W. King: Functional Food Ingredients and Nutraceuticals: Processing Technologies. CRC Press, 2006. ISBN 0849324416 S. 360
Wikimedia Foundation.

