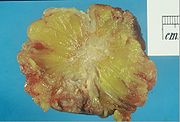
- Mammacarcinom
-
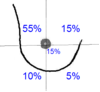
Klassifikation nach ICD-10 C50 Mammakarzinom C50.0 Brustwarze und Warzenhof C50.1 Zentraler Drüsenkörper der Brustdrüse C50.2 Oberer innerer Quadrant der Brustdrüse C50.3 Unterer innerer Quadrant der Brustdrüse C50.4 Oberer äußerer Quadrant der Brustdrüse C50.5 Unterer äußerer Quadrant der Brustdrüse C50.6 Recessus axillaris der Brustdrüse C50.8 Brustdrüse, mehrere Teilbereiche überlappend C50.9 Brustdrüse, nicht näher bezeichnet ICD-10 online (WHO-Version 2006)  Rosa Schleife – Symbol der Solidarität mit von Brustkrebs betroffenen Frauen
Rosa Schleife – Symbol der Solidarität mit von Brustkrebs betroffenen FrauenBrustkrebs (medizinisch Mammakarzinom) ist der häufigste bösartige Tumor der Brustdrüse des Menschen. Er kommt hauptsächlich bei Frauen vor; nur etwa jede hundertste dieser Krebserkrankungen tritt bei Männern auf.[1]. In den westlichen Staaten ist Brustkrebs die häufigste Krebsart bei Frauen. Am Brustkrebs sterben mehr Frauen, als an irgendeiner anderen Krebserkrankung. Die meisten Erkrankungen treten sporadisch (zufällig) auf, es gibt aber sowohl erbliche als auch erworbene Risikofaktoren. Neben der Heilung sind der Erhalt der betreffenden Brust und vor allem der Lebensqualität erklärtes Ziel der medizinischen Behandlung. Die Therapie besteht in der Regel in einer an das Erkrankungsstadium angepassten Kombination aus Operation sowie Zytostatika-, Hormon- und Strahlentherapie. Neue Ansätze werden außerdem durch monoklonale Antikörper ermöglicht. Das medizinische Vorgehen basiert in hohem Maß auf Erfahrungen aus Studien und ist in weltweit akzeptierten Leitlinien standardisiert. Zahlreiche nationale und internationale Programme zur Früherkennung und zur strukturierten Behandlung sollen die Mortalität (Sterblichkeit) künftig senken.
Inhaltsverzeichnis
Epidemiologie
In Deutschland ist das Mammakarzinom mit einem Anteil von 28 % aller Krebsneuerkrankungen die häufigste Krebserkrankung bei Frauen. Jede achte bis zehnte Frau erkrankt im Laufe ihres Lebens an Brustkrebs. Dies sind in Deutschland etwa 57.000 Neuerkrankungen pro Jahr oder 130 Fälle pro 100.000 Einwohner und Jahr. Bei internationalen Vergleichen muss die unterschiedliche Altersverteilung der nationalen Bevölkerungen berücksichtigt werden. Die nach dem sogenannten Europastandard (ESR) altersstandardisierte Inzidenz (Neuerkrankungsrate) liegt in Deutschland bei 102/100.000, nach dem Weltstandard (WSR) bei 80/100.000. Die brustkrebsbedingte Sterberate (Mortalität) beträgt 42/100.000 Frauen beziehungsweise altersstandardisiert 27,6/100.000 nach dem ESR und 22/100.000 nach dem WSR. Die Wahrscheinlichkeit, dass eine Erkrankung tödlich ausgeht (Letalität), liegt über alle Stadien gemittelt bei ca. 30 %[2]. Seit 1970 haben sich die Erkrankungszahlen verdoppelt, während die Mortalität eher rückläufig ist [3].
In der westlichen Welt ist Brustkrebs die häufigste Todesursache bei Frauen zwischen dem 30. und 60. Lebensjahr. Weltweit gibt es nach Schätzungen der WHO (2003) zirka 1.050.000 neue Erkrankungsfälle pro Jahr, davon 580.000 in den Industriestaaten. Vergleichsweise seltener ist die Erkrankung in Afrika und Asien. Weltweit starben 1998 ca. 412.000 Frauen an Brustkrebs, das sind 1,6 % aller gestorbenen Frauen. [4]. Brustkrebs ist weltweit der häufigste Krebs und die häufigste Todesursache bei Frauen. Während jedoch in den reichen Ländern die Sterberate sinkt, ist sie in den ärmeren Ländern hoch. Dies hängt zum einen mit der immer höheren Lebenserwartung zusammen, zum anderen mit den schlechteren diagnostischen und therapeutischen Möglichkeiten in den ärmeren Ländern. WHO-Angaben zufolge starben 2007 etwa 72 Prozent aller an Krebs erkrankten Menschen in Ländern mit mittlerem und niedrigem Einkommen.[5]
Männer erkranken selten an Brustkrebs. Nach Schätzungen sind es in Deutschland etwa 400 Männer im Jahr. Das Verhältnis von Erkrankungen bei Männern zu Frauen liegt bei 1:100 [6]. Im Schnitt erkranken sie 10 Jahre später als Frauen. Die Mortalität bei Männern liegt bei rund 200 Todesfällen pro Jahr.
Anzahl der am Mammakarzinom verstorbenen Frauen
nach Altersgruppen
[7]Alter 2003 2004 2005 2006 0–30 1) 16 2) 20 16 13 30–40 348 318 294 294 40–50 1.271 1.296 1.283 1.176 50–60 2.493 2.404 2.419 2.489 60–70 4.158 4.441 4.252 4.035 70–80 4.140 4.354 4.273 4.283 >80 4.747 4.759 4.918 4.996 gesamt 17.173 17.592 17.455 17.286 1) ein Mädchen 5–10 Jahre
2) ein Mädchen 10–15 JahreAnteil der Todesursache „Mammakarzinom“
in Prozent nach Altersgruppen
(nur Frauen)[7]Alter 2003 2004 2005 2006 0-30 0,4 0,5 0,5 0,4 30-40 10 11 10 11 40-50 13 14 14 13 50-60 14 14 13 14 60-70 9 10 10 10 70-80 4 5 4 5 80 > 2 2 2 2 Ursachen und Risikofaktoren
Genetische Risikofaktoren
Etwa 5 % der Brustkrebserkrankungen sind erblich bedingt.[8] Nur bei einer kleinen Gruppe von Frauen (etwa 1 pro 500) findet man definierte, krankheitsverursachende Mutationen. Wesentlich häufiger sind genetische Veränderungen, die die Suszeptibilität (Empfänglichkeit) für Brustkrebs auf äußere Faktoren erhöhen.
Die höchste Wahrscheinlichkeit, an der erblichen Form des Brustkrebs zu erkranken, besteht bei Frauen mit Mutation in den Breast-Cancer-Genen BRCA1 und BRCA2. Es kommt bereits bei einer Mutation in einem Allel dieser Gene zur Erkrankung (man spricht von sogenannten Proto-Onkogenen mit autosomal-dominantem Erbgang). Die Wahrscheinlichkeit, im Laufe des Lebens an Brustkrebs zu erkranken, wird für Trägerinnen des BRCA1 mit 65 %, für Trägerinnen des BRCA2 mit 45 % angegeben.[9]
Mutationen im p53-Gen, einem der Tumorsuppressorgene, werden autosomal rezessiv vererbt (Li-Fraumeni-Syndrom). Weitere Genveränderungen, die das Risiko erhöhen, betreffen Mutationen von PTEN (Cowden-Syndrom), STK11 (Peutz-Jeghers-Syndrom) und CDH1 (E-Cadherin); deren Häufigkeit und Risikoerhöhung für die Brustkrebserkrankung ist jedoch nicht genau bekannt. Mäßig erhöht ist die Wahrscheinlichkeit bei Bestehen der seltenen genetischen Veränderungen mit mittlerer Penetranz, diese betreffen unter anderem die folgenden Gene: ATM (Ataxia teleangiectatica), CHK2 (checkpoint kinase 2) und BRIP1.[10] Insgesamt lassen sich nicht mehr als 5 % der Brustkrebserkrankungen auf diese Genveränderungen mit hohem oder mittlerem Risiko zurückführen.[11]
Die wesentlich häufigeren Allelveränderungen mit geringer Penetranz erhöhen das Brustkrebsrisiko höchstens auf das 1,25-fache bei heterozygoten Veränderungen und auf das 1,65-fache bei homozygoten Veränderungen. Dazu gehören insbesondere Veränderungen von FGFR2 (fibroblast growth factor receptor 2) und auf dem Chromosom 2q. Es wird geschätzt, dass solche Mutationen mit geringer Penetranz bei 58 % der Brustkrebserkrankungen eine Rolle spielen.[12]
Die Wahrscheinlichkeit, selbst zu erkranken, steigt statistisch nachweisbar ab zwei an Brustkrebs Erkrankten in der direkten Verwandtschaft an [13]. Familien, in denen mehrere Personen an Brust- oder Eierstockkrebs erkrankt sind, wird eine tumorgenetische Beratung in einem Beratungszentrum, beispielsweise aus dem Verbundprojekt familiärer Brustkrebs der Deutschen Krebshilfe empfohlen.[14]
Bei Frauen mit einer entsprechenden Prädisposition (hohe Wahrscheinlichkeit des Krankheitsauftretens) kann auf Wunsch eine beidseitige prophylaktische Mastektomie (Brustamputation) und / oder eine Eierstockentfernung vorgenommen werden: Einen gewissen Schutz vor einer Brustkrebserkrankung scheint die weitgehende Unterbindung der Östrogenproduktion durch die Entfernung beider Eierstöcke zu bieten. Verschiedene Autoren berichten von einer Verringerung des Erkrankungsrisikos von 50 bis 70 %, wenn in der Familie bereits Brustkrebs auftrat.[15]
Hormonelle Faktoren
Weibliche Körperzellen, auch Tumorzellen, tragen Rezeptoren für die Sexualhormone Estrogene und Gestagene. Viele Mammakarzinome werden in ihrem Wachstum durch diese Hormone beeinflusst. Östrogen- und progesteronhaltige Medikamente gegen Wechseljahresbeschwerden (Hormonersatztherapie) erhöhen das Erkrankungsrisiko um bis zu 45 % [16]. Auch Frauen mit früher Menarche (erstes Auftreten der Regelblutung in der Pubertät) und später Menopause (Ende der Menstruation, „Wechseljahre“) tragen ein etwas höheres Erkrankungsrisiko. Frauen, die früh Kinder bekommen und lange stillen, haben dagegen ein niedrigeres Risiko [17].
Ob die Antibabypille das Risiko erhöht, ist substanz- und dosisabhängig und daher nicht vollständig geklärt. Die Nurses' Health Study und weitere Studien haben eine Erhöhung des Risikos auf das 1,2- bis 1,4-fache nach einer Einnahme der „Pille“ über mehr als fünf Jahre gezeigt.
Schwangerschaftsabbrüche erhöhen das Brustkrebsrisiko einer Metaanalyse aus dem Jahr 2004 zufolge nicht [18]. Auch in anderen Studien mit hohen Fallzahlen konnte man einen solchen Zusammenhang nicht nachweisen [19] [20] [21].
Phytoöstrogene sind Pflanzeninhaltsstoffe mit schwach östrogenartiger Wirkung. Ob Diäten, die reich an solchen Stoffen sind (etwa auf Sojabasis), das Erkrankungsrisiko erhöhen oder im Gegenteil durch Interaktion mit der körpereigenen Hormonproduktion senken, ist noch nicht bekannt, da die Ergebnisse der wissenschaftlichen Untersuchungen widersprüchlich sind [22] [23].
Weitere Faktoren
Die Exposition mit ionisierender Strahlung in jungen Jahren erhöht das spätere Brustkrebsrisiko [24]. Mammographie-Untersuchungen bei Frauen über 40 Jahren führen zu keiner bedeutsamen Risikosteigerung mehr [25].
Auch die Lebensweise beeinflusst das Risiko. So erkranken deutlich übergewichtige Frauen 2,5 mal so häufig, wie Normalgewichtige [26]. Starkes und langdauerndes Zigarettenrauchen erhöht die Erkrankungswahrscheinlichkeit um 30 % [27]. Auch Frauen, die täglich mindestens 20 g Alkohol trinken, tragen ein um 30 % erhöhtes Risiko, an einem Mammakarzinom zu erkranken, möglicherweise wegen des höheren Sexualhormonspiegels [26]. Ein weiterer Risikofaktor könnte Sonnen- bzw. Vitamin-D-Mangel sein. Dieser Zusammenhang wird auch für Prostatakrebs, Dickdarmkrebs, Ovarialkrebs, Melanome und Blasenkrebs vermutet [28]. Wenn ältere, (postmenopausale) Frauen zur Vorbeugung von Knochenbrüchen Calcium und Vitamin D einnehmen, scheint deren Erkrankungsrisiko stark zu sinken [29].
Brustkrebsauslösung durch eine Infektion („Brustkrebsvirus“) wurde bisher nicht nachgewiesen. Brustimplantate verursachen keinen Brustkrebs [30], ebenso wenig wie das Tragen von Büstenhaltern [30].
Seit einigen Jahren wird außerdem eine aktive Rolle von Endothelin und Endothelin-konvertierendem Enzym (ECE) im Rahmen der Brustkrebsentstehung und insbesondere der Metastasierung von Brustkrebszellen diskutiert.[31]
Früherkennung und Screening
Etwa 80 bis 90 % aller Geschwulste in der weiblichen Brust wurden bisher von den Frauen selbst zufällig entdeckt. Diese tast- und sichtbaren Tumoren sind bei ihrer Entdeckung oft schon relativ groß und sind deshalb meist mit einer schlechten Prognose verbunden. Durch konsequente Früherkennung kleinerer, nicht tastbarer Tumoren könnte die Sterblichkeit großen Studien zufolge um 25 % gesenkt werden. Zur Früherkennung dienen Programme zur systematischen Selbstuntersuchung sowie die Screening-Mammographie.
Selbstuntersuchung
Systematische Schulungen der Frauen zur Brust-Selbstuntersuchung sind in ihrem Nutzen umstritten. Nicht jede Brustkrebserkrankung führt zu einer tastbaren Geschwulst. Umgekehrt ist nur etwa jede zwölfte selbst ertastete Veränderung bösartig [32]. Studien zufolge senkt die systematische Selbstuntersuchung der Brust die Sterblichkeit nicht [33] [34]. Die US-amerikanische Preventive Services Task Force (USPSTF) gibt wegen der unzureichenden Datenlage keine Empfehlung für oder gegen die Brustselbstuntersuchung [35]. Die kanadische Task Force on Preventive Health Services gab 2001 eine Empfehlung gegen die Selbstuntersuchung ab [36], weil die Entdeckungsrate schlecht und falsch positive Befunde häufig seien.
Zum Erlernen der Selbstuntersuchung gibt es Brustmodelle aus Silikon, die verschiedenen Knotentypen enthalten, beigefügt sind Begleitvideo und Anleitung. Die Kosten hierfür werden jedoch in Deutschland nicht von der Krankenkasse bzw. Pflegeversicherung übernommen.[37]
In Deutschland wird die Selbstuntersuchung von den medizinischen Fachgesellschaften empfohlen [38], weil sie zur Bewußtseinsbildung der Frauen beitrage und so die eigentliche Früherkennung durch apparative Verfahren begünstige. Die Selbstuntersuchung, die monatlich zirka 5 bis 7 Tage nach Einsetzen der Regelblutung durchgeführt werden soll, erfolgt nach einem bestimmten, sich immer wiederholenden Muster. Bei ertasteten Auffälligkeiten sollen sich Frauen bei einem Arzt vorstellen.
Ärztliche Krebsfrüherkennung
Die klinische Untersuchung der Brust durch einen Arzt ist Bestandteil des gesetzlichen Krebs-Früherkennungsprogramms ab dem 30. Lebensjahr. Für die Aussagefähigkeit der ärztlichen Tastuntersuchung gilt im Prinzip dieselbe Einschränkung wie für die Selbstuntersuchung.
Bildgebende Verfahren
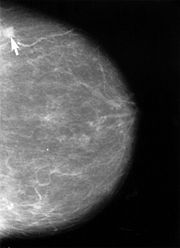
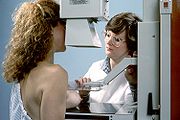
Die Röntgen-Mammographie ist einer S3-Leitlinie (Medizinische Leitlinie der höchsten Qualitätsstufe) zufolge bis jetzt das einzige Verfahren, dessen Eignung zur Erkennung früher Karzinome und Karzinomvorstufen allgemein anerkannt ist [38]. Die Mamma-Kernspintomographie ist möglicherweise überlegen, jedoch für ein Massenscreening zu teuer [39]. In Deutschland wird deshalb ein qualitätsgesichertes Mammographie-Screening-Programm auf der Grundlage der „Europäischen Leitlinien für die Qualitätssicherung des Mammographie-Screenings“ für Frauen von 50–69 Jahren aufgebaut. Insgesamt 94 dieser Einheiten sollen bis Ende 2008 in ganz Deutschland errichtet sein. Etwa 84 Regionen bieten das Mammographie-Screening bereits für die Frauen zwischen 50 und 69 Jahren, an (Stand Januar 2008). [40] In den USA gibt es die Empfehlung, das Mammographiescreening bereits mit 40 Jahren zu beginnen[35].
Durch Dreifachbefundung und weitere Diagnostik soll erreicht werden, dass möglichst wenige gutartige Mammatumoren biopsiert oder gar entfernt werden. Die EUREF-Richtlinie verlangt, dass in mindestens 50 % der genommenen Gewebeproben bösartige Tumoren nachgewiesen werden können; [41] in manchen Untersuchungsprogrammen werden bis zu 80 % erreicht[42].
CAD-Systeme (Computer Assisted Detection) können den Radiologen bei der Auswertung der Mammographien unterstützen. Solche Untersuchungen können in den USA und den Niederlanden von den Krankenkassen bezahlt werden. Nach bisher veröffentlichten Studien verbessern die bislang verfügbaren Geräte die Erkennungsrate jedoch nicht [43]. In den europäischen Screeningprogrammen wird daher die Doppelbefundung durch zwei Ärzte (und durch einen dritten bei Auffälligkeiten) bevorzugt.
Die Mammographie ist bei Frauen mit dichtem Drüsengewebe in ihrer Aussagekraft begrenzt. Bei extrem dichtem Gewebe werden etwa 50 % der Brusttumoren mit der Mammographie nicht entdeckt. Dies betrifft in erster Linie jüngere Frauen. Frauen mit dichtem Gewebe im Mammogramm wird daher der Einsatz eines zweiten Untersuchungsverfahrens (in der Regel Sonographie, im Einzelfall auch Kernspin-Mammographie) empfohlen.
Diagnose
Klinische Untersuchung
Bei der Selbstuntersuchung oder bei der ärztlichen, klinischen Untersuchung kann ein neuer, unscharf begrenzter Tumor auffallen. Weitere Anzeichen sind Verhärtungen, Größen- und Umrissveränderungen der Brust im Seitenvergleich, verminderte Bewegung der Brust beim Heben der Arme, bleibende Hautrötung, Hauteinziehung oder Apfelsinenhaut (verdickte Haut mit eingezogenen Stellen), Einziehung oder Entzündung der Brustwarze, Absonderungen aus der Brustwarze. Knoten in der Achselhöhle können Lymphknoten-Metastasen entsprechen. Allgemeinsymptome bei weit fortgeschrittenen Erkrankungen sind u. a. Leistungsknick, ungewollter Gewichtsverlust oder Knochenschmerzen.
Bildgebende Diagnostik
Werden bei der Tast- oder Ultraschalluntersuchung Auffälligkeiten gefunden, folgt als nächste Untersuchung üblicherweise die Mammographie: Die Röntgenaufnahmen werden aus zwei Blickrichtungen (von der Seite und von oben) aufgenommen, bestimmte Veränderungen manchmal zusätzliche Aufnahmen. Die Galaktographie wird nur durchgeführt, wenn die Brustwarzen Sekret absondern.
Umgekehrt werden mit der Mammographie entdeckte Veränderungen immer sonographisch nachuntersucht. Dabei werden gutartige Zysten erkannt. Die Leitlinie der Kassenärztlichen Bundesvereinigung schreibt hierfür Schallköpfe mit mindestens 5 MHz Frequenz vor [44].
Die Kernspintomographie der Brust (MR-Mammographie, MRT) wird zur Zeit nur empfohlen für das invasive lobuläre Mammakarzinom zur Bestimmung der Resektions-Grenzen und allgemein bei Verdacht auf das Vorliegen mehrerer Tumorherde[45], gegebenenfalls ist auch eine MRT-gesteuerte Biopsie möglich. Nach brusterhaltender Therapie kann die MRT eingesetzt werden, um zwischen narbigen Verdichtungen in der operierten Brust und neuem Tumorwachstum zu unterscheiden. Außerhalb der ambulanten Versorgung der gesetzlich krankenversicherten Patientinnen gibt es weitere Indikationen.
Die Positronen-Emissions-Tomographie ist derzeit keine Routinemethode, kann jedoch in Einzelfällen oder im Rahmen klinischer Studien eingesetzt werden, um nach Lymphknotenmetastasen oder nach dem Tumor in der Brust zu suchen, wenn dieser mit anderen Methoden nicht gefunden werden kann.
Knochenszintigramme, Computertomographien, Röntgenaufnahmen der Lunge, Sonographien der Leber und ggf. Kernspintomographien dienen dazu, nach Metastasen zu suchen, also die Ausbreitung der Erkrankung zu erkennen.
Gewebeentnahmen
Wurde mit dem Ultraschall und der Mammographie ein Tumor diagnostiziert, wird dieser auf seine Gut- oder Bösartigkeit untersucht. Dazu werden jedem Tumor mittels Stanzbiopsie, in seltenen Fällen mittels Vakuumbiopsie, mehrere Gewebeproben entnommen und unter dem Mikroskop auf Krebszellen untersucht. Methode der Wahl für die Probenentnahme tastbarer und sonografisch sichtbarer Befunde ist die Stanzbiopsie, für im Kernspintomogramm sichtbare Befunde und Mikrokalzifikationen die stereotaktisch gestützte Vakuumbiopsie. Wurde der Tumor als bösartig erkannt, wird das Karzinom durch weitere Untersuchungen des entnommenen Gewebes näher bestimmt. Hierzu gehören der Status der Hormon- und HER2/neu-Rezeptoren sowie der Entartungsgrad.
Nach der Operation wird das aus der Brustdrüse entfernte Operationspräparat in der histologischen Untersuchung seine exakte Größe gemessen und das Gewebe auf weiteren Befall untersucht. Die entfernten Lymphknoten werden auf Metastasen geprüft. Die Größe des Karzinoms und die Anzahl der befallenen Lymphknoten sind für die TNM-Klassifikation, Prognose und weitere Behandlung von Bedeutung. Das Operationspräparat wird auch daraufhin vermessen, ob der Abstand zwischen dem Karzinom und dem verbliebenen, gesunden Gewebe ausreichend groß ist. Sollte dies nicht der Fall sein, kann eine Nachoperation nötig werden, damit ein angemessener Sicherheitsabstand zwischen gesundem und erkranktem Gewebe erreicht wird.
Klassifikation
.jpg) Histologisches Bild eines duktalen Carcinoma in situ der Brust
Histologisches Bild eines duktalen Carcinoma in situ der BrustDie Klassifikation eines Tumors ist dessen exakte Beschreibung auf der Grundlage der pathologischen Untersuchung einer Gewebeprobe oder des OP-Präparats und der entnommenen Lymphknoten.
Histologische Klassifikation
Der häufigste Tumortyp des Mammakarzinoms ist mit etwa 70-80% ein Adenokarzinom ohne besondere Merkmale; aufgrund der Entstehung aus dem Epithel der Milchgänge wird dieser Tumortyp als invasives duktales Karzinom (IDC) bezeichnet. Seltener (in etwa 10–15 %) sind das invasive lobuläre Karzinom (ILC), das invasive tubuläre, muzinöse, medulläre, papilläre Karzinom (je etwa 2 %), gemischte und andere Tumortypen. Diese Tumortypen unterscheiden sich in ihrer klinischen Präsentation, den Befunden bei bildgebenden Untersuchungen, dem histologischen Ausbreitungsmuster und in der Prognose. Bei fast allen Tumortypen liegt auch eine nicht invasive (duktale oder lobuläre) Tumorkomponente vor, aus der sie hervorgegangen sind und die für die Größe der Operation mitentscheidend ist. Seltener geht das Mammakarzinom direkt aus gutartigen Erkrankungen hervor (von denen einige bei Mammatumor genannt sind, es handelt sich hier aber nicht um bösartige Tumorerkrankungen). Das inflammatorische Mammakarzinom bezeichnet keinen histologischen Tumortypen, sondern eine sicht- und tastbare Veränderung, nämlich eine massive Entzündungsreaktion mit Rötung und Schwellung der gesamten Brust bei fortgeschrittenem Befall der Brust und des umgebenden Lymphsystems.
Die nicht-invasiven Karzinome sind definiert als Karzinome innerhalb der Brustdrüsengänge (duktales Carcinoma in situ, DCIS) oder -läppchen (lobuläres Carcinoma in situ, LCIS) ohne Stromainvasion. Eine Sonderstellung nimmt der Morbus Paget der Brustwarze (Mamille) ein, der auf einer nicht-invasiven Tumorausbreitung in die Mamillenhaut beruht und in der Regel mit einem intraduktalen Mammakarzinom, seltener auch mit einem invasiven Mammakarzinom assoziiert ist. Dieses Paget-Karzinom der Brustwarze kann klinisch mit einem Ekzem oder gutartigen Geschwür verwechselt werden.
Differenzierungsgrad
Die histologischen Tumortypen werden anhand struktureller und zellulärer Eigenschaften sowie ihrer Kernteilungsrate unterteilt in drei Differenzierungsgrade (synonym Malignitätsgrad, englisch auch Grading). Die Einstufung des invasiven Karzinoms beruht auf den drei Kriterien Tubulusbildung (Strukturveränderung der Zellkerne), Kernpolymorphie (Gestalt und Größe der Zellen) und Mitoserate (Teilungsrate der Zellen). Je höher das Grading, desto ungünstiger ist das Verhalten der Tumorzellen. Man unterscheidet Tumoren mit Differenzierungsgrad 1, 2 oder 3 (G1 = gut differenziert, G2 = mäßig differenziert, G3 = gering differenziert).
TNM-Klassifikation
Die TNM-Klassifikation beschreibt die Größe des Tumors (T), die Anzahl der befallenen Lymphknoten (N) und eine eventuelle Fernmetastasierung (M). Die tabellierte Kurzfassung der TNM-Klassifikation für Brustkrebs:
T
TumorgrößeT0 kein Tumor nachweisbar Tis Carcinoma in situ, nicht invasiv T1mic Mikroinvasion bis 0,1 cm T1 bis 2 cm T2 > 2 cm bis 5 cm T3 > als 5 cm T4 jede Größe mit Ausdehnung
auf die Brustwand oder HautN
Befallene LymphknotenN0 keine N1 1-3 in der Achsel N2 4-9 in der Achsel N3 10 oder mehr in der Achsel oder
unter/über dem SchlüsselbeinM
(Fern-) MetastasenM0 keine nachweisbar M1 nachweisbar (meist
Lunge, Leber, Knochen)Stadieneinteilung
Aus der TNM-Klassifikation (bzw. pTNM-Klassifikation, das 'p' steht für histologisch gesicherte Daten) des Mammakarzinoms ergibt sich die Stadiengruppierung nach UICC bzw. AJCC (TNM 6. Aufl., 2003) wie folgt:
Stadium 0 Tis N0 M0 Stadium I T1 N0 M0 Stadium IIA T0,T1 N1 M0 T2 N0 M0 Stadium IIB T2 N1 M0 T3 N0 M0 Stadium IIIA T0,T1,T2 N2 M0 T3 N1,N2 M0 Stadium IIIB T4 N0,N1,N2 M0 Stadium IIIC Jedes T N3 M0 Stadium IV Jedes T Jedes N M1 Hormonrezeptor- und HER2-Status
Der Östrogenrezeptor- und Progesteronrezeptorstatus (ER- und PgR-Expression) wird ebenfalls histologisch, genauer immunhistologisch untersucht. Man bestimmt den Prozentsatz derjenigen Tumorzellen, an denen sich die Rezeptoren nachweisen lassen und errechnet aus Prozentsatz und der Färbeintensität einen 12-stufigen Immunreaktiven Score (IRS), oder den international gebräuchlicheren 8-stufigen Allred-Score.
Färbeintensität (IS) Positive Zellen (PP) 0 keine Reaktion 0 keine 1 schwache Reaktion 1 weniger als 10 % 2 mäßige Reaktion 2 zwischen 10 und 50 % 3 starke Reaktion 3 zwischen 51 und 80 % 4 mehr als 80 % IRS 0–2 negativ 3–4 schwach positiv 6–8 mäßig positiv 9–12 stark positiv Beim HER2-Rezeptor, der für die Entscheidung, ob eine Nachbehandlung mit Trastuzumab sinnvoll ist, wird ein 4-stufiger Score angewandt, der sich nach der immunhistochemischen Färbeintensität richtet (ASCO-Empfehlung 2007 [46]). Lassen sich keine Zellen anfärben, ist das Ergebnis negativ: Score 0. Auch der Score 1+ ist negativ, d. h. eine Behandlung mit Trastuzumab wäre ohne Effekt auf den Tumor. Bei einer mittleren Färbeintensität (Score 2) wird der Tumor mit dem FisH-Test nachuntersucht und anhand Vermehrung (Amplifikation) des HER2-Gens entschieden, ob es sich um einen HER2-positiven Tumor handelt.
Positive Zellen Membranfärbung Färbeintensität Score keine keine keine 0 1 % oder mehr nicht komplett schwach 1+ weniger als 10 % vollständig schwach bis mäßig 1+ 10 % oder mehr vollständig schwach bis mäßig 2+ 30 % oder weniger vollständig stark 2+ mehr als 30 % vollständig stark 3+ Risikogruppen, Einteilung nach Ergebnissen der Konsensuskonferenzen in St.-Gallen
Die alle zwei Jahre in St. Gallen abgehaltene Konsensuskonferenz beschäftigt sich vor allem mit der adjuvanten Therapie. Um die Chemo- und Hormontherapie möglichst zielgerecht einsetzen zu können, werden der Empfehlung von 2007 folgend die operierten Patientinnen in drei Risiko-, besser Behandlungsgruppen eingeteilt [47]:
Niedriges Risiko Mittleres Risiko Hohes Risiko Anzahl der befallenen
Lymphknoten:keiner 1 bis 3 oder
keiner, aber 1 weiteres Kriterium:mehr als 4 oder
1 bis 3 undTumorgröße: T1 (max. 2 cm) T2 bis T4 (größer als 2 cm) Differenzierung: G1 G2 und G3 Tumoreinbruch: Invasion in Gefäße Hormonstatus: ER/PR-positiv (Östrogen-/Progesteron-positiv) HER2/neu-Status: HER2/neu-negativ HER2/neu-positiv HER2/neu-positiv Alter: 35 Jahre und älter oder jünger als 35 Jahre Molekulare Tumorklassifikation
Anhand des Genexpressionsprofils, welches mit DNA-Microarrays aus dem Tumorgewebe gewonnen werden kann, kann man fünf verschiedene Hauptgruppen des Mammakarzinoms unterscheiden: Hormonrezeptorpositive Tumoren mit geringer bzw. höherer Aggressivität (genannt Luminal-A und Luminal-B), HER2-positive Tumoren (erbB2-Phänotyp) und Hormonrezeptor- und HER2-negative Karzinome mit oder ohne Basalzell-Eigenschaften (basal-like und normal-like Phänotypen). Die zur Zeit noch experimentelle molekulare Tumorklassifikation könnte in Zukunft eine bessere Abschätzung der Prognose und der voraussichtlichen Wirkung der adjuvanten Hormon- und Chemotherapie ermöglichen [48].
Therapie
Zur Vereinheitlichung und Verbesserung der Krankenversorgung gibt es in Deutschland seit 2003 im Auftrag der DKG und der Deutschen Gesellschaft für Senologie von OnkoZert zertifizierte Brustzentren an Krankenhäusern[49] und seit 2004 ein Disease-Management-Programm für Brustkrebs[50], an dem sich auch niedergelassene Ärzte beteiligen können. Die gemeinsame Leitlinie der Stufe S3 der Deutschen Krebsgesellschaft und der medizinischen Fachgesellschaften ist für diese Programme die Orientierung zur Behandlung von Brustkrebs. Diese Leitlinie wird regelmäßig aktualisiert, zuletzt im Februar 2008.[45]
Die Strategie zur Brustkrebsbehandlung wird meist im Rahmen einer Tumorkonferenz geplant, an der sich Gynäkologen, internistische Onkologen, Radiologen, Strahlentherapeuten und Pathologen beteiligen. Die Einbindung der Patientin in die Entscheidungsfindung ist wie bei jeder eingreifenden medizinischen Maßnahme von großer Bedeutung (siehe informierte Einwilligung). Auch der deutsche Gesetzgeber spricht in der DMP-Richtlinie deutlich vom Status der aufgeklärten Patientin [51].
Die Therapie der Brustkrebserkrankung soll im Frühstadium eine Heilung, beim metastasierten Karzinom eine Lebenszeitverlängerung und im Spätstadium eine Linderung der Krankheitsbeschwerden erreichen. Bei der Wahl der konkreten Therapie steht die Erhaltung der Lebensqualität im Vordergrund [51][45]. Darum wird neben den weiter oben beschriebenen Klassifikationen des Tumors auch die körperliche, psychosoziale und emotionale Situation der Patientin berücksichtigt. Eine „Standardtherapie“ gibt es nicht, die Berücksichtigung aller verschiedener Faktoren führt zu einer individuellen Anpassung der Therapie an die Krankheit und an die jeweilige Patientin [51][45].
Brustkrebs kann sich sehr schnell im Körper ausbreiten und wird daher schon in frühen Stadien mit einer systemischen (im ganzen Körper wirksamen) Therapie behandelt. Diese nach dem amerikanischen Chirurgen Bernard Fisher benannte „Fisher-Doktrin“ ist die Grundlage der Chemo- und Hormontherapie beim Brustkrebs[52]. Fast immer besteht die Behandlung heute aus einer Kombination verschiedener Therapieformen. Werden zusätzliche Maßnahmen vor einer Operation durchgeführt, werden sie als neoadjuvant bezeichnet, werden sie nach einer Operation eingesetzt, nennt man sie adjuvant.
Neoadjuvante Therapie
In einigen Fällen wird eine Chemotherapie oder antihormonelle Therapie schon vor der chirurgischen Entfernung des Tumors durchgeführt [53]. Diese primäre, oder neoadjuvante Therapie hat einerseits das Ziel, den Tumor zu verkleinern, um eine vollständige Entfernung des Tumors oder sogar eine brusterhaltende Operation zu ermöglichen, andererseits kann an der mit den neoadjuvanten Verfahren erreichbaren Veränderung der Erfolg einer weiteren, adjuvanten Behandlung abgeschätzt werden. Standard ist die neoadjuvante Therapie beim inflammatorischen Karzinom und bei zunächst inoperablen (T4-)Tumoren. Die Chemotherapieschemata sind die gleichen wie bei der postoperativen Behandlung (siehe unten).
Operation
Mit der Operation der Brustkrebserkrankung werden zwei Ziele verfolgt: Einerseits soll durch möglichst vollständige Entfernung der entarteten Zellen eine Ausbreitung (Metastasierung) der Tumorzellen in andere Körperregionen verhindert werden, sofern das noch nicht geschehen ist, andererseits soll ein Wiederauftreten der Krankheitszeichen an Ort und Stelle (ein Rezidiv) verhindert werden.
Brusterhaltende Chirurgie vs. Mastektomie
Eine brusterhaltende Therapie (BET) ist heute bei 60–70 % der Erkrankten möglich [54], wenn die Relation zwischen der Tumorgröße und dem Brustvolumen günstig und der Tumor noch nicht in die Muskulatur oder Haut eingedrungen ist. Bei dieser Operation wird entweder der Tumor mit dem umliegenden Gewebe, ein größeres Segment oder ein ganzer Quadrant entfernt. Um ein kosmetisch ansprechendes Ergebnis zu erhalten, wird bei größerer Gewebeentfernung vor allem aus beiden unteren Quadranten eine sogenannte intramammäre Verschiebeplastik vorgenommen. Dabei wird die Brustdrüse ganz oder teilweise von Haut und Muskulatur gelöst und so verschoben, dass nach der Operation trotz des Gewebeverlustes eine ausgeglichene Brustform erhalten bleibt. Ist eine Verschiebeplastik nicht möglich, kann die Brust entweder direkt nach der Tumorentfernung oder nach Abschluss aller Behandlungen rekonstruiert werden.
Sollte eine Brusterhaltung nicht möglich sein, wird der gesamte Brustdrüsenkörper und ein Teil der darüber liegenden Haut entfernt (Ablatio, Mastektomie). Die Empfehlung zur Mastektomie wird ausgesprochen, wenn:
- der Tumor sehr groß ist (> 3 cm) oder den Brustmuskel infiltriert hat,
- ein inflammatorisches Karzinom diagnostiziert wurde,
- ein ausgedehnter Befall der Lymphgefäße der Brustdrüse nachgewiesen wurde,
- der Tumor ausgedehnte „Arme“ in den Milchgänge gebildet hat,
- die gesamte Brustdrüse eine durch die Mammographie nachgewiesene Mikroverkalkung enthält,
- der Tumor trotz Nachoperation nicht mit einem ausreichenden Sicherheitsabstand zum gesunden Gewebe entfernt werden konnte,
- die Patientin dies wünscht. Manche Patientinnen entscheiden sich gegen die Möglichkeit zur brusterhaltenden Operation, um sich sicherer zu fühlen oder um die sonst notwendige Strahlentherapie zu vermeiden.
Die Empfehlung zur Mastektomie wird auch ausgesprochen, wenn ein multizentrisches (Tumorknoten in mehreren Quadranten) oder multifokales (mehrere Tumorknoten im selben Quadranten) Karzinom diagnostiziert wurde. Diese Empfehlung kann manchmal relativiert werden, wenn der Operateur alle Tumoren mit einem ausreichenden Sicherheitsabstand zum gesunden Gewebe entfernen kann [55] [56]. Auch, wenn eine Krebserkrankung schon in andere Organe metastasiert hat, kann der ursprüngliche Tumor schonender operiert werden, wenn das radikale chirurgische Vorgehen keinen Vorteil bringen würde.
Achsellymphknoten
Die Lymphknoten der Achsel sind meist der erste Ort, an dem sich Metastasen bilden. Um diesen Befall zu erfassen, werden die Lymphknoten, zumindest einige von ihnen, bei der Operation in der Regel mit entfernt.
Um die Folgeschäden (Lymphödem) so gering wie möglich zu halten, kann zunächst nur ein einzelner Lymphknoten entfernt und untersucht werden, wenn der Tumor in der Brust kleiner als 2 cm ist und die Achsellymphknoten nicht tastbar sind [57]. Dazu wird in die betreffende Brust ein Farbstoff oder ein Radionuklid injiziert, um den Lymphabfluss darzustellen. Der erste, Lymphknoten, in dem das eingespritzte Material nachgewiesen werden kann, wird herausoperiert und untersucht. Nur wenn dieser sogenannte Wächterlymphknoten (sentinel node) von Tumorzellen befallen ist, werden die übrigen Lymphknoten der Achselhöhle ebenfalls entfernt. Auch wenn der Wächterlymphknoten nur von einer Mikrometastase befallen ist, wird zur Zeit eine Ausräumung der Achselhöhle empfohlen, ob in dieser Situation auf die Entfernung der übrigen Lymphknoten verzichtet werden kann, wurde noch nicht mit einer Studie belegt (Stand 2/2008).
Adjuvante Therapie
Fast alle Patientinnen erhalten nach der Operation eine adjuvante (unterstützende) Behandlung.
Chemotherapie
Nach der Operation folgt für die meisten Patientinnen eine Chemotherapie, um möglicherweise verbliebene Tumorzellen abzutöten. Welche Medikamente verabreicht werden, hängt vom Zustand der Patientin und von der Klassifikation des Tumors ab, vor allem von der Risikogruppe nach der St.-Gallen-Empfehlung. Die Behandlung wird in mehreren Zyklen durchgeführt, beispielsweise insgesamt viermal im Abstand von drei Wochen oder sechsmal in Abstand von zwei Wochen. Der Zeitabstand zwischen den einzelnen Gaben soll dem Körper einerseits die Gelegenheit zur Regeneration geben, andererseits hofft man darauf, dass Mikrometastasen (ruhende Tumorzellen) bzw. Krebsstammzellen in den Erholungsphasen mit der Teilung beginnen und mit der erneuten Zuführung der Zytostatika zerstört werden können.
In der Regel werden die Zytostatika als Kombinationen eingesetzt. Die häufigsten Schemata sind zur Zeit AC oder EC, FAC oder FEC. Wenn die Lymphknoten mit Metastasen befallen waren, wird eine Ergänzung der jeweiligen Kombination mit Taxanen empfohlen (St. Gallen, 2007). Das ältere CMF-Schema wird kaum noch verwendet. (A = Adriamycin, C = Cyclophosphamid, E = Epirubicin, F = Fluorouracil, M = Methotrexat, T = Taxane)
Bei HER2/neu-positiven Tumoren wird in der Regel nicht auf eine Chemotherapie verzichtet, da die Therapie mit Trastuzumab zur Zeit nur als ergänzende Behandlung verstanden wird („Antikörper-Therapie“, siehe unten). Die Dauer und die Zusammensetzung der Chemotherapie wird vom Ausmaß der befallenen Lymphknoten mitbestimmt (St. Gallen 2007).
Wenn der Tumor hormonabhängig und die Lymphknoten frei von Metastasen sind, kann unter Umständen auf eine Chemotherapie verzichtet werden. Bei dieser Konstellation können mit einer antihormonellen Therapie ähnliche Ergebnisse erzielt werden (St. Gallen 2007).
Bestrahlung
Nach der brusterhaltenden Operation sollte eine Strahlentherapie der Restbrust erfolgen[45]. Sie senkt die Rezidivrate von 30 auf unter 5 %. Mikroskopisch kleine (nicht mit bloßem Auge erkennbare) Tumorreste können auch bei sorgfältigster Operation in der Brustdrüse verbleiben.
Auch nach einer Mastektomie wird zur Nachbestrahlung geraten, wenn der Tumor größer als 5 cm war (T3 oder T4), die Brustdrüse mehrere Tumore enthielt oder der Tumor bereits in Haut oder Muskulatur eingedrungen war. Auch der Befall von Lymphknoten ist ein Anlass zur Nachbestrahlung der Brustwand, insbesondere bei mehr als drei befallenen Lymphknoten.
Das ehemalige Tumorgebiet soll bei Frauen unter 60 Jahren mit einer um 10-16 Gy höheren Dosis bestrahlt werden, damit sich an den Schnitträndern keine Rezidive ausbilden können.
Die Strahlentherapie beginnt zirka 4–6 Wochen nach der Operation und dauert sechs bis acht Wochen.
Antihormonelle Therapie
Ist das Karzinom hormonsensitiv, wird zusätzlich eine Therapie mit Hormonantagonisten durchgeführt. Es gibt verschiedene, vom menopausalen Status der Frau abhängige Varianten.
Vor der Menopause:
Eine chirurgische Ovariektomie oder radiotherapeutische Ausschaltung der Ovarfunktion wird nur noch selten vorgenommen. Studien zufolge genügt eine temporäre Ausschaltung der Hormonproduktion über zwei Jahre, die medikamentös erreicht werden kann [53].
Bei Frauen, die noch die Periode haben, wird schon durch Chemotherapie die Hormonfunktion der Eierstöcke gestört [58]. Dieser Effekt richtet sich auch gegen die hormonabhängigen Tumorzellen und sind daher erwünscht. Frauen mit Kinderwunsch oder Frauen, denen das Risiko einer vorzeitigen Menopause zu groß ist[59], können ihre Eierstöcke mit GnRH-Analoga (die die ovariale Produktion von Östrogen und Progesteron unterdrücken) vor der schädigenden Wirkung schützen und gleichzeitig die Hormonausschaltung bewirken. GnRH-Analoga werden in der Regel über zwei Jahre gegeben [53].
Nach der Chemotherapie wird normalerweise ein Estrogen-Rezeptor-Modulator wie Tamoxifen, welcher die Anbindung des körpereigenen Östrogens an den Östrogen-Rezeptoren des Tumors verhindert, für 5 Jahre gegeben [60]. Aromatasehemmer sind vor der Menopause nicht angezeigt.
Nach der Menopause:
Ist die Patientin postmenopausal, erhält sie für in der Regel fünf Jahre entweder Tamoxifen oder einen Aromatasehemmer, welcher durch eine Enzymblockade die Bildung von Östrogen im Muskel- und Fettgewebe unterbindet. Neuere Studienergebnisse deuten an, dass die Aromatasehemmer wirksamer sind als das Tamoxifen, das heißt, die krankheitsfreie Überlebenszeit steigt an. In Studien wird der Aromatasehemmer manchmal sofort verwendet (upfront), in der Regelbehandlung erst nach zwei bis drei Jahren unter Tamoxifen (switch, zu Deutsch Wechsel), oder nach fünf Jahren (extended) [53]. Die jeweiligen Nebenwirkungen der Substanzen müssen bei der Entscheidung berücksichtigt werden. Eine weitere Möglichkeit besteht in der Gabe eines reinen Estrogen-Rezeptor-Antagonisten.
Bei vielen Patientinnen mit hormonabhängigen Tumoren verliert Tamoxifen nach einigen Jahren seine Schutzwirkung (sogenannte Tamoxifenresistenz). Laborversuchen zufolge kann im Gegenteil sogar eine Beschleunigung des Zellwachstums eintreten [61]. Betreffende Frauen sollten besser mit anderen Substanzen behandelt werden. Es ist bislang aber noch nicht möglich, das Verhalten eines individuellen Tumors in dieser Beziehung vorauszusagen. Ein Hinweis könnte das gleichzeitige Auftreten einer HER2/neu- und AIB1-Expression an einem ER-positivem Tumor sein [62].
Antikörper
Etwa ein Viertel aller Mammakarzinome weisen eine Überexpression des HER2/neu-Rezeptors auf. Der Nachweis dieses Rezeptors steht für einen aggressiven Krankheitsverlauf und eine ungünstige Prognose, ist aber auch Bedingung für die Behandlung mit dem Antikörper Trastuzumab.
1998 wurde der Wirkstoff (Handelsname Herceptin®) in den USA und 2000 in der Europäischen Union zunächst für Patientinnen mit metastasiertem Brustkrebs zugelassen. Trastuzumab ist ein monoklonaler Antikörper gegen den Wachstumsrezeptor HER2/neu auf der Zelloberfläche von Krebszellen. Studien ergaben, dass mit dieser sogenannten Targeted-Therapy-Substanz das Risiko eines Rezidivs (Wiederauftretens) um etwa 50 % gemindert werden konnte. Seit 2005 deutet sich in klinischen Studien an, dass auch Frauen ohne Metastasen profitieren. Seit 2006 ist Trastuzumab deshalb auch für die adjuvante Therapie zugelassen.
Therapie des metastasierten Mammakarzinoms
Werden Fernmetastasen nachgewiesen, ist in der Regel keine Heilung mehr möglich. Deshalb richtet sich die Behandlung auf die Lebenszeitverlängerung und den Erhalt einer angemessenen Lebensqualität mit einer langfristigen Stabilisierung der körperlichen und psychischen Verfassung.
Rezidive und Metastasen können operativ entfernt oder mit Strahlentherapie behandelt werden. Trotz der Nebenwirkungen kann unter Umständen auch mit der Verabreichung einer Chemo-, Hormon- oder Antikörpertherapie eine Erhöhung der Lebensqualität erreicht werden.
Wenn der Krebs in seiner Ausbreitung so weit fortgeschritten ist, dass er nicht mehr zurückgedrängt werden kann, richtet sich die Behandlung vor allem auf die Beherrschung von Schmerzen und anderen Krankheitsbeschwerden. Zur Palliativmedizin gehört die psychosoziale Betreuung und eine Schmerzbehandlung, die schnell und vollständig erfolgen sollte und eine frühzeitige und ausreichende Gabe von Opiaten einschließt, siehe WHO-Stufenschema.
Nachsorge
Die Nachsorge der behandelten Patientinnen dauert in der Regel fünf Jahre und richtet sich zumeist nach den Leitlinien der Deutschen Krebsgesellschaft. Auf Nebenwirkungen der Strahlentherapie (Lymphödem, Lungen- oder Herzprobleme), der Chemotherapie (Blutbildveränderungen, Organschäden) und der Hormontherapie (Thrombosen, Osteoporose) muss besonders geachtet werden. Neben der Befragung und klinischen Untersuchung soll in den ersten drei Jahren, da hier die meisten Rezidive auftreten, alle sechs Monate eine Mammographie angefertigt werden. Im vierten und fünften Jahr erfolgt die Mammographie – ebenso wie bei der zweiten, gesunden Brust von Anfang an – jährlich. Zur Verlaufskontrolle können in der Blutuntersuchung die Tumormarker CA 15-3 und CEA bestimmt werden, was allerdings nicht in den Richtlinien vorgesehen ist und meistens eher bei konkretem Verdacht der Fall ist. Es muss bei jeder einzelnen Patientin sehr sorgfältig abgewogen werden, ob die Nachsorge in der hier angegebenen Form tatsächlich durchgeführt werden soll; jede kleine nachgewiesene Veränderung kann eine erhebliche psychische Belastung nach sich ziehen, die wiederum die Lebensqualität entscheidend beeinflussen kann.
Für eine einheitliche Qualität bei der Nachbetreuung bieten die deutschen gesetzlichen Krankenkassen seit 2004 das Disease-Management-Programm „Brustkrebs“ an. Die teilnehmenden Ärzte orientieren sich bei der Therapie an den jeweils aktuellen Leitlinien zur Behandlung und Nachsorge des Brustkrebses. Eine Teilnahme ist bei allen Ärzten möglich, die sich diesen qualitätssichernden Programmen angeschlossen haben. Für die Patientinnen bedeutet die Teilnahme an diesem Programm eine Einschränkung der freien Arztwahl.
Einzelnachweise
- ↑ Marilyn A Roubidoux: Breast cancer, male. Emedicine, 2005
- ↑ Robert-Koch-Institut – Krebs in Deutschland 2003–2004: Brustdrüse der Frau
- ↑ Alexander Katalinic, Carmen Bartel: Epidemiologie Mammakarzinom. Universität Lübeck, 2006.
- ↑ WHO/IARC: World Cancer Report. Lyon 2003
- ↑ Brustkrebs bei Frauen häufigste Todesursache, Ärzte-Zeitung, 1. September 2008, http://www.aerztezeitung.de/extras/druckansicht/?sid=509044&pid=514995
- ↑ Backe, Jael: Brustkrebs beim Mann. Dtsch Arztebl 2002; 99(17): A-1168 / B-970 / C-913
- ↑ a b Zusammenstellung der Daten des Statistischen Bundesamtes Deutschland aus den Jahren 2003 bis 2006, Fachserie 12, Reihe 4 Datei:Todesursache Mammakarzinom.pdf
- ↑ Deutsche Krebsgesellschaft: Patientinneninformation, 5.6.07 „Familiäre Vorbelastung“
- ↑ Antoniou A, Pharoah PD, Narod S et al. Average risks of breast and ovarian cancer associated with BRCA1 or BRCA2 mutations detected in case Series unselected for family history: a combined analysis of 22 studies. Am J Hum Genet. 72: 1117–30, 2003. PMID: 12677558
- ↑ M. R. Stratton, N. Rahman:The emerging landscape of breast cancer susceptibility. In: Nature Genetics 40/2008, S. 17–22. PMID 18163131
- ↑ Schmutzler R, Meindl A: Das hereditäre Mammakarzinom: Genetik und Prävention. In: Aktuelle Empfehlungen zur Therapie primärer und fortgeschrittener Mammakarzinome (Hrsg. C. Thomssen für die Kommission Mamma der Arbeitsgemeinschaft Gynäkologische Onkologie e. V.). Zuckschwerdt-Verlag, 2007, ISBN 3-88603-916-1
- ↑ Hemminki K, Försti A, Lorenzo Bermejo J. Surveying germline genomic landscape of breast cancer. Breast Cancer Res Treat. 2008. [Epub ahead of print] PMID 18297427
- ↑ Familial breast cancer. Lancet 2001 (358):1389-99, zitiert nach Uta Wagenmann: Auf der Suche nach dem magischen Krebs-Gen. Feitag, 26.4.02
- ↑ Schmutzler, K. u.a.: Familiärer Brust- und Eierstockkrebs: Von der Forschung zur Regelversorgung Dtsch Arztebl 102(50): A-3486, 2005
- ↑ Internet/Behelfsquelle: http://www.europadonna.at/aktuelles/brustkrebs_gen_beratung.html
- ↑ [http://www.aerzteblatt.de/v4/archiv/artikel.asp?id=58821 Siegmund-Schultze N, et al.: Hormontherapie und Brustkrebs: Ein Blick auf aktuelle Datenlage. Dtsch Ärztebl 2008 (105): A-260 / B-234 / C-230]
- ↑ U. Ackermann-Liebrich: Stillen als Prävention gegen Brustkrebs. infomed.org, November/Dezember 2002. Nach einer Veröffentlichung in The Lancet, 260/2002, S. 187–95.
- ↑ V. Beral u. a.: Breast cancer and abortion: collaborative reanalysis of data from 53 epidemiological studies, including 83.000 women with breast cancer from 16 countries. In: The Lancet 363/2004, S. 1007–16. PMID 15051280
- ↑ D. H. Brewster u. a.: Risk of breast cancer after miscarriage or induced abortion: a Scottish record linkage case-control study. In: J Epidemiol Community Health 59/2005, S. 283–7. PMID 15767381
- ↑ X. Paoletti, F. Clavel-Chapelon: Induced and spontaneous abortion and breast cancer risk: results from the E3N cohort study. In: Int J Cancer 106/2003, S. 270–6. PMID 12800205
- ↑ G. K. Reeves u. a.: Breast cancer risk in relation to abortion: Results from the EPIC study. In: Int J Cancer 119/2006, S. 1741–5. PMID 16646050
- ↑ Rice S, Whitehead SA: Phytoestrogens and breast cancer –promoters or protectors? Endocrine-Related Cancer 2006 (13):995-1015
- ↑ http://envirocancer.cornell.edu/FactSheet/Diet/fs1.phyto.cfm
- ↑ E. Nekolla: Epidemiologie des strahleninduzierten Mammakarzinoms. Dissertation, LMU München, 2004.
- ↑ F. A. Mettler u. a.: Benefits versus risks from mammography: a critical reassessment. In: Cancer 77/1996, S.903–9. PMID 8608482
- ↑ a b Women’s Health Initiative, zitiert nach Gyne online, 4.6.07
- ↑ [Reynolds P, et al.: Active smoking, household passive smoking, and breast cancer: evidence from the California Teachers Study. Journal of the National Cancer Institute 2004 (96):29-37]
- ↑ Sonnenmangel fördert Krebs!, Medical Tribune, 42. Jg., Nr. 23, 8. Juni 2007, S. 21
- ↑ J. M. Lappe u. a.: Vitamin D and calcium supplementation reduces cancer risk: results of a randomized trial. In: The American journal of clinical nutrition 85/2007, S. 1586–91. PMID 17556697
- ↑ a b cancer.org: Detailed Guide: Breast Cancer – What Are the Risk Factors for Breast Cancer? abgerufen am 6. Mai 2008
- ↑ Smollich M, Götte M, Kersting C, Fischgräbe J, Radke I, Kiesel L, Wülfing P: On the role of Endothelin-Converting Enzyme-1 (ECE-1) and neprilysin in human breast cancer. Breast Cancer Res Treat 2007 106:361-369. PMID 17295044
- ↑ Aiello EJ, et al.: Rate of breast cancer diagnoses among postmenopausal women with self-reported breast symptoms. J American Board of Family Practice 2004 (17):408-15
- ↑ Thomas DB, et al.: Randomized Trial of Breast Self-Examination in Shanghai: Final Results. Journal of the National Cancer Institute 2002 (94):1445-57
- ↑ J. P. Kösters, P. C. Gøtzsche: Regular self-examination or clinical examination for early detection of breast cancer. In: Cochrane Database Syst Rev 2/2003, S. CD003373. PMID 12804462
- ↑ a b [1]
- ↑ Jolie Ringash and the Canadian Task Force on Preventive Health Care: Preventive health care, 2001 update: screening mammography among women aged 40-49 years at average risk of breast cancer.
- ↑ Silikonmodell zur Brustselbstuntersuchung. In: Constanze Schäfer, Ingo Donieth: Hilfsmittel und Medizinprodukte. Wissenschaftliche Verlagsgesellschaft mbH. Stuttgart, 2003. ISBN 3-8047-1948-1.
- ↑ a b S3-Leitlinie „Brustkrebs-Früherkennung“ der dtsch. Fachgesellschaften, 2008
- ↑ http://www.curado.de/krebs/brustkrebs/brustkrebsvorsorge/mr-tomographie-findet-mehr-tumore/
- ↑ http://www.kooperationsgemeinschaft-mammographie.de/cms_upload/pressemitteilungen_43/PM_Start_Brandeburg_2008_01_08.pdf
- ↑ Deutsche Programmrichtlinie für das Mammographiescreening, PDF, siehe S. 43
- ↑ Fabbri S, et al.: Benign breast diseases in breast cancer screening programs in italy 2000–2001. Tumori 90 (2004):547-9
- ↑ Taylor P, Potts HW: Computer aids and human second reading as interventions in screening mammography. Eur J Cancer. 2008;44(6):798-807 Abstract
- ↑ Ultraschall-Vereinbarung gem. §135 Abs. 2 SGB V, Stand 2003
- ↑ a b c d e Interdisziplinäre S3-Leitlinie für die Diagnostik, Therapie und Nachsorge des Mammakarzinoms, 1. Aktualisierung 2008
- ↑ American Society of Clinical Oncology/College of American Pathologists Guideline Recommendations for Human Epidermal Growth Factor Receptor 2 Testing in Breast Cancer. Arch Pathol Lab Med 2007 (131): (PDF)
- ↑ Goldhirsch A, Wood WC, Gelber RD, Coates AS, Thürlimann B, Senn HJ; 10th St. Gallen conference. Progress and promise: highlights of the international expert consensus on the primary therapy of early breast cancer 2007. Ann Oncol. 2007 Jul;18(7):1133-44 (PDF) PMID 17675394
- ↑ Carey LA, et al.: Race, Breast Cancer Subtypes, and Survival in the Carolina Breast Cancer Study. JAMA 2006 (295):2492–2502
- ↑ http://www.krebsgesellschaft.de/news_detail,,,10156.html?markierung=brustzentrum
- ↑ http://www.kvb.de/servlet/PB/menu/1004909/index.html
- ↑ a b c „Anforderungen an strukturierte Behandlungsprogramme für Patientinnen mit Brustkrebs“, Anlage 3 zu §§ 28b bis 28 g der Risikostrukturausgleichs-Verordnung nach § 137f SGB Fünftes Buch (V)
- ↑ Travis K: Bernard Fisher reflects on a half-Century’s worth of breast cancer research. Journal of the National Cancer Institute 2005 (97):1636-7
- ↑ a b c d Janni W, et al.: Zertifizierte medizinische Fortbildung: Therapie des primären, invasiven Mammakarzinoms. Dtsch Ärztebl 2005 (102): A-2795 / B-2360 / C-2226 (PDF)
- ↑ Janni W, et al.: Zertifizierte medizinische Fortbildung: Therapie des primären, invasiven Mammakarzinoms. Dtsch Arztebl 2005; 102(41): A-2795 / B-2360 / C-2226
- ↑ Hartsell WF, et al.: Should multicentric disease be an absolute contraindication to the use of breast-conserving therapy? Int J Radiat Oncol Biol Phys. 30 (1994):49-53Abstract
- ↑ Gentilini O, et al.: Conservative surgery in patients with multifocal/multicentric breast cancer. Breast Cancer Res Treat. 2008, E-Publication Abstract
- ↑ Kühn T, et al.: Sentinel-Node-Biopsie beim Mammakarzinom. Geburtsh Frauenheilk 2003 (63):835-40
- ↑ Gonadotoxizität der Chemotherapie http://www.aerzteblatt.de/v4/archiv/artikel.asp?id=52799
- ↑ Vorzeitige Menopause schädigt Gehirn und Nerven
- ↑ von Minckwitz G; for The Breast Commission of the German Gynaecological Oncology Working Group (AGO). Evidence-based treatment of metastatic breast cancer – 2006 recommendations by the AGO Breast Commission. Eur J Cancer. 2006 Nov; 42: 2897-908, 2008. PMID: 17046240
- ↑ Tamoxifen: Hayes DF: Dr. Jekyll and Mr. Hyde? Journal of the National Cancer Institute 2004 (96):895-7
- ↑ Osborne CK, et al.: Role of the estrogen receptor coactivator AIB1 (SRC-3) and HER-2/neu in tamoxifen resistance in breast cancer. Journal of the National Cancer Institute 2003 (95):353-61
Literatur
- Heinrich Schmidt-Matthiesen, Gunther Bastert, Diethelm Wallwiener (Hrsg.): Gynäkologische Onkologie. 7. Auflage. Schattauer Verlag, Stuttgart 2002. ISBN 3-7945-1974-4.
- Orlando Silva, Stefano Zurrida (Hrsg.): Brustkrebs: Diagnostik und Therapie. Urban & Fischer, München 2007. ISBN 3-437-24260-1.
- Broschüre „Brustkrebs“ der Deutschen Krebsgesellschaft PDF
- Rainer Kürzl: Evidenzbasierte Missverständnisse beim Mammakarzinom. Erkrankungsrisiko und Mortalitätsreduktion. In: Deutsches Ärzteblatt, Köln 2004, 101(36), S. A2387-A2390. ISSN 0012-1207
Weblinks
- Links zum Thema Brust (Krebs) im Open Directory Project
- Wege zur Prävention von Brustkrebs Breast Cancer Action Germany
- S3-Leitlinie Brustkrebs-Früherkennung der Deutschen Gesellschaft für Senologie und der deutschen Krebshilfe e. V. bei AWMF online (Stand Februar 2008)
- S3-Leitlinie Diagnostik, Therapie und Nachsorge des Mammakarzinoms der Frau der Deutschen Gesellschaft für Gynäkologie und Geburtshilfe und der Deutsche Krebsgesellschaft e. V. bei AWMF online (Stand 2008)
- Übersicht nationale, europäische und internationale Brustkrebs-Leitlinien Breast Cancer Action Germany
- Brustkrebs - die blauen Ratgeber Nr. 2 der Deutschen Krebshilfe.
- Krebsinformationsdienst am DKFZ Heidelberg, Seite „Brustkrebs“
- Deutsche Gesellschaft für Senologie
- Brustkrebs beim Deutschen Grünen Kreuz e.V.
- Entscheidungshilfen: Brustkrebs - Was kommt danach? und Brusterhaltende Therapie oder Brustentfernung? der AOK - Die Gesundheitskasse
Wikimedia Foundation.
Schlagen Sie auch in anderen Wörterbüchern nach:
Benigner Tumor — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Bösartiger Tumor — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Hormonersatztherapie — (HET) (engl. hormone replacement therapy / HRT) bezeichnet die medizinische Verwendung von Hormonen zur Behandlung von Beschwerden, die auf einen relativen oder absoluten Mangel eines oder mehrerer Hormone zurückgeführt werden können. Im engeren… … Deutsch Wikipedia
Krebserkrankung — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Krebsherd — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Krebsmedizin — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Krebstherapie — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Krebsvorsorge — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Krebszelle — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia
Maligner Tumor — Krebs bezeichnet in der Medizin einen malignen (bösartigen) Tumor – eine bösartige Neoplasie. Im engeren Sinn sind die malignen epithelialen Tumoren (Karzinome) und die malignen mesenchymalen Tumoren (Sarkome) gemeint. Umgangssprachlich werden… … Deutsch Wikipedia


.jpg)