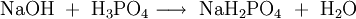- NaH2PO4
-
Strukturformel 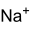
Allgemeines Name Natriumdihydrogenphosphat Andere Namen - Mononatriummonophosphat
- Saures Mononatriummonophosphat
- Mononatriummorthophosphat
- Natriumbiphosphat
- prim-Natriumphosphat
Summenformel NaH2PO4 CAS-Nummer - 7558-80-7 (Anhydrat)
- 10049-21-5 (Monohydrat)
- 13472-35-0 (Dihydrat)
PubChem 23672064 Kurzbeschreibung farb- und geruchloser kristalliner Feststoff[1][2][3] Eigenschaften Molare Masse 119,98 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Löslichkeit Sicherheitshinweise Gefahrstoffkennzeichnung [1][2][3] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze WGK 1[1][2][3] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Natriumdihydrogenphosphat ist ein farb- und geruchloses Salz aus den Ionen Na+ und H2PO4−.
Inhaltsverzeichnis
Gewinnung und Darstellung
Natriumdihydrogenphosphat wird, wie andere Phosphate auch, aus Erzen, wie beispielsweise Apatit gewonnen.
Im Labor kann die Darstellung durch die Neutralisation von Natronlauge mit Phosphorsäure erfolgen:
Das Dihydrat kann rein aus einer kalten Wasser/Ethanollösung kristallisiert werden.[4]
Eigenschaften
Neben der wasserfreien Verbindung treten noch das Monohydrat (NaH2PO4 · H2O) und das Dihydrat (NaH2PO4 · 2H2O) auf.
Nachfolgend sind die Eigenschaften der Hydrate aufgeführt, die von denen der wasserfreien Verbindung abweichen.
Chemische Eigenschaften
Natriumdihydrogenphosphat reagiert, in Wasser gelöst, sauer (pH 4,5 bei 12 g/l, 25 °C).
Verwendung
Natriumdihydrogenphosphat findet in der Molekularbiologie und Biochemie zur Herstellung von Pufferlösungen Anwendung. Man kann durch Mischen von Natriumdihydrogenphosphat- mit Dinatriumhydrogenphosphat-Lösung einen Puffer mit bestimmten pH-Wert herstellen oder man kann auch durch Zupipettieren von konzentrierter Natronlauge zu einem Phosphat-Puffer den pH-Wert einstellen. Weiterhin ist es Bestandteil von Medikamenten: als arzneilich wirksamer Bestandteil von Laxantien oder Hilfsstoff in solchen, die in wässriger Form verabreicht werden (z. B. Nasensprays).
Sicherheitshinweise
Natriumdihydrogenphosphat kann bei Augenkontakt leichte Reizungen hervorrufen. Es ist nicht brennbar, kann bei Erhitzen jedoch zur Freisetzung von Phosphoroxiden führen. Die LD50 für Ratten beträgt bei oraler Applikation 8290 mg/kg Körpergewicht. Die LD50 dermal bei Kaninchen beträgt >7940 mg/kg. Natriumdihydrogenphosphat ist schwach wassergefährdend: Wassergefährdungsklasse 1.
Quellen
Wikimedia Foundation.