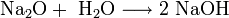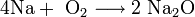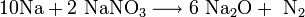- Natriummonoxid
-
Kristallstruktur 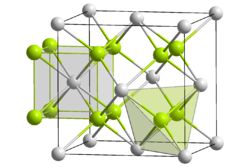
gelb: Na+, grau: O2- Allgemeines Name Natriumoxid Andere Namen - Natriummonoxid
- Dinatriumoxid
Verhältnisformel Na2O CAS-Nummer 1313-59-3 Kurzbeschreibung weißes Pulver[1] Eigenschaften Molare Masse 61,98 g·mol−1 Aggregatzustand fest
Dichte 2,27 g·cm−3[1]
Schmelzpunkt 1275 °C (Sublimation)[1]
Siedepunkt 1950 °C (Zersetzung)
Löslichkeit zersetzt sich in Wasser[1], unlöslich in anderen Lösungsmitteln
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Ätzend (C) R- und S-Sätze R: 14-34 S: 8-26-30-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Natriumoxid ist das Oxid des Natriums. Es besitzt die Summenformel Na2O.
Inhaltsverzeichnis
Vorkommen
Natriumoxid kommt in der Natur nicht frei, sondern nur in gebundener Form vor. In dieser Form ist es weit verbreitet, z.B. ist es gebunden in zahlreichen Mineralien enthalten.
Eigenschaften
Es handelt sich um einen farblosen Feststoff, der in einer Antifluoritstruktur kristallisiert. Natriumoxid reagiert heftig mit Wasser unter Bildung von Natriumhydroxid
Herstellung
Es kann direkt aus den Elementen gewonnen werden. Hierbei ist es jedoch erforderlich, die Stöchiometrie der Reaktion sowie die Temperatur zu beachten, da sonst auch Natriumperoxid und Natriumhyperoxid gebildet werden.[2]
Die Reaktion wird in einem Temperaturbereich von 150 − 200 °C durchgeführt. Höhere Temperaturen begünstigen die Bildung von Natriumperoxid.
Eine weiter Möglichkeit ist durch die Umsetzung von flüssigem Natrium mit Natriumnitrat gegeben.
Verwendung
Natriumoxid wird als Ätzmittel, bei der Glasherstellung und zur Polymerisation verwendet.
Quellen
Wikimedia Foundation.