- Neutrophiler Granulocyt
-
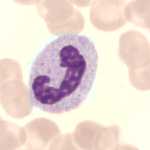
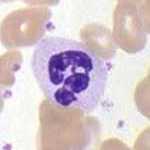
Die neutrophilen Granulozyten, auch kurz Neutrophile genannt, gehören mit einem Anteil von 50% - 65% zu den häufigsten weißen Blutkörperchen (Leukozyten). Als Phagocyten sind sie Teil der angeborenen Immunabwehr und dienen der Identifizierung und Zerstörung von Mikroorganismen.
Inhaltsverzeichnis
Struktur
Neutrophile sind kugelförmige Zellen mit einem Durchmesser von 12 bis 15 µm (Mikrometer). Charakteristisch für ausgereifte Neutrophile ist der aus drei bis fünf Segmenten bestehende Kern. Das Cytoplasma von Neutrophilen enthält zwei Arten von Granula: Die Häufigsten sind „spezifische“ Granula, die Enzyme wie Lysozym, Kollagenase, Elastase, Plasminogenaktivatoren, Neuramidase und Cathepsin G enthalten. Diese Granula lassen sich nicht mit basischen und sauren Farbstoffen färben, was sie ebenfalls in namensgebender Weise von Basophilen und Eosinophilen unterscheidet. Das Lysosom entspricht den sogenannten „azurophilen“ Granula und enthält neben den typischen Bestandteilen wie saure Hydrolasen und antimikrobielle Enzyme und Substanzen wie Defensine, Myeloperoxidase, Cathelicidine und Laktoferrin.
Reifung
Ein erwachsener Mensch produziert mehr als 1011 Neutrophile pro Tag. Sie werden im Knochenmark gebildet. Junge Neutrophile haben im Gegensatz zu Ausgereiften noch keinen vielfach segmentierten Kern, weshalb sie als „stabkernig“ beschrieben werden. Sollten Neutrophile nicht innerhalb von 6 Stunden nach Neubildung in Kontakt mit Infektionen und/oder Entzündungsreaktionen kommen, erfahren sie den programmierten Zelltod (Apoptose) und werden durch Makrophagen in Leber oder Milz abgebaut. Selbst bei Kontakt mit Infektionen haben Neutrophile nur eine um wenige Stunden verlängerte Lebensdauer.
Funktion
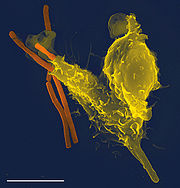 Eine REM-Aufnahme eines neutrophilen Granulozyten (gelb) beim Aufnehmen eines Anthrax-Bakteriums (orange); der weiße Strich unten links entspricht 5µm.
Eine REM-Aufnahme eines neutrophilen Granulozyten (gelb) beim Aufnehmen eines Anthrax-Bakteriums (orange); der weiße Strich unten links entspricht 5µm.Neutrophile zirkulieren im Blut und wandern im Falle einer Infektion zum Ort des Geschehens. Dies gilt in gleichem Maße für Monozyten. Dort nehmen sie die infektionsauslösenden Mikroben auf und verdauen sie. Um infiziertes und/oder entzündetes Gewebe zu erreichen, verlassen beide in einem durch Adhäsionsmoleküle und Chemokine (lösliche „Lockstoffe“) vermittelten mehrstufigen Prozess den Blutstrom und dessen Gefäße. Dabei wandern sie durch die Interzellular-Räume der endothelialen Zellen in postkapillaren Venolen. Der Vorgang der Rekrutierung von Neutrophilen und Monozyten zum Infektionsherd lässt sich in vier Schritte unterteilen:
- Selectin-vermitteltes „Entlang“-Rollen am Gefäß-Endothelium:
Makrophagen, die vor Ort Mikroben verdaut haben, schütten Cytokine wie Interleukin-1 (IL-1) und Tumornekrosefaktor (TNF) aus. Diese induzieren bei in der Nähe liegenden Epithelzellen die Zunahme von Selectinen (P-Selectin und E-Selectin) auf der Oberfläche. Neutrophile und Monozyten besitzen auf ihrer Oberfläche das L-Selectin als Adhäsionsmolekül und die für P- und E-Selectin spezifischen Kohlenhydrat-Liganden. Die entstehenden Selectin-Selectin-Interaktionen sind sehr schwach und werden durch die Scherkräfte des Blutstroms unterbrochen. Das führt zu einem langsameren „Entlang“-Rollen von Neutrophilen und Monozyten auf dem Endothelium, indem sie sich permanent an die Oberfläche binden und wieder lösen.
- 'Chemokin-vermittelte Verstärkung der Integrin-Affinität:
Ausgeschüttete Cytokine wie IL-1 und TNF induzieren in Makrophagen, endothelialen und anderen Zell-Typen die Produktion von Chemokinen. Sie werden an der Oberfläche des Epithel-Lumen gebunden und dadurch konzentriert. „Vorbei“-rollende Neutrophile und Makrophagen erkennen diese mit spezifischen Chemokin-Rezeptoren. Dies führt dazu, dass Integrine auf deren Oberfläche von einer geringen Affinität zu einer hohen Affinität wechseln. Zusätzlich lagern sich diese Integrine zusammen und führen zu einer stärkeren Bindung an die Endothel-Oberfläche und ein verlangsamtes „Rollen“.
- Stabile Integrin-vermittelte Adhäsion an das Endothelium:
Parallel zur Integrin-Affinitätsänderung auf Neutrophilen und Monozyten werden auf deren Zelloberfläche Liganden wie VCAM-1 (engl. vascular cell adhesion molecule-1) und ICAM-1 (engl. intercellular adhesion molecule-1) exprimiert, die an Integrine des Endothels binden. Auch diese Liganden-Produktion wird durch Chemokine induziert. Zusammen mit den in 2. beschriebenen Effekten führt dies zu einer festen Bindung an das Endothelium. Hierdurch finden Umlagerungen des Cytoskeletts statt und die Leukozyten positionieren sich abgeflacht auf dem Endothelium.
- Durchwanderung des endothelialen Gewebes:
Neutrophile und Monozyten folgen nun den Konzentrationsgradienten der lokalen Chemokine und wandern zwischen den endothelialen Zellen zum infizierten Gewebe. Für diesen Vorgang werden Teile der extrazellulären Matrix (EZM) der Endothelzellen aufgelöst, um genügend Freiraum für die durchwandernden Leukozyten zu bieten. Diese schütten hierfür ihre spezifischen Granula aus, deren Proteasen die Auflösung ermöglichen.
Durch diese Prozesse akkumulieren Neutrophile und Monozyten am Infektionsort, wodurch die Hauptkomponente einer Entzündung gegeben ist. Durch zeitliche Unterschiede der induzierten Chemokin-Rezeptor- und Integrin-Expression werden innerhalb von Stunden bis Tagen zuerst Neutrophile zum Infektionsort rekrutiert, innerhalb von Tagen bis Wochen erst Monozyten. Bei einer Infektion steigt im Blut die Konzentration von Neutrophilen an (Neutrophilie), was durch eine Zunahme von „Stabkernigen“ (ein Merkmal junger Neutrophiler) eine gesteigerte Neubildung beweist. Am Infektionsort angekommen, werden Mikroben durch Neutrophile und Makrophagen aufgenommen und zerstört, ein Prozess, der Phagozytose genannt wird.
Neutrophile Granulozyten haben zudem die Fähigkeit, Bakterien mittels einer freigesetzten fibrillären Matrix aus Granula-Proteinen und Chromatin zu binden. Dies verhindert einerseits die weitere Verbreitung von Bakterien und fördert andererseits das Zerstören der dort festgesetzten Bakterien. [1] Diese Netze werden engl. „Neutrophil Extracellular Traps“ (NETs) bezeichnet.
Primäre Erkrankungen
Die septische Granulomatose führt trotz einer funktionsfähigen Wanderung zum Infektionsort und der Aufnahme von Mikroben bei Neutrophilen zu einem Defekt im Abbau, dem „Verdau“. Somit stehen Neutrophile als Teil der Immunantwort nicht mehr zur Verfügung, wodurch Infektionen einen kritischen Verlauf nehmen können.
Einzelnachweise
- ↑ Brinkmann V, Reichard U, Goosmann C, Fauler B, Uhlemann Y, Weiss DS, Weinrauch Y, Zychlinsky A.: Neutrophil extracellular traps kill bacteria. Science. 2004 Mar 5;303(5663):1532-5. PMID 15001782
Literatur
Abul K. Abbas, Andrew H. Lichtman, Shiv Pillai: Cellular and Molecular Immunology, 6th Edition, Saunders Elsevier 2007
Weblinks
- Selectin-vermitteltes „Entlang“-Rollen am Gefäß-Endothelium:
Wikimedia Foundation.