- Nierenfunktion
-
Die Glomeruläre Filtrationsrate (GFR) gibt das Gesamtvolumen des Primärharns an, das von allen Glomeruli beider Nieren zusammen, in einer definierten Zeiteinheit, gefiltert wird. Dies sind bei einem Menschen mit normalen Blutdruckwerten ca. 0,12 Liter pro Minute bzw. ca.170 Liter pro Tag. Die GFR sinkt physiologisch mit zunehmendem Alter oder pathologisch bei Nierenerkrankungen verschiedenster Art.
Die GFR ist für die Abschätzung der Nierenfunktion die wichtigste Größe. Die GFR wird im klinischen Alltag durch die Ermittlung der Kreatininclearance näherungsweise ermittelt (siehe auch renale Clearance).
Clearance
Clearance bezeichnet das Plasmavolumen, das pro Zeiteinheit von einer bestimmten Substanz befreit wird. Um die GFR ermitteln zu können, wird die Clearance einer Markersubstanz betrachtet, die im Tubulussystem der Niere weder sezerniert noch rückresorbiert wird.
Exogene Marker
Exogene Markersubstanzen werden durch Injektion und Infusion zugeführt.
Goldstandard der Indikatorsubstanzen ist Inulin. Inulin ist ein physiologisch inertes Polysaccharid, das im Glomerulus frei filtriert, und durch die Niere weder sezerniert, rückresorbiert, synthetisiert oder metabolisiert wird. Inulin ist schwer zu messen, die Bestimmung der Inulin-Clearance erfordert zudem eine kontinuierliche Infusion und zwei zusätzliche Blutentnahmen. Daher wird die Bestimmung der Inulin-Clearance in der Regel nur noch im Rahmen wissenschaftlicher Untersuchungen durchgeführt.[1][2]
Alternativ werden heute die Röntgenkontrastmittel Iothalamat und Iohexol, sowie radioaktiv markierte Substanzen wie 99mTc-DTPA und 51Cr-EDTA als exogene Markersubstanzen eingesetzt.
Endogene Marker
Für die klinische und ambulante Routinediagnostik sind exogene Marker in der Regel zu aufwändig. Die glomeruläre Filtrationsrate wird daher im klinischen Alltag anhand der endogenen Marker Kreatinin und Cystatin C bestimmt.[2]
Kreatinin
Kreatinin entsteht im Muskelgewebe durch Abbau von Kreatin. Im Plasma ist Kreatinin in relativ konstanter Konzentration vorhanden. Kreatinin wird frei im Glomerulus filtriert, und durch die Niere weder rückresorbiert noch metabolisiert. 10-40% des im Urin ausgeschiedenen Kreatinin stammen allerdings nicht aus der glomerulären Filtration, sondern werden durch die Nierentubuli in den Primärharn sezerniert. Das Serum-Kreatinin steigt mit zunehmender Nierenfunktionseinschränkung an. In den frühen Stadien einer Nierenerkrankung ist das Serum-Kreatinin aber ein ungenauer Marker von geringer Sensitivität, insbesondere bei Menschen mit geringerer Muskelmasse, wie Frauen, älteren Menschen oder Diabetikern. Wird ausschließlich das Serum-Kreatinin als Marker einer Nierenfunktionseinschränkung benutzt, kann die Diagnose einer Niereninsuffizienz übersehen werden. Dies kann zu unterlassener Behandlung, falscher Einschätzung des Herz-Kreislauf-Risikos und Fehlern bei der Dosierung von Medikamenten führen. Aus diesem Grund sind genauere Methoden zur Bestimmung der Nierenfunktion unerlässlich.
Kreatinin-Clearance
Zur Ermittlung der Kreatinin-Clearance bedarf es des Sammelns des Urins über einen definierten Zeitraum (im klinischen Alltag: t = 24 Stunden). Es wird das Volumen (V) des Sammelurins bestimmt, sowie die Kreatininkonzentration. Des Weiteren wird die Plasmakonzentration des Kreatinins aus einer Blutprobe des Patienten bestimmt. Die Plasmakonzentration des Kreatinins ist gleich der Konzentration im glomerulären Filtrat (Primärharn) cKrea,Plasma = cKrea,glom.Filtrat .
Das Prinzip der Berechnung ist die Überlegung, dass die im Glomerulum abfiltrierte Menge Kreatinins in einer gewissen Zeit (t), gleich der Menge Kreatinins ist, die in eben dieser Zeitspanne im Endharn ausgeschieden wird. Das ist nur der Fall, wenn die Indikatorsubstanz, wie oben erwähnt, nicht tubulär sezerniert oder resorbiert wird:
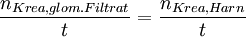
Da sich die Menge (n) nicht direkt bestimmen, aber durch die o.g. im klinischen Setting ermittelbaren Werte berechnen lässt (n = c * V), verändert sich die Formel folgendermaßen:
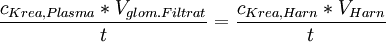
Diese Formel lässt sich einfach umstellen und so die Glomeruläre Filtrationsrate berechnen.
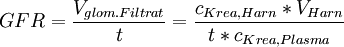
Zur genaueren Berechnung wird manchmal noch die Körperoberfläche als korrigierender Faktor mit einbezogen.
Der Zusammenhang zwischen Serum-Kreatinin-Konzentration und glomerulärer Filtrationsrate ist nicht proportional, sondern antiproportional. Bei einer hohen glomerulären Filtrationsrate entsprechen daher kleine Änderungen des Serum-Kreatinins großen Änderungen der glomerulären Filtrationsrate, bei einer niedrigen glomerulären Filtrationsrate entsprechen dagegen große Änderungen des Serum-Kreatinins nur kleinen Änderungen der glomerulären Filtationsrate. So entspricht bei einer 60-jährigen Frau ein Anstieg des Serum-Kreatinins von 0,8 auf 0,9 mg/dl einem Abfall der glomerulären Filtrationsrate um 10 ml/min von 78 auf 68 ml/min, ein gleich großer Abfall der glomerulären Filtrationsrate von 20 auf 10 ml/min geht dagegen mit einem Anstieg des Serum-Kreatinins von 2,6 auf 4,8 mg/dl einher.
Einschränkungen der Kreatinin-Clearance
- Fehler beim Sammeln des Urins: Die Bestimmung der Kreatinin-Clearance setzt ein exaktes Sammeln des Urins über 24 Stunden voraus. Zu Beginn der Sammelperiode muss die Harnblase vollständig entleert werden. Während der Sammelperiode muss der Urin vollständig gesammelt werden. Am Ende der Sammelperiode nach exakt 24 Stunden muss die Blase vollständig in das Urin-Sammelgefäß entleert werden. In der Praxis kommt es häufig zu Fehlern beim Sammeln des Urins.
- Tubuläre Kreatinin-Sekretion: Bei normaler oder gering eingeschränkter Nierenfunktion ist der Anteil des tubulär sezernierten Kreatinins gegenüber der glomerulär filtrierten Menge gering und kann vernachlässigt werden. Bei schwerer Nierenfunktionseinschränkung kann der tubulär sezernierte Anteil über 50% der ausgeschiedenen Kreatinin-Menge betragen, die glomeruläre Filtrationsrate wird dadurch unter Umständen erheblich überschätzt. Liegt die glomeruläre Filtrationsrate unter 30 ml/min, sollte daher zusätzlich die Harnstoff-Clearance bestimmt werden. Harnstoff wird im Gegensatz zu Kreatinin tubulär rückresorbiert, die Harnstoff-Clearance unterschätzt daher die glomeruläre Filtrationsrate. Bildet man den Mittelwert zwischen Kreatinin- und Harnstoff-Clearance, heben sich die Fehler beider Messungen in Näherung auf.
Näherungsformeln, die auf der Bestimmung des Serum-Kreatinin beruhen
In der Praxis ist das Sammeln des Urins aufwändig und mit Fehlern behaftet. Zudem hängt die Konzentration des Kreatinin im Serum nicht nur ab von der Nierenfunktion, sondern auch von der Muskelmasse, und diese wiederum ist abhängig von Alter, Geschlecht und Hautfarbe. So entspricht ein Serum-Kreatinin von 1,3 mg/dl bei einem 20-jährigen Mann einer glomerulären Filtrationsrate von 75 ml/min, bei einer 80-jährigen Frau dagegen einer glomerulären Filtrationsrate von 50 ml/min. Um dennoch auf das Sammeln des Urins verzichten zu können, wurden Näherungsformeln entwickelt, die es erlauben, die glomeruläre Filtrationsrate aus dem Serumkreatinin zu bestimmen.[1]
Cockcroft-Gault-Formel
Die Cockcroft-Gault-Formel wurde 1973 entwickelt. Zu Grunde lagen die Daten von 249 Männern mit einer Kreatinin-Clearance zwischen 30 und 130 ml/min.
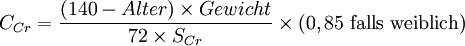
- CCr: Kreatinin-Clearance
- SCr: Serum-Kreatinin in mg/dl
- Alter: Alter in Jahren
- Gewicht: Körpergewicht in kg.
Das Ergebnis ist nicht auf die Körperoberfläche bezogen. Die Cockcroft-Gault-Formel überschätzt die glomeruläre Filtrationsrate, da sie die tubuläre Sekretion nicht berücksichtigt.
MDRD-Formel (Modifikation of Diet in Renal Disease)
Die MDRD-Formel wurde 1999 anhand der Daten von 1628 ambulanten Patienten mit chronischer Nierenkrankheit entwickelt. Die Einbeziehung der Hautfarbe berücksichtigt die erhöhte Muskelmasse von Amerikanern schwarzafrikanischer Herkunft. Es gibt mehrere Varianten der MDRD-Formel, als Standard hat sich die Vier-Variablen-MDRD-Formel durchgesetzt, in die Alter, Geschlecht, Hautfarbe und Serum-Kreatinin (sCr) eingehen (Angabe in exponentieller und in logarithmischer Schreibweise):
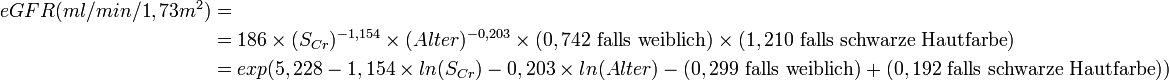
- eGFR: estimated Glomerular Filtration Rate, geschätzte glomeruläre Filtrations-Rate
- SCr: Serum-Kreatinin in mg/dl
- Alter: Alter in Jahren
Die MDRD-Formel benötigt keine Angabe des Körpergewichts, da sie die glomeruläre Filtrationsrate für eine standardisierte Körperoberfläche von 1,73 m2 angibt und ist bei Menschen mit moderater bis schwerer chronischer Nierenfunktionseinschränkung genauer als Cockcroft-Gault-Formel und Kreatinin-Clearance. Der Wert der MDRD-Formel bei Nierengesunden ist nicht geklärt, eine Anwendung bei hospitalisierten Patienten wird nicht empfohlen.[3]
Einschränkungen der Näherungsformeln
Die Näherungsformeln sind validiert für ambulante, chronisch nierenkranke Patienten mit moderater bis schwerer Nierenfunktionseinschränkung (Stadium 3 und 4). Die Formeln sind nicht geeignet zur Bestimmung der glomerulären Filtrationsrate bei Personen mit normaler Nierenfunktion oder leichter Nierenfunktionseinschränkung. Insbesondere die MDRD-Formel unterschätzt bei Menschen mit einer glomerulären Filtrationsrate über 60 ml/min diese um ca. 10 ml/min.[4] Ebenso wenig geeignet sind die Näherungsformeln zur Bestimmung der glomerulären Filtrationsrate bei Krankenhauspatienten mit akuter Nierenfunktionsverschlechterung, bei Menschen mit schwerem Übergewicht, bei stark verminderter Muskelmasse (Amputation von Gliedmaßen, Unterernährung) oder bei Menschen mit besonders hoher (Nahrungsergänzungen bei Bodybuildern) oder niedriger (Vegetarier) Kreatin-Zufuhr mit der Nahrung. Als Mittel zum bevölkerungsweiten Screening und zur Überwachung der Nierenfunktion im besonders wichtigen Frühstadium der diabetischen Nephropathie sind die Näherungsformeln ebenfalls nicht geeignet[5].
Cystatin C
Cystatin C ist ein kleines, nicht glykosyliertes Protein (13 kDa, 122 Aminosäuren) aus der Familie der Cystein Proteinase Inhibitoren. Cystatin C wird in einer konstanten Rate von allen kernhaltigen Körperzellen produziert. Aufgrund seiner geringen Größe und eines basischen isoelektrischen Punktes (pI~9.0) wird Cystatin C im Glomerulum frei filtriert. Im Nierentubulus wird Cystatin C nicht sezerniert. Es wird zu über 99% durch die Tubulusepithelzellen rückresorbiert, gelangt aber nicht in den Blutkreislauf zurück, da es von den Tubuluszellen abgebaut wird. Die Konzentration von Cystatin C im Urin ist deshalb sehr gering, eine Berechnung der Cystatin C - Clearance über Sammelurin nicht möglich, aber auch nicht erforderlich. Da Cystatin C konstant gebildet wird und in der Niere frei filtriert, nicht tubulär sezerniert wird und nach Filtration nicht in die Blutzirkulation zurückkehrt, ist es ein besserer Filtrationsmarker als Kreatinin oder Harnstoff, insbesondere bei leichter Nierenfunktionseinschränkung, vermehrter Muskelmasse[6] oder akutem Nierenversagen. [7] [8]
Praktische Anwendungen
Klassifizierung der Nierenfunktion
Die Nierenfunktionsleistung wird gemäß der Empfehlung der Kidney Disease Outcome Quality Initiative (KDOQI) in folgende Stufen eingeteilt:
Grad / Clearance ml / min Stadium der Nierenschädigung
- Stufe I : > 90 bedeutet normaler oder erhöhter GFR
- Stufe II : 60-89 bedeutet geringgradiger Funktionsverlust
- Stufe III: 30-59 bedeutet mittelgradiger Funktionsverlust
- Stufe IV : 15-29 bedeutet schwerer Funktionsverlust
- Stufe V : < 15 bedeutet Nierenversagen
Diagnose chronischer Nierenkrankheiten
Eine chronische Nierenkrankheit liegt vor, wenn über drei Monate die glomeruläre Filtrationsrate unter 60 ml/min liegt oder über einen ebensolchen Zeitraum Eiweiß im Urin nachweisbar ist. Da die Näherungsformeln bei einer Reduktion der glomerulären Filtrationsrate unter 60 ml/min hinreichend genaue Werte liefern und die Eiweißausscheidung anhand des Eiweiß/Kreatinin-Quotienten im Spontanurin quantifiziert werden kann, ist zur Diagnose einer chronischen Nierenkrankheit das Sammeln des Urins über 24 Stunden nicht mehr zwingend nötig[9].
Quantifizierung der Progression chronischer Nierenkrankheiten
Wegen der antiproportionalen Korrelation zwischen Serum-Kreatinin und glomerulärer Filtrationsrate lässt sich die Rate des Nierenfunktionsverlustes in einer bestimmten Zeiteinheit nur ungenau aus der Änderung des Serum-Kreatinins abschätzen. Bei einem 50-jährigen entspricht ein Anstieg des Serum-Kreatinins von 1,0 auf 2,0 mg/dl einem Abfall der glomerulären Filtrationsrate um 46 ml/min, ein weiterer Anstieg des Serum-Kreatinins von 2,0 auf 3,0 mg/dl entspricht dagegen nur noch einem Abfall der glomerulären Filtrationsrate um 14 ml/min.
Komplikationen chronischer Nierenkrankheiten
Bei einem Abfall der glomerulären Filtrationsrate unter 60 ml/min treten mannigfaltige Komplikationen auf, insbesondere Bluthochdruck, Malnutrition, Blutarmut und Knochenerkrankungen. Da diese Komplikationen frühzeitig behandelt werden müssen, sind bei einem Abfall der glomerulären Filtrationsrate unter 60 ml/min zusätzliche diagnostische und therapeutische Maßnahmen erforderlich. Bei einem weiteren Absinken der glomerulären Filtrationsrate unter 30 ml/min sollte ein Nierenspezialist hinzugezogen werden, da bei einer glomerulären Filtrationsrate unter 15 ml/min ein Nierenersatzverfahren wie Dialyse oder Nierentransplantation erforderlich wird.
Dosierung von Medikamenten
Viele Medikamente (in Deutschland im Mittel jeder 6. Wirkstoff) werden durch die Nieren ausgeschieden. Bei eingeschränkter Nierenfunktion ist daher oftmals eine Anpassung der Dosis erforderlich. Insbesondere die seit 1973 gebräuchliche Cockcroft-Gault-Formel wird in großem Umfang bei der Berechnung von Medikamentendosierungen in Abhängigkeit von der Nierenfunktion eingesetzt (siehe auch Dosisanpassung bei Niereninsuffizienz). Als weiterführende Informationsquelle ist hier die Webseite Dosing.de des Universitätsklinikums Heidelberg zu empfehlen.
Glomeruläre Filtrationsrate als Risikofaktor
Mit zunehmendem Abfall der glomerulären Filtrationsrate steigt die Häufigkeit kardiovaskulärer Erkrankungen wie Schlaganfall und Herzinfarkt. Eine verminderte glomeruläre Filtrationsrate ist damit ein kardiovaskulärer Risikofaktor. Eine besonders hohe Korrelation besteht zwischen kardiovaskulärem Risiko und Cystatin C – Spiegel.
Messung der Clearance versus Näherungsformeln
Wegen der Einschränkungen der Näherungsformeln ist eine Bestimmung der glomerulären Filtrationsrate mittels 24 h – Sammelurin erforderlich
- bei Personen mit besonders niedrigem oder hohem Körpergewicht,
- bei besonders fleischarmer oder fleischreicher Ernährung,
- bei Personen mit Amputation von Gliedmaßen,
- bei rascher Änderung der Nierenfunktion,
- bei Diabetikern in frühen Stadien der Nierenbeteiligung,
- wenn bei normaler oder milde eingeschränkter Nierenfunktion eine genaue Kenntnis der glomerulären Filtrationsrate erforderlich ist, z. B. wenn eine Nierespende oder die Behandlung mit nierenschädlichen Medikamenten geplant ist.
Die Bestimmung der Nierenfunktion mittels exogener Markersubstanzen ist in der Regel nur noch im Rahmen von Forschungsvorhaben erforderlich.
Quellenangaben
- ↑ a b K/DOQI: „Clinical Practice Guidelines for Chronic Kidney Disease: Evaluation, Classification, and Stratification.“ American Jounal of Kidney Diseases 2002; 39 (2, Sup) Artikel
- ↑ a b L. A. Stevens et al.: „Assessing Kidney Function -- Measured and Estimated Glomerular Filtration Rate.“ N Engl J Med 2006; 354: S. 2473-2483 Abstract
- ↑ Myers GL et al.: „Recommendations for Improving Serum Creatinine Measurement: A Report from the Laboratory Working Group of the National Kidney Disease Education Program.“ Clin Chem 2006; 52: S. 5-18 Abstract Artikel
- ↑ Stevens, Lesley A. et al.: „Evaluation of the Modification of Diet in Renal Disease Study Equation in a Large Diverse Population.“ J Am Soc Nephrol 2007; 18: S. 2749-2757 Abstract
- ↑ Nephrology beyond JASN. Eberhard Ritz Feature Editor: Estimated GFR: Are There Limits to Its Utility? J Am Soc Nephrol 2006 17: 2077-2085 Zweiter Artikel des Features!
- ↑ Alessandra Calábria Baxmann et al.: „Influence of Muscle Mass and Physical Activity on Serum and Urinary Creatinine and Serum Cystatin C.“ Clin J Am Soc Nephrol 2008; 3: S. 348-354 Abstract
- ↑ Mussap M, Plebani M: „Biochemistry and clinical role of human cystatin C.“ Crit Rev Clin Lab Sci 2004; 41(5-6): S. 467-550 Abstract
- ↑ Laterza O. F. et al.: „Cystatin C: An Improved Estimator of Glomerular Filtration Rate?.“ Clinical Chemistry 2002; 48: S. 699-707 Abstract Artikel
- ↑ Joseph A. Vassalotti et al.: „Testing for Chronic Kidney Disease: A Position Statement From the National Kidney Foundation.“ American Journal of Kidney Diseases 2007; 50: S. 169-180 Artikel
Siehe auch
Weblinks
- www.Dosing.de Liste nierenrelevanter Arzneimittel (Dosierungshinweisen (Dettli-Formel, GFR-Berechnung, Dosisanpassung bei Niereninsuffizienz) des Universitätsklinikums Heidelberg
- Kreatinin-Clearance-Rechner Bestimmung der Nierenfunktion anhand der MDRD- und der Cockcroft-Gault-Formel incl. Kalkulator zum Download (industriegesponsorte Seite)
- Nierenrechner, der verschiedene Formeln berücksichtigt , eGFR-Kalkulator mit automatischer Formelauswahl GFR-Kalkulator nach MDRD/Cockcroft-Gault/Mayo
- GFR Kalkulator Cockcroft-Gault Online GFR Kalkulator nach Cockcroft-Gault-Formel
- GFR Kalkulator Jeliffe Online GFR Kalkulator nach Jeliffe-Formel
- GFR Kalkulator Chatelut Online GFR Kalkulator nach Chatelut-Formel
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.
