- Chronisches Nierenversagen
-
Klassifikation nach ICD-10 N18 Chronische Niereninsuffizienz N18.5 Terminale Niereninsuffizienz N18.8- Sonstige chronische Niereninsuffizienz N18.9 Chronische Niereninsuffizienz, nicht näher bezeichnet ICD-10 online (WHO-Version 2011) Beim chronischen Nierenversagen (chronischer Niereninsuffizienz, chronischer Nierenkrankheit) handelt es sich um einen langsamen, über Monate oder Jahre voranschreitenden Verlust der Nierenfunktion. Im engeren Sinn der aktuellen Leitlinien bezeichnet der Begriff chronisches Nierenversagen das Terminal- oder Endstadium einer chronischen Nierenkrankheit, das gekennzeichnet ist durch eine Nierenleistung von 15 % der Norm oder darunter (entsprechend einer glomerulären Filtrationsrate von unter 15 ml/min/1,73 m²) und die Notwendigkeit einer Nierenersatztherapie in Form von Dialysebehandlung oder Nierentransplantation. Dieser Artikel behandelt die chronische Nierenkrankheit in allen Stadien inklusive des Terminalstadiums.
Schlüssel-Fakten zur chronischen Nierenkrankheit
- Das Maß für die Nierenfunktion ist die glomeruläre Filtrationsrate. Eine chronische Nierenkrankheit liegt vor, wenn die glomeruläre Filtrationsrate unter einen bestimmten Wert (60 ml/min/1,73 m²) abgesunken ist, oder wenn im Urin Eiweiß ausgeschieden wird. Diese Funktionsstörungen müssen seit mindestens drei Monaten bestehen.
- Weltweit leiden mehr als 500 Mio. Menschen an chronischer Nierenkrankheit, dies entspricht einem von zehn Erwachsenen.
- Weltweit die häufigsten Ursachen sind Entzündungen und Infektionen der Nieren, Verengungen der ableitenden Harnwege und angeborene Nierenkrankheiten. In den Industrienationen sind Diabetes mellitus Typ 2 und Bluthochdruck aufgrund von Bewegungsmangel und Fehlernährung die häufigsten Ursachen. In den Entwicklungsländern steigt die Häufigkeit von Nierenkrankheiten aufgrund Diabetes und Bluthochdruck stark an.
- Eine chronische Nierenkrankheit wird durch eine einfache Blut- und Urinuntersuchung festgestellt. Im Blut wird die Konzentration der Markersubstanz Kreatinin bestimmt, daraus wird die Nierenfunktion berechnet. Im Urin wird die Eiweißkonzentration gemessen.
- Konsequenzen einer nicht erkannten Nierenerkrankung sind der fortschreitende Verlust der Nierenfunktion, möglicherweise bis zur Notwendigkeit von Dialyse und Transplantation, sowie Herz-Kreislauf-Komplikationen. Chronisch Nierenkranke haben ein mindestens 10-fach erhöhtes Risiko, vorzeitig an einer Herz-Kreislauf-Erkrankung (Koronare Herzkrankheit, Herzversagen, Durchblutungsstörungen des Gehirns und der Arterien) zu versterben.
- Die Kosten, die durch chronische Nierenkrankheiten verursacht werden, steigen. Weltweit sind 1,5 Mio. Menschen von der Dialyse abhängig oder leben mit einer Spenderniere. Diese Anzahl wird sich in den nächsten 10 Jahren voraussichtlich verdoppeln. Die Kosten für Dialyse und Nierentransplantation könnten in dieser Zeit eine Billion US$ überschreiten[1]. Dies könnte in den Industrienationen die Gesundheitsbudgets überfordern. Staaten mit geringerem Einkommen werden diese Kosten nicht tragen können.
Mehr als 80 % der Menschen, die eine Nierenersatztherapie erhalten, leben in Industrienationen. In Entwicklungsländern ist diese Behandlung weitgehend unerschwinglich. In Ländern wie Indien und Pakistan erhalten weniger als 10 % derer, die eine Behandlung benötigen, eine Nierenersatztherapie. In vielen afrikanischen Staaten wird eine Nierenersatztherapie in der Regel nicht angeboten, was bedeutet, dass viele Menschen einfach sterben. Für Entwicklungsländer wiegt die ökonomische Belastung besonders schwer, weil chronische Nierenkrankheiten dort in einem früheren Lebensalter auftreten.
- Im Frühstadium wird eine chronische Nierenkrankheit meist nicht erkannt, insbesondere in Entwicklungsländern. Durch Früherkennung wird jedoch eine Behandlung noch vor dem Auftreten von Komplikationen ermöglicht.
- Menschen mit erhöhtem Risiko sollten an Früherkennungsmaßnahmen teilnehmen, insbesondere
- Patienten mit Diabetes oder Bluthochdruck,
- Menschen mit Übergewicht,
- Raucher,
- Über-50-Jährige,
- bei familiärer Vorbelastung mit Diabetes, Bluthochdruck oder Nierenkrankheiten.
- Eine Behandlung sollte bereits im Frühstadium begonnen werden. Empfohlen werden
- Kontrolle des Körpergewichts,
- regelmäßige körperliche Betätigung,
- Raucherentwöhnung,
- medikamentöse Senkung des Blutdrucks, bei eingeschränkter Nierenfunktion oder Eiweiß im Urin sind ACE-Hemmer und AT1-Antagonisten Mittel der ersten Wahl;
- Korrektur von erhöhtem Blutzucker, erhöhten Blutfetten und Blutarmut.
- Eine frühzeitige Behandlung kann den Verlust der Nierenfunktion verlangsamen und das Auftreten von Herz-Kreislauf-Komplikationen hinauszögern.
Quelle: Statement zum Welt-Nieren-Tag 2007, Internationale Gesellschaft für Nephrologie, Internationaler Dachverband der Nierenstiftungen[2].
Aufgaben der Niere
Neben der Entfernung von Stoffwechselgiften aus dem Körper hat eine gesunde Niere eine Reihe weiterer lebensnotwendiger Aufgaben.
- Regelung des Flüssigkeitshaushaltes durch Steuerung der Wasserausscheidung.
- Regelung des Elektrolythaushaltes durch Steuerung der Konzentration von Ionen wie Natrium, Kalium, Calcium und Phosphat in den Körperflüssigkeiten.
- Regelung des Säure-Basen-Haushaltes durch Steuerung der Säureausscheidung.
- Entfernung von Medikamenten und Giften aus dem Körper.
- Abgabe von Hormonen in das Blut, welche den
- Blutdruck (Renin),
- die Bildung roter Blutkörperchen (Erythropoetin) und den
- Knochenstoffwechsel (Vitamin D3) regulieren.
Bei Menschen mit chronischer Nierenkrankheit sind eine oder mehrere dieser Funktionen der Niere gestört.
Definition und Stadieneinteilung
Definition - Nierenschädigung ≥ 3 Monate, definiert durch strukturelle oder funktionelle Anomalien, mit oder ohne Einschränkung der glomerulären Filtrationsrate (GFR), die sich manifestiert in
- pathologischen Anomalien oder
- Markern einer Nierenschädigung, inklusive Anomalien in der Zusammensetzung des Blutes oder Urins, oder Anomalien in bildgebenden Verfahren
- GFR < 60 ml/min/1,73 m² für ≥ 3 Monate, mit oder ohne Nierenschädigung
2002 wurde von der amerikanischen Nierenstiftung (National Kidney Foundation) der Begriff chronische Nierenkrankheit in der Kidney Disease Outcomes Quality Initiative (KDOQI) neu definiert[3]. Diese Definition hat sich mittlerweile weltweit durchgesetzt.
Eine chronische Nierenkrankheit liegt nach dieser Definition vor,
- wenn im Urin Eiweiß (Proteinurie) oder Albumin (Mikroalbuminurie) nachweisbar ist
- oder wenn die Nierenfunktion (glomeruläre Filtrationsrate) unter 60 % der Norm abgefallen ist
- oder wenn bei bildgebenden Verfahren (Sonographie, Computertomographie) krankhafte Veränderungen an den Nieren festgestellt werden
- und wenn dieser Zustand länger als drei Monate anhält.
Eiweiß im Urin wird nachgewiesen
- mit Hilfe von Urinteststreifen,
- chemischen (Biuretreaktion) oder
- photometrischen Verfahren.
Zur Messung der Nierenfunktion wird die Kreatinin-Konzentration im Blut bestimmt. Aus der Kreatinin-Konzentration wird mit Formeln die glomeruläre Filtrationsrate abgeschätzt. Diese stellt das Maß für die Nierenfunktion dar.
Die gebräuchlichsten Formeln sind die verkürzte MDRD-Formel und die Cockcroft-Gault Formel. In die verkürzte MDRD-Formel gehen ein Kreatinin-Konzentration, Alter, Geschlecht und die ethnische Herkunft. Die Cockcroft-Gault-Formel benützt Kreatinin-Konzentration, Alter, Geschlecht und Körpergewicht.
Anhand Proteinurie und glomerulärer Filtrationsrate (GFR) wird die chronische Nierenkrankheit in fünf Schweregrade eingeteilt:
Stadium GFR ICD-10 Proteinurie nachweisbar keine Proteinurie nachweisbar 1* > 89 N18.1* Nierenkrankheit mit normaler Nierenfunktion* Normalbefund 2* 60-89 N18.2* Nierenkrankheit mit milder Nierenfunktionseinschränkung* milde Nierenfunktionseinschränkung, aber keine Nierenkrankheit** 3 30-59 N18.3 Nierenkrankheit mit moderater Nierenfunktionseinschränkung*** 4 15-29 N18.4 Nierenkrankheit mit schwerer Nierenfunktionseinschränkung*** 5 < 15 N18.5 Chronisches Nierenversagen*** *) Im Stadium 1 und 2 ist zur Diagnose einer Nierenkrankheit immer der Nachweis von Eiweiß im Urin oder ein krankhafter Befund in einem bildgebenden Verfahren erforderlich. **) Menschen mit einer milden Nierenfunktionseinschränkung (GFR 60-89 ml/min/1,73 m²), bei denen keine Proteinurie oder andere krankhafte Veränderungen an den Nieren festgestellt werden, sind nicht nierenkrank. ***) In den Stadien 3 bis 5 gründet sich die Diagnose ausschließlich auf eine glomeruläre Filtrationsrate unter 60 ml/min/1,73 m². Nicht bei allen Individuen mit eingeschränkter Nierenfunktion liegt eine Proteinurie vor. Eine erhöhte Eiweißausscheidung findet sich bei etwa 65 % der Diabetiker[4] und nur etwa 30 % der Nichtdiabetiker mit eingeschränkter Nierenfunktion.[5] Liegt eine Proteinurie vor, besteht ein erhöhtes Risiko, dass die Nierenfunktionseinschränkung fortschreitet oder es zu einem Herzinfarkt kommt, die Sterblichkeit ist erhöht.[6]
Kritik der Stadieneinteilung nach KDOQI
Die Stadieneinteilung der KDOQI bezieht erstmals die frühen Krankheitsstadien in die Definition der chronischen Nierenkrankheit mit ein, in denen zwar Hinweise auf eine Nierenschädigung bestehen (z.B. Nachweis von Eiweiß oder roten Blutkörperchen im Urin, auffällige Ultraschalluntersuchung), aber noch keine oder nur eine geringgradige Einschränkung der Nierenfunktion vorliegt.[7]
Diese weitreichende Definition wurde von mehreren Autoren kritisiert:[8][9]
- Viele ältere Menschen mit altersbedingter Verminderung der Nierenfunktion würden automatisch als nierenkrank klassifiziert.
- Das Stadium 3 sei zu weit gefasst und beinhalte sowohl milde, klinisch nicht relevante Nierenfunktionseinschränkung bei älteren Menschen als auch schwere Nierenschäden mit weitreichenden Konsequenzen bei jüngeren Patienten.
- Das Stadium 3 sei 10- bis 20-mal häufiger als das Stadium 4 oder 5. Dies zeige, dass es nur bei einem geringen Teil der Patienten im Stadium 3 zu einer Verschlechterung der Nierenfunktion komme.
- Die Näherungsformeln zur Berechnung der glomerulären Filtrationsrate unterschätzen bei einer GFR > 60 ml/min die tatsächliche Nierenfunktion. Die Stadien 1 und 2 seien daher nicht exakt zu diagnostizieren und sollten daher abgeschafft werden.
- Der Nachweis geringer Mengen von Albumin im Urin (Mikroalbuminurie) sei zwar ein kardiovaskulärer Risikofaktor, reiche aber nicht aus, eine chronische Nierenkrankheit zu diagnostizieren.
Befürworter der KDOQI-Klassifikation weisen darauf hin, dass dadurch erstmals die Möglichkeit gegeben ist, Nierenerkrankungen bereits im Frühstadium zu diagnostizieren und frühzeitig Maßnahmen einzuleiten, die geeignet sind, einem weiteren Verlust der Nierenfunktion vorzubeugen.[10]
In einem Positionspapier von 2009 hat die KDOQI die Klassifikation von 2002 bestätigt. [11] Im Oktober 2009 fand in London eine internationale Folge-Konferenz zu Definition, Klassifizierung und Prognose der chronischen Nierenerkrankung statt, auf der ein Konsens über eine neue Stadieneinteilung erreicht wurde. Folgende Veränderungen wurde vorgeschlagen:
- Falls bekannt, ist die Ursache der Nierenschädigung in die Klassifikation mit einzubeziehen.
- Das Ausmaß der Albumin-Ausscheidung sollte in die Stadien-Einteilung mit einbezogen werden (Albuminurie < 30 mg/g, 30-300 mg/g und > 300 mg/g).
- Das Stadium 3 sollte in zwei Stadien aufgeteilt werden (eGFR 30-44 und 45-59 ml/min/1,73 m²).
Folgende Definitionen sollten beibehalten werden:
- Vorliegen einer chronischen Nierenkrankheit bei einer GFR < 60 ml/min/1,73 m², unabhängig von Alter und Geschlecht.
- Vorliegen einer chronischen Nierenkrankheit bei einer Albuminurie > 30 mg/g (Albumin/Kreatinin-Quotient im Urin).
Die geplanten Änderungen sollen eine bessere prognostische Einordnung von Nierenkrankheiten ermöglichen. So haben Patienten mit moderater Nierenfunktionseinschränkung eine relativ gute Prognose, wenn die Eiweißausscheidung gering ist, wogegen die Prognose auch bei nur milder Nierenfunktionseinschränkung schlechter ist, wenn die Eiweißausscheidung hoch ist. Eine Ausnahme ist die Minimal-Change-Glomerulonephritis mit guter Prognose, deswegen die Einbeziehung der Grunderkrankung in die Klassifikation. Die Leitlinie zur Klassifikation und Stadieneinteilung der chronischen Nierenkrankheit wird derzeit überarbeitet, die Veröffentlichung der aktualisierten Leitlinie ist für 2012 geplant.[12]
Ursachen von chronischem Nierenversagen
Häufigste Ursachen eines chronischen Nierenversagens sind Diabetes und Bluthochdruck. In Deutschland werden seit 1994 durch das Projekt QuaSi-Niere (Qualitätssicherung in der Nierenersatztherapie) statistische Daten von Patienten erhoben, die mit einer chronischen Nierenersatztherapie (Dialyse bzw. Nierentransplantation) behandelt werden. Seit 1997 werden jährlich die Ursachen erfasst, die bei diesen Patienten zum chronischen Nierenversagen geführt haben. Im Erfassungszeitraum sind dabei deutliche Verschiebungen zu beobachten.
Prozentuale Diagnosenverteilung bei Beginn einer Nierenersatz-Therapie[13] Jahr 1996 1997 1999 2000 2001 2002 2003 2004 2005 Diabetes mellitus Typ 2 24 29 30 31 32 32 33 31 32 Nephrosklerose (Hochdruck) 14 16 16 15 17 18 20 22 23 Glomerulonephritis 16 15 14 15 14 14 14 12 13 Interstitielle Nephritis 13 11 11 10 9 9 8 8 8 unbekannte Genese 11 9 10 9 10 9 9 9 8 Zystennieren 6 6 6 6 6 5 5 5 4 Systemerkrankungen* 4 4 4 4 3 4 4 4 4 Verschiedenes 4 4 3 4 4 4 4 4 4 Diabetes mellitus Typ 1 7 6 6 5 4 4 3 3 3 angeborene Krankheiten 1 1 1 1 1 1 1 1 1 *) Unter Systemerkrankungen mit Nierenbeteiligung werden zusammengefasst: Lupusnephritis, Goodpasture-Syndrom, Monoklonale Gammopathien, Amyloidose, Vaskulitiden (Mikroskopische Polyangiitis, Wegener'sche Granulomatose, Churg-Strauss-Syndrom), Anti-Phospholipid-Syndrom, Hämolytisch-urämisches Syndrom, Thrombotisch-thrombozytopenische Purpura.
Die Tabelle zeigt: Angeborene Nierenerkrankungen, Glomerulonephritis, interstitielle Nephritis und Systemerkrankungen sind nur selten Ursache einer dialysepflichtigen Niereninsuffizienz, ihr Anteil nimmt aufgrund immer besserer Behandlungsmöglichkeiten ab. Nierenschäden durch Diabetes mellitus Typ 2 und Bluthochdruck nehmen dagegen zu. So ist bei Menschen mit metabolischem Syndrom, einer Kombination aus Übergewicht, Fettstoffwechselstörung, gestörter Glukoseverwertung und Bluthochdruck, das Risiko einer chronischen Nierenerkrankung deutlich erhöht[14].
Menschen, bei denen aufgrund eines akuten Nierenversagens bereits einmal eine Dialysebehandlung erforderlich wurde, haben ein erheblich erhöhtes Risiko, im weiteren Verlauf ein fortschreitendes chronisches Nierenversagen zu entwickeln.[15][16][17]
Epidemiologie und volkswirtschaftliche Bedeutung
Stadium GFR Prävalenz (USA) 1 > 89 1,8 % 2 60-89 3,2 % 3 30-59 7,7 % 4 15-29 0,4 % Die Prävalenz der chronischen Nierenerkrankung betrug in den USA im Zeitraum von 1988–1994 bei Erwachsenen 10 % und stieg 1999–2004 auf 13,1 % an. 1999–2004 lag bei den 20– bis 39-Jährigen die Prävalenz der Stadien 1 und 2 bei 3 %, die der Stadien 3 und 4 bei 0,7 %. Mit zunehmendem Lebensalter stieg die Prävalenz der chronischen Nierenkrankheit massiv an und lag bei den über 70-Jährigen im Stadium 1 und 2 bei 10 %, im Stadium 3 und 4 bei 38 % (Abb.[18]). Neben dem Alter sind Diabetes und Bluthochdruck die wichtigsten Risikofaktoren für eine chronische Nierenerkrankung. In der Gruppe der 20- bis 59-Jährigen betrug die Prävalenz der chronischen Nierenkrankheit 8,2 % wenn weder Diabetes noch Bluthochdruck vorlagen, 15,2 % wenn nur Bluthochdruck bestand, 33,8 % wenn nur Diabetes vorlag und 43 % bei Patienten, die sowohl an Diabetes als auch an Bluthochdruck litten.[19]
Im Stadium 3 war nur 12 % der Männer und 6 % der Frauen bewusst, dass sie an einer Nierenkrankheit litten, im Stadium 4 wussten nur 42 % der Betroffenen von ihrer Erkrankung.[20]
In Deutschland gibt die QuaSi-Niere für das Jahr 2005 eine Prävalenz von 769 Dialysepatienten und 288 Nierentransplantierten pro Million Einwohner an, dies entspricht 63.427 Dialysepatienten und 23.724 Nierentransplantierten. Seit 1995 ist die Zahl der Dialysepatienten um 53 % gestiegen, die der Nierentransplantierten um 78 %. Dieser Anstieg ist ausschließlich in der Altersklasse der über 65-Jährigen erfolgt. In der Altersklasse der unter 65-Jährigen sind Inzidenz und Prävalenz der chronischen Nierenersatztherapie stabil geblieben. Es gibt in Deutschland keine Zahlen zur Prävalenz der Stadien 1–4 einer chronischen Nierenkrankheit.Durch die hohe Rate an Herz-Kreislauf-Komplikationen und durch die Notwendigkeit von teuren Nierenersatzverfahren (Dialyse und Nierentransplantation) im Stadium 5 entstehen durch das chronische Nierenversagen hohe Kosten für das Gesundheitssystem. Wenn man annimmt, dass die Dialysebehandlung im Jahr ca. 50.000–60.000 Euro pro Patient kostet, wurden in Deutschland im Jahr 2005 allein für die Dialysebehandlung über 3 Milliarden Euro ausgegeben. Über die Folgekosten der Stadien 1–4 gibt es keine Zahlen. Aufgrund des demographischen Wandels wird es in den kommenden Jahren zu einer erheblichen Zunahme an alten nierenkranken Menschen kommen, die an einer Vielzahl gravierender Begleit- und Folgeerkrankungen leiden und die Gesundheitssysteme vor erhebliche Herausforderungen stellen werden.[21]
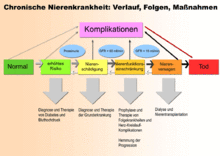
Natürlicher Verlauf, Folgekrankheiten und Komplikationen
Der Normalwert der glomerulären Filtrationsrate (GFR) hängt ab von Alter, Geschlecht und Körpergröße. Beim jungen Erwachsenen liegt der Normalwert der GFR zwischen 120 und 130 ml/min/1,73 m². Bei Frauen ist die GFR um ca. 8 % niedriger als bei Männern. Ab dem 20. bis 30. Lebensjahr nimmt die GFR jährlich um ca. 1 ml/min/1,73 m² ab. Im Alter von 70 Jahren liegt der Normalwert der GFR im Mittel bei ca. 70 ml/min/1,73 m² mit einem breiten Schwankungsbereich.
Bei den meisten Patienten mit chronischer Nierenkrankheit nimmt die Nierenfunktion im Lauf der Zeit ab.
Der Verlauf einer chronischen Nierenkrankheit hängt ab
- von der GFR zum Zeitpunkt der Diagnose und
- vom Abfall der GFR im über die Zeit, der Progression. Das Maß der Progression ist der jährliche Abfall der GFR, ausgedrückt in ml/min/1,73 m²/Jahr.
Die Progression einer Nierenkrankheit ist für einen individuellen Patienten über die Zeit meist relativ konstant, kann zwischen verschiedenen Patienten aber stark schwanken. Ein langsam progressiver Verlauf kann sich über Jahrzehnte erstrecken, ein rasch progressiver Verlauf kann innerhalb von Monaten zum Endstadium des dialysepflichtigen Nierenversagens führen.
Die Progression hängt ab
- von der Grunderkrankung: Bei diabetischer Nephropathie, Glomerulonephritis, Zystennierenerkrankung und Nierenerkrankung bei Transplantatempfängern ist die Progression rascher als bei Nierenerkrankung durch Bluthochdruck und interstitieller Nephritis.
- von nicht beeinflussbaren Faktoren: Bei Menschen mit schwarzer Hautfarbe, schlechterer Nierenfunktion zum Zeitpunkt der Diagnose, Männern und älteren Patienten ist die Progression rascher.
- von beeinflussbaren Faktoren: Eine raschere Progression findet sich bei hoher Eiweißausscheidung im Urin (Proteinurie), niedrigem Albumin im Serum, hohem Blutdruck, schlechter Blutzuckereinstellung bei Diabetikern und bei Rauchern.
- Der Einfluss von erhöhten Blutfetten und Blutarmut auf die Progression ist nicht geklärt.
GFR Herz-Kreislauf Komplikationen
Sterblichkeit >60 2,11 0,76 45-59 3,65 1,08 30-44 11,29 4,76 15-29 21,80 11,36 <15 36,60 14,14 ml/min/1,73 m² pro 100 Personen-Jahre[22] Mit zunehmender Einschränkung der Nierenfunktion treten Folgekrankheiten in mehreren Organsystemen auf:
- Bluthochdruck. Etwa 55-75 % aller Menschen mit einer eingeschränkten Nierenfunktion leiden an Bluthochdruck. Ein vorbestehender Bluthochdruck kann Ursache der Nierenfunktionseinschränkung sein. Die eingeschränkte Nierenfunktion führt ebenfalls zu Bluthochdruck, Ursachen sind eine Flüssigkeitsüberladung, eine Aktivierung des Renin-Angiotensin-Aldosteron-Systems, eine Aktivierung des sympathischen Nervensystems, eine Verkalkung des arteriellen Gefäßsystems incl. der Nierengefäße sowie Störungen im Stoffwechsel einer Vielzahl weiterer Faktoren (Prostaglandine, Bradykinine, Endothelin, Stickstoffmonoxid). Bluthochdruck ist eine wichtige Ursache für das bei Nierenkranken erheblich erhöhte Herz-Kreislauf-Risiko.
- Störungen des Knochenstoffwechsels. Ursache sind Veränderungen des Vitamin D-Stoffwechsels, eine verminderte Aufnahme von Calcium über den Darm und eine verminderte Ausscheidung von Phosphat über die Niere. Folgen sind ein verminderter Calcium- und Vitamin D-Spiegel im Blut, ein erhöhter Spiegel von Phosphat und Parathormon, ein vermehrter Knochenumbau sowie Weichteilverkalkungen, die auch die Koronargefäße und Herzklappen betreffen.
- Störungen der Blutbildung. Eine verminderte Produktion des Hormons Erythropoetin durch die Niere führt zu Anämie infolge verminderter Bildung von roten Blutkörperchen im Knochenmark.
- Störungen des Elektrolythaushaltes. Bei fortgeschrittener Nierenfunktionseinschränkung kann es zu einem Anstieg des Kalium-Spiegels im Blut infolge verminderter Ausscheidung kommen. Im Extremfall kann dies zu tödlichen Herzrhythmusstörungen führen.
- Störungen des Säure-Basen-Haushaltes. Die verminderte Ausscheidung von Protonen führt zu einer Übersäuerung des Blutes (Azidose). Die Azidose führt zu einem Verlust an Knochensubstanz.
- Überwässerung. Aufgrund einer verminderten Ausscheidung von Wasser kann es zur vermehrten Wassereinlagerung in Geweben (Ödemen) und in der Lunge kommen.
- Auftreten weiterer körperlicher und geistiger Funktionseinschränkungen wie Abnahme der geistigen Leistungsfähigkeit[23][24] und erhöhtes Risiko einer altersabhängigen Makuladegeneration[25].
- Störungen des Immunsystems: Mit zunehmender Nierenfunktionseinschränkung steigt das Risiko, an einer Lungenentzündung zu erkranken bzw. daran zu versterben bis auf das 15-fache an[26], die Ansprechraten nach Impfung gegen Hepatitis B und Pneumokokken sinken. Dem gegenüber ist das Ansprechen auf eine Impfung gegen Grippe auch bei Dialysepatienten gut[27].
Ab dem Stadium 3 ist das Risiko eines akuten Nierenversagens erhöht, insbesondere wenn zusätzlich Diabetes, Bluthochdruck oder eine erhöhte Eiweißausscheidung vorliegt.[28]
KDOQI-Stadium Dialysebeginn Sterblichkeit 2 1,1 % 19,5 % 3 1,3 % 24,3 % 4 19,9 % 45,7 % innerhalb von 5 Jahren[29] Im Stadium 5 des chronischen Nierenversagens treten zunehmend Komplikationen der Harnvergiftung (Urämie) auf: Gewichtsverlust und Unterernährung aufgrund von Appetitlosigkeit, Übelkeit und Erbrechen, Flüssigkeitsüberladung, Blutungsneigung, Herzbeutelentzündung, Depression, Abnahme körperlichen Leistungsfähigkeit, Schäden des peripheren Nervensystems, Unfruchtbarkeit und erhöhte Infektanfälligkeit. Auffällig ist der harnartige Mundgeruch (Foetor uraemicus).
Haupttodesursache für alle Patienten mit chronischem Nierenversagen sind Herz-Kreislauf-Krankheiten, wie koronare Herzkrankheit, linksventrikuläre Hypertrophie, Gefäßverkalkungen und Herzschwäche. Zweithäufigste Todesursache bei Dialysepatienten sind Infektionen.[30] Vor allem bei älteren Patienten ist die Wahrscheinlichkeit, an Komplikationen des Herz-Kreislauf-Systems zu versterben, viel höher als die Wahrscheinlichkeit, an die Dialyse zu kommen (Abb. [31]). Die Sterblichkeit (Mortalität) ist bereits bei geringer Einschränkung der Nierenfunktion deutlich erhöht und steigt mit zunehmender Nierenfunktionseinschränkung exponentiell an[32]. Unabhängig vom Grad der Nierenfunktionseinschränkung steigt die Mortalität auch mit zunehmender Urin-Eiweiß-Ausscheidung (Proteinurie).[33] Von besonderer Wichtigkeit ist in allen Stadien einer chronischen Nierenkrankheit daher die Vorbeugung von Erkrankungen des Herz-Kreislauf-Systems.
Die erhöhte Erkrankungs- und Sterberate an Herz-Kreislauf-Erkrankungen bei Patienten mit chronischer Nierenkrankheit erklärt sich nur teilweise durch das vermehrte Vorkommen von traditionellen kardiovaskulären Risikofaktoren (Herz-Kreislauf-Risikofaktoren). Zusätzlich treten bei chronischer Nierenkrankheit nicht-traditionelle Risikofaktoren[34] auf, die mit der eingeschränkten Nierenfunktion oder deren Behandlung zusammenhängen.
Traditionelle Risikofaktoren Nicht-traditionelle Risikofaktoren - Alter
- männliches Geschlecht
- familiäre Belastung
- Diabetes mellitus
- Bluthochdruck
- erhöhtes LDL-Cholesterin
- vermindertes HDL-Cholesterin
- Bewegungsmangel
- Menopause
- Nikotin
- Übergewicht
Biochemische Faktoren - Mikroalbuminurie/Proteinurie
- gestörter Mineralstoffwechsel
- Gefäßverkalkung
- Homocystein
- Gerinnungsfördernde Faktoren
- andere "Urämietoxine"
Pathologische Prozesse
- Entzündung
- Oxidativer Stress
- gestörte Endothelfunktion
- Unter- und Fehlernährung
- Sympathikus-Überaktivität
Herzmuskelverdickung begünstigende Faktoren - Volumenüberladung
- Blutarmut (Anämie)
- gestörte Salz- und Wasserausscheidung
- Dialysefistel
- Drucküberladung
Symptome von chronischem Nierenversagen
In den Stadien 1-4 verläuft eine chronische Nierenkrankheit meist ohne jegliche Symptome. Eine hohe Eiweißausscheidung im Urin kann zu Schäumen des Urins und Wassereinlagerungen führen. Eine sehr hohe Ausscheidung von roten Blutkörperchen (Makrohämaturie) kann sich in einer Braunverfärbung des Urins äußern und weist meist auf Erkrankungen der ableitenden Harnwege hin, seltener auf eine Blutung bei Zystennieren oder eine IgA-Nephropathie. Schmerzen in der Nierengegend weisen auf Wirbelsäulen- und Bandscheibenprobleme, Nierensteine, eine Nierenbeckenentzündung, akute Komplikationen einer Zystennierenerkrankung sowie sehr selten auf eine akute Glomerulonephritis hin. Eine chronische Nierenkrankheit verläuft dagegen in der Regel schmerzfrei.
Im fortgeschrittenen Stadium 4 und im Stadium 5 kommt es zu einer zunehmenden Einschränkung der körperlichen und geistigen Leistungsfähigkeit, Appetitlosigkeit, Erbrechen und Übelkeit, Wassereinlagerungen, Atemnot und Hautveränderungen[35]. Bei weit fortgeschrittener Nierenfunktionseinschränkung können Krampfanfälle auftreten.
Therapie
Behandlungsziele[36] bei chronischen Nierenkrankheiten sind
- bei Risikogruppen die Vorbeugung insbesondere die frühzeitige Erkennung und konsequente Behandlung von Diabetes und Bluthochdruck,
- im Stadium 1 und 2
- die frühzeitige Erkennung einer Nierenerkrankung und
- die Behandlung der unterschiedlichen Grunderkrankungen
- im Stadium 2 bis 4
- die Verhinderung und Behandlung von Herz-Kreislauf-Komplikationen und
- die Hemmung der Progression
- im Stadium 3 bis 5 die Behandlung von Komplikationen und Folgekrankheiten
- im Stadium 5 Dialyse und Nierentransplantation, bzw. supportive Therapie, falls ein Nierenersatzverfahren nicht möglich ist.
Vorbeugung des chronischen Nierenversagens
Die Vorbeugung chronischer Nierenkrankheiten vermindert möglicherweise die Anzahl potentieller Dialysepatienten und reduziert die Morbidität und Mortalität an Herz-Kreislauf-Komplikationen[37].
Früherkennung
Chronische Nierenerkrankungen verlaufen in den frühen Stadien ohne Beschwerden. Aus diesem Grund wurden in mehreren Staaten Früherkennungsuntersuchungen durchgeführt, so in den USA (NHANES III), Australien (AusDiab Study), Japan (Okinawa Screening Program), den Niederlanden (PREVEND Study), Island, Indien und Singapur. Als Früherkennungsuntersuchungen eingesetzt wurden der Nachweis von Eiweiß und Albumin im Urin, sowie die Kreatinin-Bestimmung im Blut. Durch gesetzlich vorgeschriebene Früherkennungsmaßnahmen konnte in Japan bei jungen Erwachsenen die Häufigkeit fortschreitender entzündlicher Nierenerkrankungen (progressiver Glomerulonephritiden) vermindert werden, das mittlere Alter zum Zeitpunkt des Dialysebeginns hat in Japan im gleichen Zeitraum signifikant zugenommen.[38]
Veränderung von Lebensgewohnheiten
Bluthochdruck und Diabetes sind die häufigsten Ursachen des chronischen Nierenversagens. Gesicherte Allgemeinmaßnahmen zur Vorbeugung sind:
- Reduktion von Übergewicht,
- regelmäßige körperliche Betätigung,
- Reduktion des Kochsalzkonsums,
- Ernährung mit reichlich Früchten und Gemüse sowie wenig gesättigtem Fett,
- Nikotinverzicht[39]
- Reduktion des Alkoholkonsums
Im Gegensatz zu einer weit verbreiteten Ansicht kann reichliches Trinken zwar die Entstehung von Nierensteinen günstig beeinflussen, verbessert aber nicht die Nierenfunktion. Es gibt sogar Hinweise, dass das Trinken von großen Flüssigkeitsmengen die Progression chronischer Nierenkrankheiten beschleunigen kann[40].
Medikamentöse Maßnahmen
Frühzeitige Erkennung und konsequente medikamentöse Behandlung von Diabetes und Bluthochdruck kann die Entstehung einer chronischen Nierenkrankheit verhindern.
Progressionshemmung
Chronische Nierenkrankheiten neigen zur kontinuierlichen Verschlechterung. Ziel der Behandlung ist daher, die Progression zu hemmen, d.h. den jährlichen Nierenfunktionsverlust zu mindern[41].
Patienten mit chronischer Nierenkrankheit sollten Medikamente meiden, die für die Niere schädlich sein können, dazu zählen z. B.
- nichtsteroidale Antiphlogistika, darunter die am weitesten verbreiteten Schmerzmedikamente wie Diclofenac oder Ibuprofen;
- jodhaltige Röntgenkontrastmittel;
- Aminoglykoside, eine ganz bestimmte Gruppe von Antibiotika.
Eine medikamentöse Senkung des Blutdruckes hemmt die Progression, als Ziel der Blutdruckbehandlung werden Blutdruckwerte unter 130/80 mmHg angegeben. Es gibt Hinweise darauf, dass von dieser intensiven Blutdrucksenkung (gegenüber einem Standard-Zielblutdruck von 140/90 mmHg) nur die Patienten profitieren, bei denen auch eine signifikante Proteinurie nachweisbar ist; bislang liegen aber nur Daten zu Amerikanern schwarzafrikanischer Herkunft vor[42]. Meist sind mehrere Hochdruckmedikamente in Kombination erforderlich, um eine intensive Blutdrucksenkung zu erreichen.
Bei Patienten mit diabetischer Nephropathie oder erhöhter Eiweiß-Ausscheidung im Urin[43] können ACE-Hemmer und AT1-Antagonisten, zwei verwandte Klassen blutdrucksenkender Medikamente, die Progression in besonderem Maße hemmen. Ziel der Behandlung ist, die Urin-Eiweiß-Ausscheidung (Proteinurie) auf Werte unter 500-1000 mg pro Tag zu senken. Um dies zu erreichen, muss unter Umständen ein niedrigerer Zielblutdruck als 130/80 mmHg angestrebt werden. Gelingt es nicht, die Proteinurie ausreichend zu senken, werden ACE-Hemmer und AT1-Antagonisten auch in Kombination[44] oder in sehr hoher Dosierung[45] eingesetzt, ggf. sogar zusätzlich mit Aldosteronantagonisten[46] kombiniert. Da diese Medikamente oftmals nur zur Behandlung des Bluthochdrucks zugelassen wurden, handelt es sich bei der Behandlung häufig um einen sogenannten Off-Label-Use, das heißt, um einen Medikamenteneinsatz außerhalb der eigentlichen Zulassung. Diese Art der Kombinationsbehandlung darf nur bei Erkrankungen mit großer Proteinurie eingesetzt werden und muss engmaschig überwacht werden[47], in der Routinebehandlung des Bluthochdrucks bringt die Kombination aus ACE-Hemmer und AT1-Antagonist keinen zusätzlichen Nutzen und ist sogar mit erhöhten Komplikationsraten behaftet[48].
Die Eiweißzufuhr mit der Nahrung sollte moderat eingeschränkt werden. Empfohlen wird, am Tag 0,8 – 1 g Eiweiß pro Kilogramm Körpergewicht zu sich zu nehmen. Eine strenge Einschränkung der Proteinzufuhr bringt keinen zusätzlichen Nutzen. [49]
Es gibt Hinweise darauf, dass eine medikamentöse Senkung der Blutfette[50] und eine Behandlung der Übersäuerung mit Natron [51] die Progression hemmen kann.
Für alle Maßnahmen gilt, je früher im Verlauf einer Nierenkrankheit damit begonnen wird, desto größer ist die Aussicht auf Erfolg.
Behandlung von Folgekrankheiten
Definitionen der KDIGO (Kidney Disease Improving Global Outcomes)[52]
Mineral- und Knochenstoffwechselstörung bei chronischer Nierenerkrankung:
Systemische Störung des Mineral- und Knochenstoffwechsels bei chronischer Nierenerkrankung, die sich manifestiert durch
1. Veränderungen des Calcium-, Phosphat-, Parathormon oder Vitamin D - Stoffwechsels und/oder
2. Veränderungen im Umsatz, Volumen, Wachstum oder Stärke des Knochens und/oder
3. Weichteil- oder Gefäßverkalkungen. Renale Osteodystrophie: Veränderungen der Knochenstruktur (Morphologie) bei chronischer Nierenerkrankung, die nachgewiesen wird durch
quantitative feingewebliche Untersuchung einer Knochenprobe (Histomorphometrie einer Knochenbiopsie).
Störung des Mineral- und Knochenstoffwechsels
Pathogenese
Ab dem Stadium 3 der chronischen Nierenkrankheit sinkt die Ausscheidung von Phosphat in den Urin. Dies führt zu einem Anstieg des Phosphatspiegels im Blut (Hyperphosphatämie). Als Reaktion darauf wird von der Nebenschilddrüse vermehrt Parathormon in das Blut abgegeben (Hyperparathyreoidismus); die Osteoblasten des Knochens produzieren vermehrt Fibroblast Growth Factor 23 (FGF-23). In der Niere nimmt die Aktivierung von 25(OH)Vitamin D3 zu Calcitriol ab, der Calcitriol-Spiegel im Blut sinkt, die Calcium-Aufnahme im Darm nimmt ab, der Calcium-Spiegel im Blut sinkt, dies wiederum stimuliert die Freisetzung von Parathormon. In der gesunden Niere würde der Anstieg von Parathormon eine vermehrte Ausscheidung von Phosphat und eine vermehrte Rückgewinnung (Rückresorption) von Calcium aus dem Filtrat des Nierenkörperchens (Primärharn) bewirken; FGF-23 würde ebenfalls die Phosphat-Ausscheidung stimulieren. Die Folge wäre ein Abfall des Phosphat-Spiegels und Anstieg des Calciums im Blut. Die geschädigte Niere kann jedoch nicht adäquat auf Parathormon und FGF-23 reagieren, ein Anstieg von Phosphatausscheidung und Calciumrückresorption bleibt aus. Der erhöhte Parathormonspiegel führt jedoch zur Freisetzung von Calcium und Phosphat aus den Knochen, der Knochenumbau nimmt zu, die Knochensubstanz nimmt ab, die Gefahr von Knochenbrüchen steigt. Mit weiter sinkender Nierenfunktion steigt der Phosphatspiegel im Blut zunehmend an, es kommt zur aktiven Ablagerung von Calcium-Phosphat in den Weichteilen. Gefäße und Weichteilgewebe verkalken, Durchblutungsstörungen, Herz-Kreislauf-Komplikationen und eine verminderte Lebenserwartung sind die Folge. Diese Kombination aus Knochenstoffwechselstörung und Gefäßverkalkung wird neuerdings als Störung des Mineral- und Knochenstoffwechsels bei chronischer Nierenerkrankung oder CKD-MBD (Chronic Kidney Disease-Mineral and Bone Disorder) bezeichnet.
Diagnostik
Die Behandlung setzt regelmäßige Bestimmungen von Calcium, Phosphat, Parathormon und Alkalischer Phosphatase voraus. Zudem ist eine Bestimmung des 25(OH)Vitamin D3-Spiegels erforderlich. Mit der Überwachung dieser Laborparameter soll ab dem Stadium 3 begonnen werden. Die KDIGO-Leitlinien geben Untersuchungsintervalle und Zielwerte vor, die jeweils vom Krankheitsstadium abhängen.
Die feingewebliche Untersuchung einer Gewebeprobe des Knochens (Knochenbiopsie) wird empfohlen bei unerklärten Frakturen, anhaltenden Knochenschmerzen, unerklärter Calciumerhöhung (Hyperkalziämie), unerklärter Phosphaterhöhung (Hyperphosphatämie) oder -verminderung (Hypophosphatämie), Verdacht auf Aluminium-Überladung und vor einer Therapie mit Bisphosphonaten.
Mineral- und Knochenstoffwechselsstörung bei chronischer Nierenkrankheit einerseits und Osteoporose bei Nierengesunden andererseits sind unterschiedliche Krankheitsbilder, die nicht verwechselt werden dürfen. Im Gegensatz zur Allgemeinbevölkerung besteht bei chronisch nierenkranken Patienten keine Beziehung zwischen Knochendichte und Risiko von Knochenbrüchen. Die routinemäßige Bestimmung der Knochendichte (Osteodensitometrie) wird bei Vorliegen einer chronischen Nierenerkrankung daher nicht empfohlen.
Zur Diagnostik von Gefäßverkalkungen wird eine konventionelle seitliche (laterale) Abdomen-Röntgenaufnahme zum Nachweis oder Ausschluss von Gefäßverkalkungen sowie eine Echokardiographie zum Nachweis oder Ausschluss von Herzklappenverkalkungen empfohlen.
Therapie
Es wird angestrebt Calcium- und Phosphatspiegel im Normalbereich zu halten. Bei Dialysepatienten ist es allerdings oft nicht möglich, normale Phosphatwerte zu erreichen, es wird aber angestrebt, erhöhte Phosphatwerte in Richtung Normalbereich abzusenken.
Bei erhöhten Phosphatwerten wird bislang die Phosphatzufuhr über die Nahrung eingeschränkt. Eine aktuelle Untersuchung konnte den Wert einer phosphatarmen Diät jedoch nicht belegen.[53]
Die medikamentöse Behandlung erhöhter Phosphatspiegel erfolgt mit Substanzen, welche Phosphat im Darm binden und so die Aufnahme in den Körper hemmen. Als Phosphatbinder eingesetzt werden derzeit Calcium- und Aluminium-Salze, Sevelamer (ein Polymer) und Lanthankarbonat. Bei erhöhten Calcium-Werten, arteriellen Gefäßverkalkungen, vermindertem Knochenumsatz (adynamem Knochen) und/oder erniedrigtem Parathormon werden bevorzugt calciumfreie Phosphatbinder eingesetzt, die Zufuhr calciumhaltiger Phosphatbinder wird eingeschränkt, ebenso die Gabe von Calcitriol und aktiven Vitamin-D-Abkömmlingen. Aluminium kann sich ebenfalls in den Knochen einlagern und zu einer Erkrankung des Knochens führen. Eine Langzeitbehandlung mit Alumnium-haltigen Phosphatbindern wird daher vermieden, der Aluminium-Spiegel muss regelmäßig kontrolliert werden.
Vitamin-D-Mangel Vitamin D Defizienz 25(OH) D3 (Calcidiol) < 10 ng/ml (25 nmol/l) Vitamin D Insuffizienz 25(OH) D3 (Calcidiol) 10-30 ng/ml (25-80 nmol/l) Ein Vitamin-D-Mangel (Vitamin-D-Defizienz, Vitamin-D-Insuffizienz) wird durch Gabe eines Vitamin-D-Präparates ausgeglichen.
Der optimale Parathormon-Bereich ist nicht bekannt. Spricht ein erhöhtes Parathormon auf Behandlung durch Diät, Phosphatbinder, Calcium und/oder Vitamin D nicht an, oder steigt sogar weiter an, kommen aktive Vitamin-D-Metabolite zum Einsatz. Bei diesen Substanzen (Alfacalcidol, Calcitriol) ist der Stoffwechselschritt der Vitamin-D-Aktivierung, der normalerweise in der Niere abläuft, bereits erfolgt. Als Nebenwirkung wird allerdings die Calcium- und Phosphataufnahme über den Darm stimuliert. Neuerdings werden daher aktive Vitamin-D-Abkömmlinge (z.B. Paricalcitol) eingesetzt, welche die Parathormonsekretion aus der Nebenschilddrüse besonders stark hemmen, und eine geringere Wirkung auf den Darm ausüben. Steigt die Konzentration von Calcium und Phosphat unter Vitamin-D-Therapie zu stark an, muss Vitamin D reduziert werden. Eine zu starke Hemmung der Parathormonsekretion sollte ebenfalls vermieden werden, da diese zu einem verminderten Knochenumbau (adyname Knochenerkrankungen) führt und Weichteilverkalkungen begünstigt.
Bei zunehmender Nierenfunktionseinschränkung ändert sich der Knochenstoffwechsel. So nimmt die Empfindlichkeit des Knochens gegenüber Parathormon ab. Aus diesem Grund versucht man bei Dialysepatienten, die Parathormon-Werte in einem Bereich zwischen ungefähr dem Zweifachen und dem Neunfachen des oberen Normalbereichs der eingesetzten Bestimmungsmethode zu halten.
Zur Behandlung erhöhter Parathormonwerte bei Dialysepatienten ist seit 2004 Cinacalcet zugelassen. Cinacalcet bindet an den Calciumrezeptor der Nebenschilddrüse, simuliert einen erhöhten Calciumspiegel und hemmt so die Parathormonsekretion. Trotz dieser Maßnahmen gelingt es manchmal nicht, ein Ansteigen des Parathormons zu verhindern. In diesem Fall müssen die Nebenschilddrüsen operativ entfernt werden.
Eine Behandlung mit Bisphosphonaten sollte bei erhöhtem Parathormon und/oder Stadium 3-5 vermieden werden, im Zweifelsfällen sollte vor einer Bisphosphonat-Behandlung eine Knochenbiopsie erfolgen. Nach erfolgreicher Nierentransplantation und Behandlung mit Steroiden kann dagegen eine Knochendichtemessung (Osteodensitometrie) und eine Behandlung mit Bisphosphonaten, ggf. in Kombination mit Vitamin D und aktiven Vitamin-D-Metaboliten sinnvoll sein. [52][54]
Eine Übersäuerung des Blutes führt ebenfalls zu einem Verlust an Knochensubstanz. Die Behandlung erfolgt mit Alkalisalzen wie Citrat oder Bicarbonat. Die Gabe von Bicarbonat verlangsamt zudem möglicherweise den Nierenfunktionsverlust und verbessert den Ernährungszustand.[51]
Renale Anämie
Ferritin-Zielbereich KDOQI-Stadium Ferritin-Zielbereich 3 und 4 100-500 ng/ml 5 200-500 ng/ml Mit fortschreitender Nierenfunktionseinschränkung sinkt die Produktion des Botenstoffes Erythropoetin. Erythropoetin wird in den Nieren gebildet und steuert die Produktion der roten Blutkörperchen im Knochenmark. Die Konzentration des roten Blutfarbstoffes (Hämoglobin) nimmt daher mit zunehmender Nierenfunktionseinschränkung ab. Es kommt zur Blutarmut (renalen Anämie) mit einem Abfall der körperlichen Leistungsfähigkeit.[55][56]
Zur Diagnose und Behandlung der renalen Anämie sind regelmäßige Bestimmungen von Hämoglobin, Ferritin und Transferrinsättigung erforderlich. Bei der Erstuntersuchung sollte ein großes Blutbild incl. der Retikulozyten angefertigt werden. Eine Bestimmung des Erythropoetin-Spiegels ist nicht erforderlich. Eine Anämie liegt vor, wenn die Hämoglobinkonzentration des Blutes bei Frauen auf einen Wert unter 12,0 g/dl abgesunken ist, bei Männern unter 13,5 g/dl.
Hämoglobin-Zielbereich KDOQI-Stadium Hb-Zielbereich 3 bis 5 11,0-12,0 g/dl Durch Gabe von Eisen, bei Dialysepatienten bevorzugt intravenös, werden Ferritin-Spiegel und Transferrin-Sättigung in den hochnormalen Bereich angehoben. In der Regel muss jedoch zusätzlich Erythropoetin gegeben werden um das Hämoglobin in den Zielbereich anzuheben. Die Zielbereiche für Ferritin und Hämoglobin entsprechen dabei nicht den Normalbereichen. Die angestrebten Ferritin-Spiegel liegen höher als die Normwerte, die angestrebte Hämoglobinkonzentration liegt etwas unter dem Normalbereich. Eine Anhebung des Hämoglobin-Wertes in den Normalbereich bringt keinen zusätzlichen Nutzen, sondern führt zu vermehrtem Auftreten von Bluthochdruck, Schlaganfällen und Shunt-Thrombosen; möglicherweise nehmen auch Mortalität, Herz-Kreislauf-Komplikationen und Progression der Nierenfunktionseinschränkung zu.[57][58][59][60] Die Ursache der erhöhten Komplikationsraten bei höheren Hämoglobin-Zielwerten ist nicht bekannt. Diskutiert werden, ein direkter Effekt des Hämoglobins, z. B. durch erhöhte Viskosität des Blutes, eine Nebenwirkung von Erythropoetin, eine Nebenwirkung von Eisen, der unter Erythropoetin-Behandlung erhöhte Blutdruck oder die Folge eines verminderten Ansprechens auf Erythropoetin.[61]
Blutübertragungen sind nur in seltenen Fällen erforderlich und werden nach Möglichkeit vermieden.
Vorbeugung von Komplikationen
Patienten mit chronischer Nierenkrankheit sind in erster Linie durch Herz-Kreislauf-Erkrankungen bedroht, wie koronare Herzkrankheit, Herzversagen[62], Schlaganfall[63] und arterielle Verschlusskrankheit. Die Gefahr, im Verlauf der Erkrankung von der Dialyse abhängig zu werden, ist demgegenüber deutlich geringer. Eine Nierenkrankheit im Stadium 5 ist ein kardiovaskulärer Risikofaktor, der so schwer wiegt, wie ein durchgemachter Herzinfarkt[64]; die Sterblichkeit an Herz-Kreislauf-Komplikationen ist etwa 10 - 20 mal höher als in der Allgemeinbevölkerung. Liegt zusätzlich ein Diabetes mellitus vor, ist die Sterblichkeit etwa 40 % höher als bei Nierenkranken im Stadium 5 ohne Diabetes[65].
Bei Vorliegen einer chronischen Nierenkrankheit sollten daher die Blutfette Gesamt-Cholesterin, LDL-Cholesterin, HDL-Cholesterin und Triglyceride bestimmt werden. Ist das LDL-Cholesterin erhöht und durch eine Umstellung der Ernährung und vermehrte körperliche Betätigung nicht ausreichend zu senken, wird eine medikamentöse Senkung durch Einsatz eines Statins empfohlen, entsprechend den Leitlinien, die für die Normalbevölkerung gelten[66]. Für das Stadium 5 der chronischen Nierenkrankheit empfehlen die K/DOQI-Leitlinien eine besonders aggressive Senkung des LDL-Cholesterin auf Werte unter 100 mg/dl (2,6 mmol/l), bei Vorliegen eines Diabetes werden von manchen Autoren sogar Zielwerte unter 70 mg/dl (1,82 mmol/l) empfohlen.
Es muss allerdings kritisch angemerkt werden, dass diese Empfehlungen derzeit nicht durch randomisierte, kontrollierte Studien abgesichert sind. In den meisten großen Studien zur Lipidsenkung waren Nierenkranke ausgeschlossen, so dass nur Post-hoc-Analysen weniger Studien zur Verfügung stehen[67]. Diese belegen im Stadium 3 der Nierenerkrankung den günstigen Einfluss einer Senkung des LDL-Cholesterins auf das Auftreten von Herz-Kreislauf-Komplikationen[68][69]. Die einzige kontrollierte Studie zum Einsatz des Lipidsenkers Atorvastatin bei Dialysepatienten mit Diabetes mellitus ergab dagegen keinen Vorteil in der Behandlungsgruppe[70]. Kohortenstudien an chronisch Nierenkranken und Hämodialyse-Patienten ergaben sogar ein besseres Überleben bei höheren Gesamt- und LDL-Cholesterin[71]. Diese im Vergleich zur Normalbevölkerung umgekehrte Beziehung zwischen Risikofaktor und Verlauf wird auch als reverse Epidemiologie bezeichnet[72][73]. Für das Stadium 4 der chronischen Nierenkrankheit gibt es bislang keine kontrollierten Studien zum Einsatz von Lipidsenkern, die Ergebnisse einer großen multinationalen Doppelblindstudie werden in den nächsten Jahren erwartet[74].
Diese diskrepanten Befunde werden neuerdings dahingehend interpretiert, dass im Stadium 5 die Veränderungen am Herz-Kreislauf-System so weit fortgeschritten sind, so dass sie nicht mehr gut auf eine medikamentöse Senkung des LDL-Cholesterins ansprechen. Zudem können niedrige Cholesterin-Spiegel Folge der bei Nierenkranken häufigen vorkommenden Fehlernährung und chronischen Entzündungskonstellation sein. Konsequenterweise empfiehlt die Amerikanische Herz-Gesellschaft (American Heart Association), bereits die frühen Stadien einer chronischen Nierenkrankheit in die höchste kardiovaskuläre Risikostufe einzuordnen und eine besonders aggressive Senkung des Cholesterins anzustreben[75].
Bislang gibt es noch keine Daten, die bei chronischer Nierenkrankheit einen zusätzlichen günstigen Effekt zeigen, wenn zusätzlich zum LDL-Cholesterin die Triglyceride oder das HDL-Cholesterin medikamentös beeinflusst werden.
Nierenersatztherapie
Im Stadium 4 einer chronischen Nierenerkrankung (GFR < 30 ml/min/1,73 m²) sollten Patient, Angehörige und Arzt entscheiden, welches Nierenersatzverfahren im Fall eines weiteren Nierenfunktionsverlustes eingesetzt werden sollte[76]. Zur Auswahl stehen:
- Hämodialyse (Blutwäsche),
- Peritonealdialyse (Bauchfelldialyse),
- Nierentransplantation (ggf. präemptiv, d.h. noch vor Beginn einer Dialysebehandlung, wenn ein geeigneter Spender zur Verfügung steht),
- konservative Therapie (medikamentöse und supportive Therapie, wenn eine Dialysebehandlung oder eine Nierentransplantation vom Patienten nicht gewünscht wird).
Im Stadium 5 einer chronischen Nierenerkrankung (GFR < 15 ml/min/1,73 m²) wird mit einem Nierenersatzverfahren begonnen. Ein früher Beginn der Nierenersatztherapie (d.h. bei einer eGFR 10-14 ml/min/1,73 m²) bringt gegenüber einem späteren Dialysebeginn (eGFR 5 - 7 ml/min/1,73 m²) keinen Vorteil.[77][78] Ohne Nierenersatztherapie führt der weitere Krankheitsverlauf zum Tod in der Urämie. Bei sehr alten und gebrechlichen Menschen bewirkt die Dialysebehandlung im Stadium 5 eine Lebensverlängerung von ca. zwei Jahren,[79] im Rahmen der Einleitung der Nierenersatztherapie kann es aber auch zu einer deutlichen Verschlechterung des Allgemeinzustandes kommen[80]; in solchen Fällen kann eine konservative Behandlung eine akzeptable Alternative darstellen.[81]
Leitlinien
1997 wurde von der National Kidney Foundation (Nationale Nierenstiftung der USA) die Dialyse-Ergebnisqualitäts-Initiative (Dialysis Outcomes Quality Initiative oder DOQI) begonnen. Dieses Projekt hatte zum Ziel, die Betreuung von Dialysepatienten zu verbessern. Es entstanden evidenzbasierte Leitlinien zur Hämodialyse, zur Peritonealdialyse (Bauchfelldialyse), zum Gefäßzugang und zur Ernährung von Dialysepatienten. 1999 beschloss die nationale Nierenstiftung, die Qualitätsinitiative auf frühe Stadien der chronischen Nierenkrankheit auszuweiten (Kidney Disease Outcomes Quality Initiative oder K/DOQI). 2002 erschien die erste Leitlinie der K/DOQI. Diese Leitlinie legte diagnostische Maßnahmen fest (Evaluation), definierte die derzeit gebräuchliche Stadieneinteilung (Klassifikation) und schlug Maßnahmen zur Abschätzung des Risikos einer Krankheitsverschlechterung und des Auftretens von Komplikationen (Stratifikation) vor.
Derzeit sind zwölf Leitlinien veröffentlicht:
- Hämodialyse
- Peritonealdialyse
- Gefäßzugang
- Anämie-Management
- Ernährung
- Evaluation, Klassifikation und Stratifikation von chronischer Nierenkrankheit
- Fettstoffwechselstörung
- Knochenstoffwechselstörungen
- Knochenstoffwechselstörungen bei Kindern
- Bluthochdruck und Blutdruckbehandlung
- Herz-Kreislauf-Erkrankungen bei Dialysepatienten
- Diabetes und chronische Nierenkrankheit.
Die Kidney Disease: Improving Global Outcomes (KDIGO) ist eine globale gemeinnützige Stiftung mit dem Ziel einer weltweiten Verbesserung der Versorgung von chronischen Nierenkranken und deren Behandlungsergebnissen.[82] Die KDIGO hat folgende Leitlinien veröffentlicht:
- Vorbeugung, Diagnose Evaluation und Behandlung der Hepatitis C bei chronischer Nierenkrankheit.[83]
- Diagnose, Evaluation, Vorbeugung und Behandlung von Störungen des Mineral- und Knochenstoffwechsels bei chronischer Nierenkrankheit.[52]
- Betreuung des nierentransplantierten Patienten.[84]
Die European Renal Association (Europäische Nieren-Vereinigung) hat Leitlinien veröffentlicht zum Anämie-Management, zur Hämodialyse und zur Nierentransplantation.
Die Leitlinien der Canadian Society of Nephrology (Kanadische Gesellschaft für Nephrologie) beschäftigen sich mit Prinzipien der Behandlung des Terminalstadiums einer Nierenkrankheit, mit der Überweisung vom Allgemeinmediziner zum Nephrologen, sowie mit Hämodialyse, Peritonealdialyse, Gefäßzugang, Dialysebeginn und Anämie-Management.
Die britischen Leitlinien des Royal College of Physicians in Zusammenarbeit mit der britischen Nierenvereinigung wurden 2005 publiziert und 2008 aktualisiert. Es werden Maßnahmen zur Erkennung und zum Management von Nierenkrankheiten, sowie Kriterien zur Überweisung zum Spezialisten vorgeschlagen.
Die Leitlinien der Nephrologischen Gesellschaft von Australien und Neuseeland werden seit 2000 veröffentlicht. Sie umfassen Diagnostik, Vorbeugung und Behandlung von chronischer Nierenkrankheit, Dialyse und Nierentransplantation.
In der Datenbank der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften finden sich Leitlinien zur diabetischen Nephropathie, zur urämischen Polyneuropathie sowie zur Nierentransplantation aus urologischer Sicht. Deutschsprachige Leitlinien zur chronischen Nierenkrankheit fehlen.
Selbsthilfeorganisationen
In Deutschland gibt es eine große Anzahl von lokalen Selbsthilfegruppen, die sich insbesondere für Dialysepatienten und Nierentransplantierte einsetzen.
Viele dieser Gruppen sind im "Bundesverband Niere - Selbsthilfe Niere -Prävention, Dialyse, Transplantation- e.V." zusammengeschlossen. Ziele des Vereins sind u. a.
- die Förderung der Organspendebereitschaft in der Öffentlichkeit,
- die Prävention von Nierenerkrankungen,
- der Einsatz für das Qualitätsmanagement in der Nierenersatztherapie,
- die Wahrnehmung der Interessen der Mitglieder der ihm angeschlossenen Mitgliedervereine.
Der Bundesverband Niere gibt die Zeitschrift "Der Nierenpatient" heraus.
Das "Netzwerk von Menschen mit chronischen Nierenerkrankungen und deren Angehörige c/o Heimdialyse-Patienten (HDP) e.V." hat insbesondere die Förderung von Heimdialyseverfahren wie Bauchfelldialyse oder Heimhämodialyse zum Ziel.
Die "PKD Familiäre Zystennieren e.V." richtet sich an Patienten mit Zystennieren und deren Familienangehörige und ist Teil eines internationalen Netzwerkes von Zystennierenpatienten.
Ziele der Selbsthilfegruppe sind Selbsthilfe - Prävention - Forschung, u.a.
- die medizinische Aufklärung mit Hilfe von Ärzten,
- Gespräche mit Betroffenen und deren Familienangehörigen,
- persönlicher Erfahrungsaustausch,
- Hilfe bei auftretenden Problemen,
- Fachvorträge zu krankheitstangierenden Themen,
- gemeinsame Freizeitaktivitäten,
- Kontaktstelle für Eltern mit erkrankten Kindern.
Der Verein "Junge Nierenkranke Deutschlands e.V." vertritt die Interessen junger nierenkranker Menschen. Er richtet sich speziell an Jugendliche und junge Erwachsene, die von einer Nierenerkrankung betroffen sind. Unter anderem bietet der Verein Veranstaltungen, Seminare und Reisen an, die auch für dialysepflichtige Nierenkranke geeignet sind und berät und unterstützt bei Problemen im sozialen, beruflichen und schulischen Umfeld.
Chronisches Nierenversagen in der Tiermedizin
In der Tiermedizin kommt chronisches Nierenversagen am häufigsten bei Hauskatzen vor und ist eine der häufigsten Todesursachen für diese Tierart (→ Chronische Niereninsuffizienz der Katze).
Weblinks
- Kidney Disease: Improving Global Outcomes - Internationales Leitlinienportal (engl.)
- German Chronic Kidney Disease - GCKD Studie Nationale Kohortenstudie zu chronischer Nierenerkrankung
- www.dosing.de - Medikamentendosierung bei Niereninsuffizienz, Universitätsklinikum Heidelberg, Abteilung Innere Medizin VI, Klinische Pharmakologie und Pharmakoepidemiologie
- Hartmann, Bertram; Czock, David; Keller, Frieder: Arzneimitteltherapie bei Patienten mit chronischem Nierenversagen. In: Dtsch Arztebl Int. Nr. 107(37), 2010, S. 647-656 (Artikel).
- KDOQI-Clinical Practice Guidelines - Leitlinien der Nationalen Nierenstiftung der USA (engl.)
- Chronic kidney disease - Leitlinie des Royal College of Physicians (UK), September 2008. Volltext PDF Anhänge PDF (engl.)
- Chronisches Nierenversagen im Alter: Online Geriatric Nephrology Curriculum der American Society of Nephrology (engl.)
Quellenangaben
- ↑ Lysaght MJ: Maintenance Dialysis Population Dynamics: Current Trends and Long-Term Implications. J Am Soc Nephrol 13:S37-S40, 2002
- ↑ KIDNEY DISEASE: COMMON, HARMFUL, TREATABLE World Kidney Day, a joint initiative of the International Society of Nephrology (ISN) and the International Federation of Kidney Foundations (IFKF). [1]
- ↑ K/DOQI Clinical Practice Guidelines for Chronic Kidney Disease: Evaluation, Classification, and Stratification. American Journal of Kidney Diseases, 2002 Feb;39 (2, Sup) [2]
- ↑ Richard J MacIsaac, et al.: Nonalbuminuric renal insufficiency in type 2 diabetes. In: Diabetes Care. 27, Nr. 1, 2004-01, S. 195-200. PMID 14693989. Abgerufen am 18. Januar 2010.
- ↑ Andrew S Levey, Lesley A Stevens, Josef Coresh: Conceptual model of CKD: applications and implications. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 53, Nr. 3 Suppl 3, 2009-03, S. S4-16. doi:10.1053/j.ajkd.2008.07.048. PMID 19231760. Abgerufen am 25. September 2009.
- ↑ Hemmelgarn BR et al.: Relation Between Kidney Function, Proteinuria, and Adverse Outcomes.. In: JAMA. Nr. Feb 3;303(5), 2010, S. 423-429 (ArtikelAbstract).
- ↑ Andrew S Levey, Lesley A Stevens, Josef Coresh: Conceptual model of CKD: applications and implications. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 53, Nr. 3 Suppl 3, 2009-03, S. S4-16. doi:10.1053/j.ajkd.2008.07.048. PMID 19231760. Abgerufen am 23. Juli 2009.
- ↑ Carolyn Bauer, Michal L Melamed, Thomas H Hostetter: Staging of chronic kidney disease: time for a course correction. In: Journal of the American Society of Nephrology: JASN. 19, Nr. 5, 2008-05, S. 844-846. doi:10.1681/ASN.2008010110. PMID 18385419. Abgerufen am 23. Juli 2009.
- ↑ Christopher G Winearls, Richard J Glassock: Dissecting and refining the staging of chronic kidney disease. In: Kidney International. 75, Nr. 10, 2009-05, S. 1009-1014. doi:10.1038/ki.2009.49. PMID 19242501. Abgerufen am 23. Juli 2009.
- ↑ Garabed Eknoyan: Chronic kidney disease definition and classification: no need for a rush to judgment. In: Kidney International. 75, Nr. 10, 2009-05, S. 1015-1018. doi:10.1038/ki.2009.53. PMID 19262459. Abgerufen am 23. Juli 2009.
- ↑ Kai-Uwe Eckardt, Jeffrey S Berns, Michael V Rocco, Bertram L Kasiske: Definition and classification of CKD: the debate should be about patient prognosis--a position statement from KDOQI and KDIGO. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 53, Nr. 6, 2009-06, S. 915-920. doi:10.1053/j.ajkd.2009.04.001. PMID 19406541. Abgerufen am 23. Juli 2009. Artikel, PDF
- ↑ KDIGO Controversies Conference: Definition, Classification and Prognosis in CKD, London, October 2009
- ↑ Frei, U., Schober-Halstenberg, H.-J.: Nierenersatztherapie in Deutschland. QuaSi-Niere Jahresberichte 1995 bis 2005/2006, Berlin, Deutschland. Die Daten wurden von QuaSi-Niere gGmbH zur Verfügung gestellt. Eine Interpretation und die weiterführende Auswertung dieser Daten liegen allein in der Verantwortung des Autors.[3]
- ↑ I.M. Wahba et. al.: Obesity and Obesity-Initiated Metabolic Syndrome: Mechanistic Links to Chronic Kidney Disease Clin J Am Soc Nephrol 2007 2: 550-562[4]
- ↑ Ron Wald, et al.: Chronic dialysis and death among survivors of acute kidney injury requiring dialysis. In: JAMA: The Journal of the American Medical Association. 302, Nr. 11, 2009-09-16, S. 1179-1185. doi:10.1001/jama.2009.1322. Abgerufen am 7. Dezember 2010.
- ↑ Lowell J Lo, et al.: Dialysis-requiring acute renal failure increases the risk of progressive chronic kidney disease. In: Kidney International. 76, Nr. 8, 2009-10, S. 893-899. doi:10.1038/ki.2009.289. Abgerufen am 7. Dezember 2010.
- ↑ Areef Ishani, et al.: Acute kidney injury increases risk of ESRD among elderly. In: Journal of the American Society of Nephrology: JASN. 20, Nr. 1, 2009-01, S. 223-228. doi:10.1681/ASN.2007080837. Abgerufen am 7. Dezember 2010.
- ↑ Abbildung: Prävalenz der chronischen Nierenkrankheit nach Alter NHANES 1988-1994 und 1999-2004 JAMA 2007;298(17):2038-2047
- ↑ Allan J Collins, et. al: Who should be targeted for CKD screening? Impact of diabetes, hypertension, and cardiovascular disease. In: American Journal of Kidney Diseases. 53, Nr. 3 Suppl 3, 2009-03, S. S71-77. doi:10.1053/j.ajkd.2008.07.057. Abgerufen am 15. Mai 2010.
- ↑ Josef Coresh, Elizabeth Selvin, Lesley A Stevens, Jane Manzi, John W Kusek, Paul Eggers, Frederick Van Lente, Andrew S Levey: Prevalence of chronic kidney disease in the United States. In: JAMA: The Journal of the American Medical Association. 298, Nr. 17, 2007-11-07, S. 2038-2047. doi:10.1001/jama.298.17.2038. PMID 17986697. Abgerufen am 23. Juli 2009.
- ↑ Mitchell Rosner, Emaad Abdel-Rahman, Mark E Williams: Geriatric nephrology: responding to a growing challenge. In: Clinical Journal of the American Society of Nephrology: CJASN. 5, Nr. 5, 2010-05, S. 936-942. doi:10.2215/CJN.08731209. Abgerufen am 21. August 2010.
- ↑ A. S. Go, et al.: Chronic Kidney Disease and the Risks of Death, Cardiovascular Events, and Hospitalization. N. Engl. J. Med. 351:1296-1305 (2004)[5]
- ↑ Manjula Kurella Tamura, Virginia Wadley, et al.: Kidney function and cognitive impairment in US adults: the Reasons for Geographic and Racial Differences in Stroke (REGARDS) Study. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 52, Nr. 2, 2008-08, S. 227-34. doi:10.1053/j.ajkd.2008.05.004. PMID 18585836. Abgerufen am 8. November 2008.
- ↑ Minesh Khatri, et al.: CKD associates with cognitive decline. In: Journal of the American Society of Nephrology: JASN. 20, Nr. 11, 2009-11, S. 2427-2432. doi:10.1681/ASN.2008101090. Abgerufen am 24. Juli 2010.
- ↑ Gerald Liew, Paul Mitchell, Tien Yin Wong, Sudha K Iyengar, Jie Jin Wang: CKD increases the risk of age-related macular degeneration. In: Journal of the American Society of Nephrology: JASN. 19, Nr. 4, 2008-04, S. 806-11. doi:10.1681/ASN.2007080844. PMID 18216312. Abgerufen am 8. November 2008.
- ↑ Matthew T James, et al.: CKD and risk of hospitalization and death with pneumonia. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 54, Nr. 1, 2009-07, S. 24-32. doi:10.1053/j.ajkd.2009.04.005. PMID 19447535. Abgerufen am 13. Januar 2010.
- ↑ Annamaria Kausz, Dilip Pahari: The value of vaccination in chronic kidney disease. In: Seminars in Dialysis. 17, Nr. 1, 2004-02, S. 9-11. PMID 14717802. Abgerufen am 13. Januar 2010.
- ↑ C Y Hsun et al.: The risk of acute renal failure in patients with chronic kidney disease. In: Kidney Int. Nr. 74, 2008, S. 101-107 (Abstract).
- ↑ D. S. Keith, et al.. Longitudinal Follow-up and Outcomes Among a Population With Chronic Kidney Disease in a Large Managed Care Organization. Arch Intern Med. 2004;164:659-663 [6]
- ↑ Allan J Collins, Robert N Foley, David T Gilbertson, Shu-Chen Chen: The state of chronic kidney disease, ESRD, and morbidity and mortality in the first year of dialysis. In: Clinical Journal of the American Society of Nephrology: CJASN. 4 Suppl 1, 2009-12, S. S5-11. doi:10.2215/CJN.05980809. PMID 19996006. Abgerufen am 19. Januar 2010.
- ↑ Grenzwert der GFR, ab dem die Wahrscheinlichkeit, dialysepflichtig zu werden, die Wahrscheinlichkeit, zuvor zu sterben, übersteigt; nach Altersgruppen aus Ann M. O'Hare, et al.: Age Affects Outcomes in Chronic Kidney Disease. In: J Am Soc Nephrol. 18, Nr. 10, 2007-10-01, S. 2758-2765. doi:10.1681/ASN.2007040422. Abgerufen am 29. September 2010.
- ↑ M. Tonelli et. al.: Chronic Kidney Disease and Mortality Risk: A Systematic Review J Am Soc Nephrol 2006 17: 2034-2047[7]
- ↑ Kunihiro Matsushita, et al.: Association of estimated glomerular filtration rate and albuminuria with all-cause and cardiovascular mortality in general population cohorts: a collaborative meta-analysis. In: Lancet. 375, Nr. 9731, 2010-06-12, S. 2073-2081. doi:10.1016/S0140-6736(10)60674-5. Abgerufen am 11. September 2010.
- ↑ Roberts MA, et. al: Cardiovascular Biomarkers in CKD: Pathophysiology and Implications for Clinical Management of Cardiac Disease American Journal of Kidney Diseases 48, 341-360 (2006)[8]
- ↑ Brewster U. C. et al.: Dermatological Disease in Patients With CKD. In: American Journal of Kidney Diseases. Nr. 51, 2008, S. 331-344 (Artikel).
- ↑ Stadienabhängige Behandlungspläre für chronisch Nierenkranke unter www.kidney.org: [9]
- ↑ A.K. Bello et al.: Prevention of chronic kidney disease. A global challenge. In: Kidney International. Nr. 68, Supplement 98, 2005, S. S11–S17 (Artikel).
- ↑ E. Imai et al.: Kidney Disease Screening Program in Japan. History, Outcome, and Perspectives. In: Clin J Am Soc Nephrol. Nr. 2, 2007, S. 1360-1366 (Abstract).
- ↑ Orth, Stephan R., Hallan, Stein I.: Smoking: A Risk Factor for Progression of Chronic Kidney Disease and for Cardiovascular Morbidity and Mortality in Renal Patients Absence of Evidence or Evidence of Absence?. In: Clin J Am Soc Nephrol. Nr. 3, 2008, S. 226-236 (Abstract).
- ↑ U.O. Wenzel et. al: My Doctor Said I Should Drink a Lot! Recommendations for Fluid Intake in Patients with Chronic Kidney Disease. In: Clin J Am Soc Nephrol. Nr. 1, 2006, S. 344-346 (Artikel).
- ↑ K/DOQI Clinical Practice Guidelines on Hypertension and Antihypertensive Agents in Chronic Kidney Disease American Jounal of Kidney Diseases, 2004; 43:5(Suppl 1):S1 [10]
- ↑ Lawrence J Appel, et al.: Intensive blood-pressure control in hypertensive chronic kidney disease. In: The New England Journal of Medicine. 363, Nr. 10, 2010-09-02, S. 918-929. doi:10.1056/NEJMoa0910975. Abgerufen am 9. September 2010.
- ↑ D.M. Kent et al.: Progression Risk, Urinary Protein Excretion, and Treatment Effects of Angiotensin-Converting Enzyme Inhibitors in Nondiabetic Kidney Disease J Am Soc Nephrol 2007 18: 1959-1965[11]
- ↑ MacKinnon M, et al.: Combination Therapy With an Angiotensin Receptor Blocker and an ACE Inhibitor in Proteinuric Renal Disease: A Systematic Review of the Efficacy and Safety Data American Journal of Kidney Diseases, 2006; 48: 8-20[12]
- ↑ Roland E. Schmieder et. al. Additional Antiproteinuric Effect of Ultrahigh Dose Candesartan: A Double-Blind, Randomized, Prospective Study J Am Soc Nephrol 16: 3038–3045, 2005[13]
- ↑ Leszek Tylicki, et al.: Triple pharmacological blockade of the renin-angiotensin-aldosterone system in nondiabetic CKD: an open-label crossover randomized controlled trial. In: American Journal of Kidney Diseases. 52, Nr. 3, 2008-09, S. 486-93. doi:S0272-6386(08)00467-8. PMID 18423812. Abgerufen am 1. Dezember 2008.
- ↑ Fausta Catapano, Paolo Chiodini, Luca De Nicola, Roberto Minutolo, Pasquale Zamboli, Ciro Gallo, Giuseppe Conte: Antiproteinuric response to dual blockade of the renin-angiotensin system in primary glomerulonephritis: meta-analysis and metaregression. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 52, Nr. 3, 2008-09, S. 475-85. doi:S0272-6386(08)00582-9. PMID 18468748. Abgerufen am 1. Dezember 2008.
- ↑ Salim Yusuf, et al.: Telmisartan, ramipril, or both in patients at high risk for vascular events. In: The New England Journal of Medicine. 358, Nr. 15, 2008-04-10, S. 1547-59. doi:NEJMoa0801317. PMID 18378520. Abgerufen am 3. Dezember 2008.
- ↑ Bruno Cianciaruso, et al.: Effect of a low- versus moderate-protein diet on progression of CKD: follow-up of a randomized controlled trial. In: American Journal of Kidney Diseases: The Official Journal of the National Kidney Foundation. 54, Nr. 6, 2009-12, S. 1052-1061. doi:10.1053/j.ajkd.2009.07.021. Abgerufen am 11. Dezember 2010.
- ↑ Shepherd, J. et al.: Effect of Intensive Lipid Lowering with Atorvastatin on Renal Function in Patients with Coronary Heart Disease: The Treating to New Targets (TNT) Study. In: Clin J Am Soc Nephrol. Nr. 2, 2007, S. 1131-1139 (Abstract).
- ↑ a b Ione de Brito-Ashurst, Mira Varagunam, Martin J Raftery, Muhammad M Yaqoob: Bicarbonate supplementation slows progression of CKD and improves nutritional status. In: Journal of the American Society of Nephrology: JASN. 20, Nr. 9, 2009-09, S. 2075-2084. doi:10.1681/ASN.2008111205. PMID 19608703. Abgerufen am 14. Januar 2010.
- ↑ a b c Improving Global Outcomes (KDIGO) CKD-MBD Work Group: KDIGO clinical practice guideline for the diagnosis, evaluation, prevention, and treatment of chronic kidney disease–mineral and bone disorder (CKD–MBD).. In: Kidney International. Nr. 76 (Suppl 113), 2009, S. S1–S130 (PDF). Deutsche Übersetzung
- ↑ Steven M. Brunelli: The Association between Prescribed Dietary Phosphate Restriction and Mortality among Hemodialysis Patients. In: CJASN. Nr. December 2010, 2011 (Artikel).
- ↑ K/DOQI Clinical Practice Guidelines for Bone Metabolism and Disease in Chronic Kidney Disease American Journal of Kidney Diseases, 2003: 42 Supplement 3[14]
- ↑ KDOQI Clinical Practice Guidelines and Clinical Practice Recommendations for Anemia in Chronic Kidney Disease American Journal of Kidney Diseases, 2006: 47 Supplement S3 [15]
- ↑ KDOQI Clinical Practice Guideline and Clinical Practice Recommendations for Anemia in Chronic Kidney Disease: 2007 Update of Hemoglobin Target American Journal of Kidney Diseases, 2007: 50, pp 522-528 [16]
- ↑ Drüeke TB et. al. Normalization of hemoglobin level in patients with chronic kidney disease and anemia. N Engl J Med 2006;355:2071-2084. [17]
- ↑ Singh AK et. al. Correction of anemia with epoetin alfa in chronic kidney disease. N Engl J Med 2006;355:2085-2098. [18]
- ↑ Marc A Pfeffer, et al.: A trial of darbepoetin alfa in type 2 diabetes and chronic kidney disease. In: The New England Journal of Medicine. 361, Nr. 21, 2009-11-19, S. 2019-2032. doi:10.1056/NEJMoa0907845. PMID 19880844. Abgerufen am 11. Januar 2010.
- ↑ Suetonia C Palmer, et al.: Meta-analysis: erythropoiesis-stimulating agents in patients with chronic kidney disease. In: Annals of Internal Medicine. 153, Nr. 1, 2010-07-06, S. 23-33. doi:10.1059/0003-4819-153-1-201007060-00252. Abgerufen am 21. September 2010.
- ↑ Fishbane, S. Besarab, A.: Mechanism of Increased Mortality Risk with Erythropoietin Treatment to Higher Hemoglobin Targets. In: Clin J Am Soc Nephrol. Nr. 2, 2007, S. 1274-1282 (Abstract).
- ↑ Kottgen, Anna et al.: Reduced Kidney Function as a Risk Factor for Incident Heart Failure: The Atherosclerosis Risk in Communities (ARIC) Study. In: J Am Soc Nephrol. Nr. 18, 2007, S. 1307-1315 (Artikel).
- ↑ Meng Lee, et al.: Low glomerular filtration rate and risk of stroke: meta-analysis. In: BMJ (Clinical Research Ed.). 341, 2010, S. c4249. Abgerufen am 5. Januar 2011.
- ↑ K/DOQI Clinical Practice Guidelines for Managing Dyslipidemias in Chronic Kidney Disease American Journal of Kidney Diseases, 2003: 41 Supplement S3 [19]
- ↑ Molitch M. E., Management of Dyslipidemias in Patients with Diabetes and Chronic Kidney Disease Clin J Am Soc Nephrol 2006 1: 1090-1099 [20]
- ↑ National Heart, Lung and Blood Institute: Third Report of the Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) [21]
- ↑ Nogueira, Joseph, Weir, Matthew: The Unique Character of Cardiovascular Disease in Chronic Kidney Disease and Its Implications for Treatment with Lipid-Lowering Drugs. In: Clin J Am Soc Nephrol. Nr. 2, 2007, S. 766-785 (Artikel).
- ↑ Marcello Tonelli et al.: Effect of Pravastatin on Cardiovascular Events in People With Chronic Kidney Disease. In: Circulation. Nr. 110, 2004, S. 1557-1563 (Artikel).
- ↑ Michael J. Koren et al.: Focused Atorvastatin Therapy in Managed-Care Patients With Coronary Heart Disease and CKD. In: American Journal of Kidney Diseases. Nr. Vol. 53, Issue 5, 2009, S. 741-750 (Abstract).
- ↑ Wanner C., et. al. the German Diabetes and Dialysis Study Investigators Atorvastatin in Patients with Type 2 Diabetes Mellitus Undergoing Hemodialysis N Engl J Med 2005; 353:238-248 [22]
- ↑ Kwan, Bonnie C.H. et al.: Lipoprotein Metabolism and Lipid Management in Chronic Kidney Disease. In: J Am Soc Nephrol. Nr. 18, 2007, S. 1246-1261 (Artikel).
- ↑ R.D. Kilpatrick et al.: Association between Serum Lipids and Survival in Hemodialysis Patients and Impact of Race. In: J Am Soc Nephrol. Nr. 18, 2007, S. 293-303 (Artikel).
- ↑ C. P. Kovesdy et. al: Inverse Association between Lipid Levels and Mortality in Men with Chronic Kidney Disease Who Are Not Yet on Dialysis: Effects of Case Mix and the Malnutrition-Inflammation-Cachexia Syndrome. In: J Am Soc Nephrol. Nr. 18, 2007, S. 304-311 (Artikel).
- ↑ Homepage der SHARP-Studie
- ↑ Sarnak M. J., et. al.: Kidney Disease as a Risk Factor for Development of Cardiovascular Disease: A Statement From the American Heart Association Councils on Kidney in Cardiovascular Disease, High Blood Pressure Research, Clinical Cardiology, and Epidemiology and Prevention Circulation 2003; 108: 2154-2169 [23]
- ↑ NKF K/DOQI GUIDELINES: Clinical Practice Guidelines and Clinical Practice Recommendations, 2006 Updates, Hemodialysis Adequacy, Peritoneal Dialysis Adequacy, Vascular Access American Journal of Kidney Diseases, 2006: 48 Supplement S1[24]
- ↑ Bruce A Cooper, et. al: A Randomized, Controlled Trial of Early versus Late Initiation of Dialysis. In: The New England Journal of Medicine. 2010-06-27. doi:10.1056/NEJMoa1000552. Abgerufen am 2. Juli 2010.
- ↑ Seth Wright, et al.: Timing of dialysis initiation and survival in ESRD. In: Clinical Journal of the American Society of Nephrology: CJASN. 5, Nr. 10, 2010-10, S. 1828-1835. doi:10.2215/CJN.06230909. Abgerufen am 5. Juli 2011.
- ↑ Rachel C. Carson, Maciej Juszczak, Andrew Davenport, Aine Burns: Is Maximum Conservative Management an Equivalent Treatment Option to Dialysis for Elderly Patients with Significant Comorbid Disease?. In: Clin J Am Soc Nephrol. 4, Nr. 10, 2009-10-01, S. 1611-1619. doi:10.2215/CJN.00510109. Abgerufen am 6. Februar 2010.
- ↑ Manjula Kurella Tamura, Kenneth E Covinsky, Glenn M Chertow, Kristine Yaffe, C Seth Landefeld, Charles E McCulloch: Functional status of elderly adults before and after initiation of dialysis. In: The New England Journal of Medicine. 361, Nr. 16, 2009-10-15, S. 1539-1547. doi:10.1056/NEJMoa0904655. PMID 19828531. Abgerufen am 28. November 2009.
- ↑ Vincenzo De Biase, Olga Tobaldini, Claudia Boaretti, Cataldo Abaterusso, Nicoletta Pertica, Carmelo Loschiavo, Gaetano Trabucco, Antonio Lupo, Giovanni Gambaro: Prolonged conservative treatment for frail elderly patients with end-stage renal disease: the Verona experience. In: Nephrology, Dialysis, Transplantation: Official Publication of the European Dialysis and Transplant Association - European Renal Association. 23, Nr. 4, 2008-04, S. 1313-1317. doi:10.1093/ndt/gfm772. PMID 18029376. Abgerufen am 28. November 2009.
- ↑ Kidney Disease: Improving Global Outcomes (KDIGO) Homepage
- ↑ KDIGO clinical practice guidelines for the prevention, diagnosis, evaluation, and treatment of hepatitis C in chronic kidney disease. In: Kidney International. Supplement. Nr. 109, 2008-04, S. S1-99. doi:10.1038/ki.2008.81. PMID 18382440. Abgerufen am 20. Januar 2010. PDF
- ↑ KDIGO clinical practice guideline for the care of kidney transplant recipients. In: American Journal of Transplantation: Official Journal of the American Society of Transplantation and the American Society of Transplant Surgeons. 9 Suppl 3, 2009-11, S. S1-155. doi:10.1111/j.1600-6143.2009.02834.x. PMID 19845597. Abgerufen am 20. Januar 2010. PDF

Bitte den Hinweis zu Gesundheitsthemen beachten! Kategorie:- Krankheitsbild in der Nephrologie
Wikimedia Foundation.