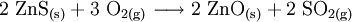- Pigment Weiß 4
-
Kristallstruktur 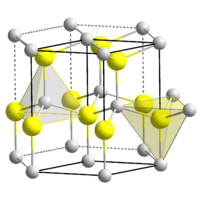
__ Zn2+ __ O2- Allgemeines Name Zinkoxid Andere Namen - Zink(II)-oxid
- Zinci oxidum
- Zinkweiß
- Chinesischweiß
- C.I. 77947
- Pigment Weiß 4
Verhältnisformel ZnO CAS-Nummer 1314-13-2 ATC-Code D02AB
Kurzbeschreibung weißer bis gelblicher pulverförmiger Feststoff Eigenschaften Molare Masse 81,39 g·mol−1 Aggregatzustand fest
Dichte Schmelzpunkt Löslichkeit Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 
Umwelt-
gefährlich(N) R- und S-Sätze R: 50/53 S: 60-61 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln MAK 1 mg·m−3[1]
WGK 2 – wassergefährdend[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Zinkoxid (ZnO) ist eine chemische Verbindung aus Zink und Sauerstoff, die einerseits farblose, hexagonale Kristalle bildet oder andererseits, aufgrund der Lichtbrechung bei sehr kleinen Kristallen, als lockeres, weißes Pulver vorliegt.
Die traditionelle Bezeichnung Zinkweiß (Chinesischweiß, Ewigweiß, Schneeweiß) stammt von der Verwendung als weißes Farbmittel in Malerfarbe.
Medizinische Präparate zur Haut- und Wundbehandlung enthalten oft Zinkoxid wegen dessen antiseptischer Wirkung. Es wird häufig in der Zahnheilkunde (z. B. bei Wurzelkanalbehandlungen) eingesetzt und gilt als Biomaterial.
Inhaltsverzeichnis
Vorkommen
Mineralische Vorkommen von Zinkoxid sind in Form von grobkörnigem Rotzinkerz (Zinkit) zu finden.
Gewinnung und Darstellung
Je nach Herstellungsverfahren gewinnt man Zinkweiß oder Zinkoxid. Zinkweiß wird nach dem so genannten französischen Verfahren aus Zinkdampf und Luftsauerstoff hergestellt.
Zinkoxid dagegen gewinnt man entweder aus der Durchführung der Herstellung nach dem so genannten amerikanischen Verfahren aus Zinkerzen oder -Schrott durch Röstung, durch Reduktion mit Kohle und direkte anschließende Reoxidation oder nasschemisch durch Fällung als Hydroxid oder Carbonat aus Zinksalzlösungen und anschließende Calcination.
Zinkoxid entsteht durch die Verbrennung von Zink. Dabei kann sich das Oxid in feinfilziger, wollartiger Form (Lana philosophia) bilden.
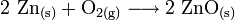
- Zink verbrennt bei Anwesenheit von Sauerstoff zu Zinkoxid.
Es kann aber auch durch Glühen (Pyrolyse) von Zinkhydroxid, Zinkcarbonat oder Zinknitrat gewonnen werden:
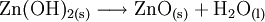
- Bei höheren Temperaturen gibt Zinkhydroxid Wasser ab. Es entsteht Zinkoxid.
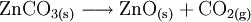
- Aus Zinkcarbonat entstehen beim Glühen Zinkoxid und Kohlenstoffdioxid.
Beim Rösten von Zinksulfid entsteht ebenfalls Zinkoxid:
Je nach Anwendungsbereich kann durch variieren der Reaktionsbedingungen Zinkoxid in unterschiedlichen Qualitäten hergestellt werden. Industriell produzierte Zinkoxidpigmente sind häufig bleihaltig und somit zusätzlich mit dem Gefahrensymbol Xn (gesundheitsschädlich) zu kennzeichnen.
Dünne Schichten von Zinkoxid stellt man durch physikalische Abscheideverfahren (PVD) wie Sputtern und Chemische Gasphasenabscheidung (CVD) her. CVD ermöglicht die Entstehung rauher Oberflächen, die sich dadurch auszeichnen, einfallendes Licht zu streuen und z. B. Solarzellen einen höheren Wirkungsgrad zu verleihen.
Eigenschaften
Zinkoxid verdunstet ab ca. 1300 °C, der Sublimationspunkt unter Normaldruck liegt bei etwa 1800 °C. Ein Schmelzen von Zinkoxid ist erst unter erhöhtem Druck bei 1975 °C zu beobachten. Beim Erhitzen färbt es sich zitronengelb, nach Abkühlen ist es wieder weiß (siehe Thermochromie). Im Dunkeln kann man anschließend ein schwaches Nachleuchten beobachten. Die Farbänderung ist auf einen geringen, durch Sauerstoffabgabe beim Erhitzen entstehenden Zinküberschuss (etwa 0,03 %) zurückzuführen.
Die Verbindung absorbiert ultraviolette Strahlung. Nur geringste Verunreinigungen bewirken, dass sie auch im sichtbaren Bereich des elektromagnetischen Spektrums Absorption zeigt und somit farbig erscheint.
Zinkoxid ist ein direkter Halbleiter mit einer Bandlücke von 3,2–3,4 Elektronenvolt. N-dotierte, z. B. Aluminium oder Sauerstoff-Defekte enthaltende dünne Schichten dieses Materials sind transparent und elektrisch leitend, sowie piezoelektrisch.
Zinkoxid ist in Wasser unlöslich, während verdünnte Säuren es unter Salzbildung lösen. Mit Alkali wie z. B. Natronlauge frisch gefälltes, hydratisiertes Zinkoxid löst sich bei einem Überschuss an Base wieder auf. Dabei entsteht ein lösliches Zinkat.
Wird die Verbindung mit Cobalt(II)-oxid (CoO) erhitzt, so entsteht eine grüne feste Lösung von Cobalt in Zinkoxid (Rinmanns Grün).
Reines Zinkoxid ist ungiftig.
Verwendung
Zinkoxid wird unter der Bezeichnung Zinkweiß als Pigment genutzt. Daneben findet man auch Bezeichnungen wie Chinesischweiß, Ewigweiß oder Schneeweiß. Im Gegensatz zu Bleiweiß-Anstrichen ist es schwefelwasserstoff- und lichtbeständig, aber weniger deckend. Daher wurden als Malerfarbe oft Mischungen aus Blei- und Zinkweiß verwendet. Zinkweiß ist mit allen Pigmenten gut verträglich. Alkalische Bindemittel sollten aber vermieden werden, da die Gefahr einer Zinkatbildung besteht. In Öl können sich begrenzt Zinkseifen bilden. Zinkweiß wurde vielfach in wässrigen Techniken eingesetzt, wie z. B. in Leim-, Aquarell- und Gouachefarben. Es war im Altertum bereits unter Cadmea und Porerpholyx bekannt. Die Alchimisten nannten es Nix alba. 1782 ersetzte Courtois in Dijon Blei- durch Zinkweiß, 1840 wurde es kommerziell zu Ölfarben verarbeitet. Seit 1834 gibt es Zinkweiß auch als Wasserfarbe. Zinkweiß wurde erst langsam von den Künstlern als Ersatz für Bleiweiß angenommen. Es gab regelrechte Streitereien über seine Verwendung. Da Zinkweiß einfach kühler wirkt, wurde es schließlich hauptsächlich für die Mischung mit kühlen Farbtönen verwendet, während Bleiweiß mit den wärmeren Farben vermischt wurde. Die Verwendung von Zinkweiß als Deckfarbe geht heute mehr und mehr zugunsten derer von Titanweiß zurück. Seit 1888 wird Zinkoxid auch in Deodorants verwendet, da es leicht antibakteriell wirkt.
Als Bestandteil pharmazeutischer Zinksalben, -pasten, -pflaster (Leukoplast) und -verbänden sowie Sonnenschutzmitteln und als Zusatz bei der Vulkanisation von Kautschuk findet Zinkoxid Verwendung. Zudem kommt es als Luminophor in Leuchtstofflampen zum Einsatz.
Forscher des schweizer Paul-Scherrer-Instituts in Villigen versuchen, die Sonnenkraft in chemische Energie umzusetzen. Sie fokussieren dazu Sonnenstrahlen auf einen Schmelztiegel. Das Licht trifft bei über 1200 °C auf Zinkoxid, das daraufhin verdampft und zu metallischem Zink umgewandelt wird, wenn dafür gesorgt wird, dass das entstehende Zink nicht sofort wieder oxidiert. Da dieses gelagert und transportiert werden kann, lässt sich so die Energie der Sonne speichern und später z. B. in Zink-Luft-Batterien direkt als elektrische Energie oder zur Produktion von Wasserstoff nutzen. Das ist vereinfacht dargestellt, denn aus den Zink-Luft-Batterien wird das entladenen Zn- ZnO zusammen mit KOH entnommen.
Als Halbleiter findet Zinkoxid Verwendung als durchsichtige leitende Schicht bei der Herstellung blauer Leuchtdioden (LED), von Flüssigkristallbildschirmen (TFT), Varistoren (VDR) und Dünnschicht-Solarzellen. Hierzu wird es meist mit Aluminium dotiert ZnO:Al, (AZO =Aluminium Zink Oxide). Die Dotierung erhöht die Leitfähigkeit um mehrere Größenordnungen. Als halbleitende Nanodrähte findet Zinkoxid in der Meßtechnik durch seine piezoelektrischen Eigenschaften und UV-Licht-Transparenz Anwendung[3].
Zinkoxid wird als DZO (Depleted Zinc Oxide) dem Kühlwasser von Kernreaktoren (Siedewasserreaktoren) beigegeben, um das Korrosionsverhalten der mit dem Kühlwasser in Berührung kommenden Komponenten zu verbessern.
Weblinks
Quellen
- ↑ a b c d e Eintrag zu Zinkoxid in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 11.11.2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 1314-13-2 im European chemical Substances Information System ESIS
- ↑ Synthesis of photoconducting ZnO nano-needles
Wikimedia Foundation.