- Hamburger Weiß
-
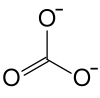
Strukturformel 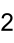
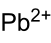
 ·
· 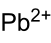
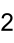
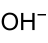
Allgemeines Name Bleiweiß Andere Namen - Basisches Bleicarbonat
- Cerussa
- Kremserweiß
- Hydrocerusit
- Tribleidicarbonatdihydroxid
Summenformel C2H2Pb3O8 CAS-Nummer 1319-46-6 Kurzbeschreibung weißes Pulver Eigenschaften Molare Masse 775,63 g/mol Aggregatzustand fest
Dichte 6,14 g/cm3[1]
Schmelzpunkt Zersetzung ab 400 °C[1]
Löslichkeit unlöslich in Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 61-20/22-33-62-50/53 S: 53-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Bleiweiß, 2 PbCO3 · Pb(OH)2, ist ein basisches Bleicarbonat und seit dem Altertum ein bedeutendes Weißpigment.
Inhaltsverzeichnis
Eigenschaften
Bleiweiß hat eine sehr hohe Deckkraft und abhängig vom Bindemittel einen schönen Glanz. Bleiweiß ist giftig.
Bleiweiß ist lichtbeständig. Allerdings dunkelt es nach, vor allem bei wässrigen Bindemitteln, was etwa bei Aquarellen stören kann. Dieses Nachdunkeln beruht auf der Bildung von tiefschwarzem Bleisulfid aus der Reaktion mit in Spuren allgegenwärtigem Schwefelwasserstoff. Deshalb ist es ungeeignet für schwefelhaltige Bindemittel sowie für alle schwefelhaltigen Buntpigmente (Ultramarin, Zinnober, Auripigment).
Die Giftigkeit von Bleiweiß war bereits in der Antike[3] bekannt. Von Frankreich ausgehend wurden ab Mitte des 19. Jahrhunderts die Pigmenteigenschaften von Zinkweiß erkannt. Seit dem Beginn des 20. Jahrhundert kam zunehmend Barytweiß als Weißpigment zum Einsatz, so dass das ursprünglich „einzige“ Bleiweiß an Bedeutung verlor.[4] Seit den 1960er-Jahre wird Titanweiß weltweit in großen Mengen produziert. In der Lack- und Kunststoffindustrie hat Bleiweiß keine Bedeutung mehr. Allerdings haben die chemischen und physikalischen Eigenschaften des Titanweiß gegenüber Bleiweiß-Künstlerfarben signifikante Nachteile.
Vorteile und Nachteile zu anderen Weißpigmenten
- Bleiweiß trocknet sehr schnell, während Titanweiß abhängig vom Bindemittel langsamer trocknet. Bleiverbindungen härten Firnisse.
- Buntmischungen mit Titanweiß ergeben kalte Töne. Die Remission von Bleiweiß sinkt bereits im sichtbaren (blauen) Bereich, es besitzt einen Gelbstich. Titanweiß remittiert bis in den ultravioletten Bereich hin fast völlig, deshalb wirkt es kalt. Bleiweiß dagegen lässt sich hervorragend mit anderen Malerfarben mischen.
- Bleiweiß ist wegen seiner Kristallstruktur ein weiches Pigment. Titanweiß ist dagegen (auch abhängig von der Kristallstruktur: Rutil oder Anatas) ein hartes Pigment (Mohs-Härte 6), es vermag trocken auch gehärteten Stahl zu ritzen. Somit lässt sich Bleiweiß besser ausreiben, zu feineren Korngrößen nachbearbeiten.
- TiO2 wechselt unter Lichteinwirkung zur Oxidationsstufe +III (Ti2O3), der freiwerdende atomare Sauerstoff greift Lackbindemittel an, dies führt zu schnellerem Abkreiden.
- Zinkweiß (ZnS ist weiß) kann ein universeller Ersatz für Bleiweiß sein. Barytweiß ist als Ersatz weniger geeignet. Im Gegensatz zu Bleiweiß und Zinkweiß unterscheidet sich der Brechungsindex von Barytweiß nur wenig von dem der meisten Bindemittel.
Bei Kreideweiß liegen die Werte noch näher, deshalb wird Kreide als Transparentweiß eingesetzt.
Herstellung
Bleiweiß ist ein künstlich hergestelltes Pigment. Als Mineral tritt es als Cerussit (ein Bleicarbonat) auf, wegen des Preises (auf Grund weniger Lagerstätten) wurde es nicht als Farbmittel eingesetzt.
In den antiken und mittelalterlichen Schriften wird die Herstellung wie folgt beschrieben: In ein Gefäß werden Bleiplatten oder Bleistücke zusammen mit einer Schale Essig gelegt und dann unter einem Misthaufen eingegraben. Das Blei ist somit den Essigdämpfen und Kohlenstoffdioxid ausgesetzt und wird durch die Fäulnisprozesse im Mist auf einer konstanten Temperatur gehalten. Nach einigen Wochen bildet sich dann auf den Bleiplatten eine weiße Substanz, das Bleiweiß.
In weiteren historischen Verfahren wird metallisches Blei ebenso der Einwirkung von Essigdämpfen und Kohlenstoffdioxid ausgesetzt. Ein Beispiel ist das holländische Loogenverfahren. Die Loogen sind Oxidationsräume, in denen bis zu zehn Tonnen Bleiplatten, eingepackt in Steinzeugtöpfe, die umgeben von Pferdemist und Lohe sind, für etwa vier Wochen der Einwirkung von Wärme, Essigsäure und Luft ausgesetzt sind. Das Bleiweiß wurde aus den Töpfen geschlämmt, getrocknet und gemahlen. In dem Klagenfurter Verfahren treten Weintrester, Bierhefe oder gärungsfähige Obstsäfte an die Stelle von Essig. Diese Herstellungsmethode verläuft langsamer, soll aber zu einem reiner weißen und besonders lockeren Produkt führen. Auf diese Weise ist das erste so genannte Kremserweiß hergestellt worden. Im Jahr 1839 wurde von Gustav Dietel in Eisenach zum ersten Mal das deutsche Kammerverfahren praktiziert. Dabei werden ca. ein Millimeter dünne, lange Bleilappen in großen gemauerten Räumen auf Holzgestelle gehängt und einer Atmosphäre von Luft, Kohlenstoffdioxid, Wasser- und Essigdämpfen in bestimmter Dosierung ausgesetzt. Das Blei wird zuerst chemisch in basisch-essigsaures Blei und später dann in basisches Bleicarbonat umgewandelt. Der Bleiweißschlamm wird dann gewaschen, gesiebt, getrocknet und gemahlen.
Heute wird Bleiweiß in einem Fällungsverfahren hergestellt, in dem in der Wärme eine Pb(II)-Salzlösung mit CO32- umgesetzt wird. Die Verfahren können im Meyers (erster Weblink) nachgelesen werden.
Verwendung
Als Farbmittel wurde Bleiweiß schon in der Antike verwendet und in der Funktion bereits von Theophrast im 4. Jahrhundert v. Chr. erwähnt. Auch Gaius Plinius Secundus (23-79 n. Chr.) erwähnt dieses Pigment. Es taucht ebenso in den mittelalterlichen Rezeptsammlungen des Lucca-Manuskriptes, der wenig veränderten Mappae Clavicula, bei Theophilus' und Heraclius' Schriften auf, in denen jeweils metallisches Blei und Essig als Ausgangsmaterial zur Herstellung von Bleiweiß dienten.
In der Antike bis ins Mittelalter wurde Bleiweiß der Schminke zugesetzt um die Haut aufzuhellen. Spätestens im 18. Jahrhundert setzte sich die Erkenntnis durch, dass diese Verwendung Gesundheitsprobleme (Zahnschmerzen, schlechter Atem) verursacht. Aufgrund dieser Giftigkeit war Bleiweiß auch ein hervorragender Holzanstrich.
Für Malfarben wurde es bevorzugt in der Öltechnik verwendet, bis ca. 1835 für Weißtöne fast ausschließlich. Eingesetzt wurde es auch in Aquarellen und Pastellen, vereinzelt sogar in der Wandmalerei. Heute ist die Anwendung von Bleiweiß aufgrund seiner Giftigkeit außer für Restaurierungszwecke verboten. Barytweiß ist für die Ölmalerei völlig ungeeignet, da seine optische Dichte (Streukraft) zu nahe bei der des Öles liegt.
Das Bleiweiß kam unter verschiedenen Bezeichnungen in den Handel, teilweise auch in unterschiedlichen Qualitäten. Die Qualitäten unterschieden sich hauptsächlich in der Zusammensetzung, beispielsweise wurde es mit Barytweiß gestreckt. Namen für Bleiweiß sind: Kremser Weiß, Schieferweiß, Holländer Weiß, Venezianer Weiß, Hamburger Weiß, Perlweiß, Schneeweiß, Silberweiß, Kremnitzer Weiß und Deckweiß.
Nachweis von Gemäldefälschungen
Die Verwendung von Bleiweiß kann leicht durch eine Untersuchung mit Röntgenstrahlen nachgewiesen werden, da Bleiweiß diese sehr stark abschirmt. Weitere Untersuchungen betreffen die chemische Zusammensetzung. Während das Bleiweiß, das Maler der niederländischen Gemälde des 17. Jahrhunderts (beispielsweise Jan Vermeer) gebrauchten, aus Blei-Lagerstätten im europäischen Mittelgebirge gewonnen wurde, kam das Bleiweiß, das in süddeutschen Gemälden des 17. Jahrhunderts eingesetzt wurde, aus Blei-Lagerstätten in den europäischen Alpen. Seit dem 19. Jahrhundert werden Bleierze aus Amerika und Australien eingeführt.
Das moderne Bleiweiß unterscheidet sich vom alten Bleiweiß: erstens im Gehalt an Spurenelementen, zweitens in der Isotopenzusammensetzung des enthaltenen Bleis.
Niederländisches Bleiweiß zeichnete sich durch hohe Silber- und Antimongehalte aus (siehe R. Strauß), während heutiges Bleiweiß, das der Vermeer-Fälscher Han van Meegeren verwendete, weder Silber noch Kupfer enthält. Diese Elemente werden heute bei der Verhüttung von Blei vorher abgetrennt (→ Literatur(1): Fälschung und Forschung p. 195-196).
Fälschungen, für die heute hergestellte Bleiverbindungen als Bleipigmente verwendet wurden, können mit Hilfe der Blei-210-Methode [5]erkannt werden[6]. Das Bleiisotop gehört zur Uran-238-Zerfallsreihe, es entsteht aus Radium-226, das mit einer Halbwertszeit von 22 Jahren zerfällt. Diese kurze Halbwertszeit kann man zur Erkennung von Fälschungen der jüngeren Zeit nutzen [7].
Die Werte des Bildes „Christus und die Jünger in Emmaus“[8] des Vermeer-Fälschers Han van Meegeren (Polonium-210: 8.5 ± 1.4, Radium-226: 0.8 ± 0.3) entsprachen nicht den Werten, die in den Gemälden der Niederländer der vergleichbaren Jahre 1600…1660 (Polonium-210: 0.23 ± 0.27, Radium-226: 0.40 ± 0.47) gemessen wurden[9].
Literatur
- Ausstellungskatalog Essen und Berlin: Fälschung und Forschung, p.191, p.195f. Hrsg.: Museum Folkwang, Essen, und Staatliche Museen Preußischer Kulturbesitz, Berlin, 1976. ISBN 3-7759-0201-5.
- Keisch, B., Feller, R. L., Levine, A. S., and Edwards, R. R.: Dating and Authenticating Works of Art by Measurement of Natural Alpha Emitters. In: Science, 155, No. 3767, p. 1238-1242, 1967.
- Keisch, B: Dating Works of Art Trough their Natural Radioactivity: Improvements and Applications. In: Science, 160, p. 413-415, 1968.
- Keisch, B: Discriminating Radioactivity Measurements of Lead: New Tool for Authentication. In: Curator, 11, No. 1., p. 41-52, 1968.
- Strauß, R.: Aktivierungsanalytische Untersuchungen von Pigmenten aus Gemälden süddeutscher Maler des 17. und 18. Jahrhunderts. Dissertation, Technische Hochschule München, 1968, 62 Seiten.
Weblinks
- ↑ a b c Eintrag zu Bleiweiß in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 15.9.2008 (JavaScript erforderlich)
- ↑ Nicht explizit in RL 67/548/EWG, Anh. I gelistet, fällt aber dort mit der angegebenen Kennzeichnung unter den Sammelbegriff „Bleiverbindungen“; Eintrag in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 31. März 2009 (JavaScript erforderlich)
- ↑ Vitruv, De architectura VI 10
- ↑ Temple C. Patton: Pigment Handbook.
- ↑ Beschreibung der 210Pb-Methode
- ↑ → Literatur (4): B. Keisch: Discriminating …)
- ↑ → Literatur (1):Fälschung und Forschung S.191
- ↑ Christus und die Jünger in Emmaus
- ↑ → Literatur (3): B. Keisch: Dating...)
Wikimedia Foundation.
