- Pikrin
-
Strukturformel 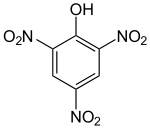
Allgemeines Name Pikrinsäure Andere Namen - 2,4,6-Trinitrophenol
- Trinitrophenol
- TNP
Summenformel C6H3N3O7 CAS-Nummer 88-89-1 PubChem 6954 Kurzbeschreibung gelbe, stark bitter schmeckende Kristalle Eigenschaften Molare Masse 229,11 g·mol−1 Aggregatzustand fest
Dichte 1,76 g·cm−3 [1]
Schmelzpunkt pKs-Wert 0,29 [2]
Löslichkeit gut in Ethanol (80 g·l−1 bei 20 °C), Benzol,
schlecht in Wasser (13 g·l−1 bei 20 °C, 60 g·l−1 bei 100 °C)Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [3] 

Explosions-
gefährlichGiftig (E) (T) R- und S-Sätze R: 3-4-23/24/25 S: (1/2)-28-35-36/37-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Pikrinsäure (gr. πικρος, pikros = bitter) ist der Trivialname für 2,4,6-Trinitrophenol (TNP). Ihre Salze heißen Pikrate.
Inhaltsverzeichnis
Eigenschaften
Pikrinsäure bildet gelbe, stark bitter schmeckende Kristalle, die nur schwer in kaltem Wasser, hingegen besser löslich in siedendem Wasser und leicht löslich in Ethanol und Benzol sind. Bedingt durch die Häufung elektronenziehender Nitrogruppen (–NO2) ist die Pikrinsäure durch ihre phenolische Hydroxylgruppe eine starke Säure (pKs = 0,29). Als starke Säure greift Pikrinsäure unedle Metalle unter Pikratbildung an. Einige der Salze z. B. Bleipikrat sind noch empfindlicher gegenüber Schlag, Reibung und Funken. Sie verhalten sich somit wie Initialsprengstoffe. Ammoniumpikrat wurde als Sprengstoff verwendet.
Ebenfalls als Pikrate bezeichnet man die Molekülverbindungen (Charge-Transfer-Komplexe) mit Aromaten. Diese Feststoffe sind oft schwerlöslich und farbig. Wegen der charakteristischen und scharfen Schmelzpunkte (z.B. Benzol-Pikrat 84 °C[2], Toluol-Pikrat 88 °C[2], Anthracen-Pikrat 138 °C[2]) dient Pikrinsäure als Nachweisreagenz.
Pikrinsäure ist giftig; auf der Haut kann sie starke allergische Reaktionen hervorrufen. Die Kontamination mit Stäuben oder Dämpfen ist daher zu vermeiden.
Darstellung
Die Pikrinsäure wird über die Sulfonierung von Phenol und nachfolgende Behandlung mit Salpetersäure hergestellt. Alternativ bietet sich die Darstellung aus Chlorbenzol über 2,4-Dinitrochlorbenzol, 2,4-Dinitrophenol und dessen erneute Nitrierung an.[4] Früher wurde Pikrinsäure aus Akaroidharz hergestellt.
Verwendung
Primär dient die Pikrinsäure der Farbstoffindustrie zur Herstellung von Pikraminsäure; so wurde es früher zusammen mit arabischem Gummi und destillierten Wasser zur Herstellung gelber Tinte verwendet. Ein weiteres Einsatzgebiet ist die organische Analytik zum Nachweis von Alkaloiden und Kreatinin. Die Verwendung von Pikrinsäure als Füllmaterial für Granaten (wie im Ersten Weltkrieg) oder allgemein als Explosivstoff wurde wegen der unkontrollierten Bildung von hochexplosiven Schwermetallpikraten eingestellt. Die Pikrinsäure wurde hier durch TNT ersetzt. In der Mikroskopie verwendet man Pikrinsäure als Bestandteil von Fixierflüssigkeiten (zur Konservierung zellulärer Strukturen) und zum Anfärben von Präparaten. Ein weiteres Einsatzgebiet von Pikrinsäure ist die Metallografie. Hier wird die Substanz zum Ätzen metallischer Oberflächen verwendet, z. B. bei der Präparation von Magnesiumlegierungen oder bei Seigerungsuntersuchungen an Stählen. Die Ätzung der Stähle wird mit Igeweskys-Reagenz, einer 5 %igen Lösung von Pikrinsäure in wasserfreiem Alkohol, durchgeführt. Pikrinsäure dient auch der Kreatinin-Konzentrationsmessung: Kreatinin bildet in alkalischer Lösung mit Pikrinsäure einen Meisenheimer-Komplex (Jaffé-Reaktion), dessen rote Farbe photometrisch gemessen wird.
Geschichte
Durch Behandlung von Indigo mit Salpetersäure konnte Peter Woulfe als erster 1771 Pikrinsäure darstellen. Neben der Gelbfärbung von Seide hatte es jedoch zunächst noch keine größere Bedeutung.
Die Substanz war das erste detonierende, brisante Geschossfüllmittel und wurde als Lyddit, Ekrasit, Schimose oder Melinit ab 1886 so verwendet, nachdem der Franzose Eugène Turpin die Sprengstoffeigenschaften der lange zuvor bekannten Säure entdeckt hatte.
Pikrinsäure war für die katastrophale Halifax-Explosion im Jahre 1917 verantwortlich. Die Verwendung von Pikrinsäure zur Anfärbung von Backwaren im ausgehenden 19. Jahrhundert war weit verbreitet und war als Weltersches Bitter bekannt, was nach einer Häufung von Vergiftungsfällen jedoch unterbunden wurde.
Gefahrenhinweise
An der Luft verbrennt Pikrinsäure mit starker Rauchentwicklung; bei sehr raschem Erhitzen oder durch eine Initialzündung erfolgt eine Detonation, bei der die Detonationsgeschwindigkeit etwa 7.100 m/s beträgt und damit circa 10 % größer ist als die des TNTs (2,4,6-Trinitrotoluol). Pikrinsäure ist empfindlich gegen thermische (Hitze, Feuer) und mechanische (Schlag, Reibung) Belastung und gilt im Sinne des Sprengstoffgesetzes als explosionsgefährlicher Stoff der Stoffgruppe A (trocken) bzw. C (mit 25 % Wasser angefeuchtet) gemäß § 1 Abs. 3 Sprengstoffgesetz.[5] Für Privatpersonen ist trockene Pikrinsäure somit nach § 27 SprengG erlaubnispflichtig. Trocken ist Pikrinsäure in Lagergruppe 1.1 oder I bzw. als Gefahrgut in Klasse 1.1 (Stoffe, die massenexplosionsfähig sind) eingestuft,[1] angefeuchtet mit 30 % Wasser in Lagergruppe 1.4.[6] Als handelsübliches Produkt ist Pikrinsäure mit > 30 Gew.-% Wasser angefeuchtet und ist damit phlegmatisiert.[1] Angefeuchtet (> 30 Gew.-% Wasser) verhält sich Pikrinsäure wie ein entzündlicher Feststoff und wird zum Transport als Entzündbarer fester Stoff der Gefahrgutklasse 4.1 nach ADR gekennzeichnet.[7]
Einzelnachweise
- ↑ a b c d Eintrag zu CAS-Nr. 88-89-1 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 19. August 2008 (JavaScript erforderlich).
- ↑ a b c d e CRC Handbook of Tables for Organic Compound Identification, Third Edition, 1984, ISBN 0-8493-0303-6.
- ↑ Eintrag zu CAS-Nr. 88-89-1 im European chemical Substances Information System ESIS
- ↑ Hans Beyer und Wolfgang Walter: Organische Chemie, S. Hirzel Verlag, Stuttgart, 22. Auflage, 1984, Seite 504−505, ISBN ,3-7776-0485-2.
- ↑ Altstoffliste im Bundesanzeiger Nr. 233 a vom 16. Dezember 1986 nebst Berichtigung BAnz. Nr. 51 S. 2635 vom 14. März 1987.
- ↑ Bundesanstalt für Materialprüfung, Lagergruppenzuordnung von anderen explosiven Stoffen, Berlin.
- ↑ Hommel: Handbuch der gefährlichen Güter, Springer-Verlag.
Weblinks
Wikimedia Foundation.
