- BOC-Anhydrid
-
Strukturformel 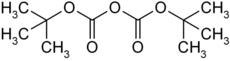
Allgemeines Name Di-tert-butyldicarbonat Andere Namen - "Boc-Anhydrid"
- "Diboc"
- Di-tert-butylpyrocarbonat
- Pyrokohlensäuredi-tert-butylester
Summenformel C10H18O5 CAS-Nummer 24424-99-5 Kurzbeschreibung farbloser Feststoff oder Flüssigkeit[1] Eigenschaften Molare Masse 218,25 g·mol−1 Aggregatzustand flüssig
Dichte 1,02 g·cm−3 (20 °C)[1]
Schmelzpunkt Siedepunkt Löslichkeit unlöslich in Wasser[1], löslich in vielen organischen Lösungsmitteln
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 
Sehr giftig (T+) R- und S-Sätze R: 10-26-36/38-43 S: 28-36/37-45 WGK 2[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Di-tert-butyldicarbonat (im Labor umgangssprachlich – aber fälschlich – meist Boc-Anhydrid oder Diboc genannt), ist eine flüssige, chemische Verbindung, die strukturell sowohl zu den Estern als auch zu den Säureanhydriden gerechnet werden kann.
Verwendung
Die hauptsächliche Verwendung von Di-tert-butyldicarbonat ist die Einführung der tert-Butyloxycarbonyl-Gruppe (Boc-Gruppe), einer der am häufigsten eingesetzten Schutzgruppen in der organischen Chemie. Es ist die weltweit meistgenutzte Chemikalie zum Schutz von Aminofunktionen bei chemischen Reaktionen, besonders in der Peptid- und Glycopeptidchemie.
Die Boc-Schutzgruppe lässt sich einfach einführen. Dazu wird das zu schützende Amin in Gegenwart einer Base mit Di-tert-butyldicarbonat umgesetzt. Sie ist unter vielen chemischen Reaktionsbedingungen stabil, kann aber leicht durch Säuren entfernt werden. Unter anderem wird häufig HCl in Methanol oder Trifluoressigsäure zum Entschützen verwendet. In Kombination z. B. mit (9-Fluorenylmethyl)oxycarbonyl (Fmoc) ergibt sich die Möglichkeit der orthogonalen Schützung: zwei verschiedene Amino-Funktionen eines Moleküls können gezielt nacheinander zur Reaktion gebracht werden.
Herstellung
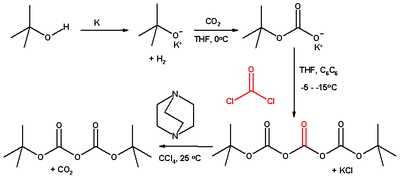
Di-tert-butyldicarbonat wird weltweit nach zwei Verfahren hergestellt: Einerseits durch Umsetzung von Natrium- oder Kalium-tert-butylat mit Phosgen oder Phosgenderivaten und andererseits die katalytische Reaktion von Natrium-tert-butylat mit Kohlendioxid. Führende Anbieter des ersten Syntheseweges sind Jinchemical (China) und Genchem China Co., den zweiten Weg nutzt die Firma Chemtec Leuna GmbH, Deutschland. Die Darstellung aus Kalium-tert-butylat und Phosgen verläuft nach folgendem Schema:[2]
Quellen
- ↑ a b c d e f g Sicherheitsdatenblatt Merck
- ↑ Barry M. Pope, Yutaka Yamamoto, and D. Stanley Tarbell, Dicarbonic acid, bis(1,1-dimethylethyl) ester, Organic Syntheses, Coll. Vol. 6, p.418 (1988); Vol. 57, p.45 (1977).
Wikimedia Foundation.