- Sieben-Tage-Fieber
-
Klassifikation nach ICD-10 A90 Denguefieber [Klassische Dengue] A91 Hämorrhagisches Denguefieber ICD-10 online (WHO-Version 2006) Das Denguefieber ist eine Infektionskrankheit, die von bestimmten Stechmückenarten übertragen wird (Arbovirose). Sie wird von vier verschiedenen Serotypen des Dengue-Virus verursacht. Die Symptome sind oft unspezifisch oder einer schweren Grippe ähnlich, können aber auch innere Blutungen umfassen. Deshalb zählt man das Denguefieber zu den hämorrhagischen Fiebern. Das Denguefieber ist auch als Sieben-Tage-Fieber, Polka-Fieber[1] oder Knochenbrecherfieber bekannt. Bislang gibt es gegen die Erkrankung weder eine Impfung noch eine spezifische antivirale Behandlung.
In Deutschland und der Schweiz besteht eine Meldepflicht bei Verdacht, Erkrankung, Tod, direktem und indirektem Erregernachweis oder hämorrhagischem Krankheitsverlauf.
Inhaltsverzeichnis
Name
Die Herkunft des Namens Dengue ist nicht eindeutig geklärt. Eine Theorie besagt, dass er sich aus dem Spanischen ableitet und mit Ziererei oder Mätzchen übersetzt werden kann. Diese Bezeichnung deutet auf eine schmerzbedingte, auffällig eigenartige Veränderung der Körperhaltung und Verhaltensweise bei erkrankten Personen hin, die eventuell auch nach Abklingen der Erkrankung fortbesteht. Nach anderen Quellen kommt „Dengue“ aus dem afrikanischen Sprachraum (Swahili: Ka-dinga pepo) und steht für einen Krampfanfall, welcher von einem bösen Geist ausgelöst wird.[2][3] Nach einer weiteren Hypothese stammt der Name aus der Malaiischen Halbinsel von Indochina.[2]
Erreger
Das krankheitsverursachende Virus ist ein behülltes Einzel(+)-Strang-RNA-Virus (ss(+)RNA), welches zur Gattung Flavivirus und zur Familie Flaviviridae gehört. Bei diesem Virus lassen sich vier unterschiedliche DEN-Serotypen (DEN-1 bis DEN-4) unterscheiden, die entweder in abgegrenzten oder überlappenden Endemiezonen vorkommen.
Als Reservoirwirte für dieses Virus sind sowohl der Mensch wie auch Affen festgestellt worden.
Die Tatsache, dass bei nicht erheblich vorgeschädigten Menschen und bei nicht erfolgter Doppelinfektion oder Sekundärinfektion (siehe auch Infektion) die von diesen Erregern verursachte Erkrankung nur extrem selten einen tödlichen Verlauf nimmt, zeigt zum Einen, dass diese Viren sehr stark an den Menschen als ihren Reservoirwirt angepasst sind. Die Schädigungen seines Reservoirwirts sind im Grunde nur Nebeneffekte der durch das Virus ausgelösten Infektion, welche die Virusvermehrung jedoch nicht unterstützen sondern ihr sogar hinderlich sein können, wie beispielsweise durch den Tod des Wirtes. Zum Zweiten wird dadurch auch deutlich, dass sich der Mensch ebenfalls im Verlaufe vieler Generationen an dieses Virus anpassen konnte.
Vorkommen
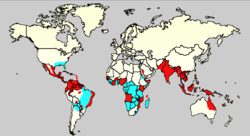 Vorkommen des Erregers, 2006. Rot: Epidemisches Auftreten. Blau: Aedes aegypti.
Vorkommen des Erregers, 2006. Rot: Epidemisches Auftreten. Blau: Aedes aegypti.Die Krankheit stammt ursprünglich aus Afrika, ist vor etwa 600 Jahren nach Asien eingeschleppt und mittlerweile auch in Amerika dokumentiert worden. Seit etwa 200 Jahren beobachtet man in vielen tropischen Gebieten weltweit ein epidemisches Auftreten des Denguefiebers.
Der internationale Handel – wie beispielsweise Containerschiffe mit Obstimporten aus Afrika – ermöglichte es infizierten Mückenlarven, weitere Infektionsgebiete zu eröffnen, in denen sie normalerweise nicht vorkamen. Auch in den Tropen infizierte Reisende können die Erkrankung in normalerweise sichere Gebiete einschleppen. Aufgrund der globalen Erwärmung breitet sich das Denguefieber nunmehr auch in den gemäßigten Breiten aus.
Hauptverbreitungsgebiet sind heute Lateinamerika, Zentralafrika, Indien, Südostasien, Teile des Pazifik (u. a. Neukaledonien) und der Süden der USA. Auch nach Europa wird das Fieber heute regelmäßig eingeschleppt. Mit jährlich etwa 2000 eingeschleppten Fällen gehört Denguefieber zu den häufigsten viralen Infektionen bei deutschen Urlaubern.
Im Jahre 2006 traten Epidemien des Fiebers sowohl in der Dominikanischen Republik wie auch in Kuba auf (hier von August bis Oktober).[4] Nach verschiedenen Berichten wurden in Kuba besonders betroffene Stadtteile von Havanna, sowie vier Provinzen von den Gesundheitsbehörden zeitweise abgeriegelt. Es wurden Hilfslazarette eingerichtet und Spezialeinheiten waren weit über das übliche Maß hinaus zur Bekämpfung der Moskitos im Einsatz. Seit November wurden nur noch vereinzelte Fälle bekannt. Obwohl dies anscheinend der stärkste Ausbruch in 25 Jahren war, berichteten kubanische Behörden nur sehr zögernd an die WHO. Es gab jedoch Berichte von vermehrten hämorrhagischen Verläufen der Infektion. Eine Ursache könnte der mehrfache Wechsel des vorherrschenden Serotyps auf Kuba sein. (1977: Dengue-1, 1981: Dengue-2, 2001: Dengue-3).[5]
Anfang 2007 kam es in mehreren südamerikanischen Ländern zu vermehrtem Auftreten von Denguefieber. Am 23. Februar 2007 verhängte die Regierung von Paraguay nach dem Ausbruch einer Denguefieberepidemie (nach offiziellen Angaben mehr als 15.000 Erkrankte) für 60 Tage den Ausnahmezustand. Der an Paraguay grenzende brasilianische Bundesstaat Mato Grosso do Sul verzeichnete 42.000 Krankheitsfälle (Anfang März 2007). In beiden Ländern kam es zu mehreren Todesfällen, teilweise infolge hämorrhagischen Verlaufs der Erkrankung. Jüngsten Zeitungsberichten (März 2008) zufolge sind im brasilianischen Bundesstaat Rio de Janeiro die Zahlen der Infektionen und Todesfälle, insbesondere von Kindern, deutlich angestiegen. Dies stellt ein besonderes Problem für Armenviertel, wie beispielsweise der sogenannten Cidade de Deus („Stadt Gottes“) der Stadt Rio de Janeiro, dar.
In 2009 ist es wieder in verschiedenen südamerikanischen Ländern zu Dengueepidemien gekommen. In Bolivien war vor allem die Stadt Santa Cruz de la Sierra betroffen. In Argentinien ist die aktuelle Dengueepidemie die schlimmste seit der Rückkehr der Krankheit im Jahr 1998, wobei sich Infektionsfälle nicht mehr nur auf die nördlichen Provinzen wie Salta und Jujuy begrenzen, sondern mittlerweile auch in bisher unbetroffenen Regionen wie Tucumán, Catamarca und Chaco vorkommen. So stieg die Zahl der Infektionen bis Ende April auf fast 18.000 Fälle an, wobei sich diese im weiteren Verlauf noch auf über 26.000 Infizierte erhöhen könnte.[6][7]
Eine aktuelle Arbeit des argentinische Agraringenieurs Alberto Lapolla [8] bringt die aktuelle Dengueepidemie mit dem zunehmenden Sojaanbau in Argentinien in Verbindung. In seiner Studie deutet er auf den Zusammenhang zwischen den Verbreitungsgebieten der Denguefieber übertragenden Aedes aegypti- Mücke und den Sojaanbaugebieten in Bolivien, Paraguay, Argentinien, Brasilien und Uruguay. Dort werden vor allem gentechnisch manupulierte Sojabohnen von Monsanto unter Verwendung des Herbizids Glyphosat sowie von 2,4-D, Atrazin,Endosulfan, Paraquat, Diquatdibromid und Chlorpyrifos angebaut. All diese Gifte töten auch die natürlichen Feinde der Mücke wie beispielsweise Fische und Amphibien (Kröten und Frösche), welche sich sowohl als Larven als auch als ausgewachsenes Tier von der Mücke ernähren. Dies lässt sich vor allem am Rückgang der Amphibienpopulation in der Pamparegion und deren Flüssen und Wasserefugien sowie am vermehrten Auftreten toter oder deformierter Fische ablesen. Dazu kommt die Abholzung von Wäldern im Nordosten Argentiniens, welche das ökologische Gleichgewicht zerstört und dabei zur Vernichtung der Lebensräume anderer Mückenfeinde geführt hat. Dies alles hat laut dieser Studie einen entscheidenden Beitrag zur zunehmenden Verbreitung der Aedes aegypti und damit des Denguefiebers geführt.
Häufigkeit
2,5 Milliarden Menschen leben in Endemiegebieten. Jährlich werden einige 10 bis 100 Millionen Menschen von dieser Erkrankung befallen, etwa 95 % der Infizierten sind Kinder. 1999 war das Denguefieber die am häufigsten durch Mücken übertragene Viruskrankheit. Etwa 2 bis 5 Prozent der Erkrankten versterben an diesem Fieber, insbesondere Kinder und Jugendliche. Bei Kindern bis zu einem Jahr liegt die Todesrate bei etwa 30 %.
Übertragung
Die wichtisten Überträger (Vektoren) von Denguefieber sind die Gelbfiebermücke (Aedes aegypti, auch Ägyptische Tigermücke oder Denguemücke genannt) und die sich auch in Europa ausbreitende Asiatische Tigermücke (Aedes albopictus).[9] In bestimmten Regionen kommen weitere Mückenarten als Übertrager von Denguefieber in Frage, z.B. die Polynesische Tigermücke (Aedes polynesiensis) im südlichen Pazifik [10] oder Aedes scutellaris in Neuguinea[11]. Bei anderen Mückenarten wurde ebenfalls eine Vektorkompetenz gezeigt.[12][13]
Denguefieber ist vor allem eine Krankheit der Großstädte, weil die Überträgermücken Aedes aegypti und Aedes albopictus besonders gut an das städtische Biotop angepasst sind. Da die erwachsenen Tigermücken tagaktiv sind, kann man sich kaum wie z.B. gegen Malaria durch Bettnetze schützen. Als Larvenbiotope reichen unverschlossene Wasserbehälter und kleine Mengen stehenden Wassers aus, das sich in Eimern, Dosen, Flaschen, Autoreifen oder Plastikfolien sammelt. Zudem sind die Eier der Tigermücken trockenresistent und können so Trockenzeiten überdauern. All dies macht die Mücken zu einem schwer zu bekämpfenden Gegner.
Überträgerbekämpfung
Da bis heute keine Prophylaxe oder Impfung gegen Dengueviren verfügbar ist, kommt der Bekämpfung der Überträgermücken eine zentrale Rolle zu. Die Verwendung von in die Umgebung gesprühten Insektiziden ist dabei nicht nur wegen möglicher negativer Folgen für Mensch und Umwelt problematisch, sie verliert mit der Zeit auch wegen der Bildung von Resistenzen an Wirksamkeit. Dazu kommt, dass sich vor allem Aedes aegypti oft im Inneren von Gebäuden aufhält und insofern vor im Freien ausgebrachten Insektiziden geschützt ist.
Die zur Zeit wichtigste Strategie fußt auf der möglichst umfassenden und durch die Allgemeinheit unterstützte Beseitigung der Larvengewässer.[14] Wichtig für den Erfolg der Bekämpfung von Dengueüberträgern ist immer eine umfassende Aufklärung und Einbindung der Bevölkerung. Größere Wasserbehälter können mit Larviziden behandelt werden. Neben chemischen Produkten wird dabei teilweise Bacillus thuringiensis israelensis verwendet. Auch der Einsatz von Bakterien der Gattung Wolbachia wird zur Bekämpfung der Überträgermücken untersucht.[15]
Eine zusätzliche biologische Bekämpfungmethode von Larvenvorkommen in größeren Behältern (vor allem Trinkwasserfässern) könnte der Einsatz von Mesocyclops thermocyclopoides (Copepoda: Cyclopidae) sein, einem in stehenden Tümpeln vorkommenden tropischen Ruderfußkrebs, der sich unter anderem von Stechmückenlarven ernährt.[16] Bei einer Studie in Vietnam war eine Kombination verschiedener und auch von der Bevölkerung getragener Bekämpfungsansätze mit der Verwendung von Mesocyclops erfolgreich.[17]
Um auch die erwachsene Überträgermücken effektiver bekämpfen zu können als bisher, sind zur Zeit weitere Methoden in Erprobung. Eine ist die Verwendung von mit Kontaktinsektiziden behandelten Textilien, aus denen Vorhänge oder Abdeckungen von Wasserbehältern gefertigt werden. Sie töten ruhende oder auf der Suche nach Eiablagegewässern befindliche Mückenweibchen.[18] Eine andere neue Methode ist der Einsatz spezieller, für den Fang von Tigermücken optimierter und auf einem Lockstoff-Cocktail basierender Fallen.[19][20]
Diagnose
Die klinische Diagnosestellung ist wegen der Vielzahl der möglichen Erreger für Infektionskrankheiten schwierig. Antikörper sind erst nach dem vierten Krankheitstag nachweisbar. Ein direkter Nachweis für das Virus mit der Reverse-Transkriptase-Polymerasekettenreaktion (RT-PCR) zwischen dem vierten und siebten Krankheitstag sichert die Diagnose.
Eine dem Denguefieber klinisch ähnliche Erkrankung ist das Chikungunyafieber. Nach Empfehlungen der WHO sollte das Blut eines Patienten mit Verdacht auf Denguefieber immer dann auf Antikörper gegen das Chikungunya-Virus untersucht werden, wenn eine Infektion mit Dengueviren nicht nachgewiesen werden kann und der Patient sich in einem Gebiet aufgehalten hat, in dem das Chikungunyafieber vorkommt.[21]
Krankheitsverlauf
In etwa 90 % der Erkrankungen wird ein stummer (oligosymptomatischer) Verlauf wie oft bei einem grippalen Infekt beobachtet.
Bei den restlichen 10 % der Fälle beginnt die Krankheit nach einer Inkubationszeit von etwa zwei bis zehn Tagen mit einem Verlauf über drei Stadien:
- Plötzlich einsetzender Krankheitsbeginn mit Fieber bis 41 °C, Schüttelfrost, Erschöpfungszuständen, Kopf-, Glieder-, Gelenk- und Muskelschmerzen („breakbone fever“), auffällig niedrigem Puls und metallisch bitterem Mundgeschmack. Gelegentlich tritt auch Hautausschlag, Übelkeit und Erbrechen auf.
- Nach dem Fieberabfall und einer weiteren Zeitspanne von vier bis fünf Tagen kommt es zu einem erneuten Fieberschub. Danach entwickelt sich ein masernähnlicher Hautausschlag mit Lymphknotenschwellungen.
- Nach weiteren fünf bis sechs Tagen beginnt die Erholungsphase, die sich über mehrere Wochen hinziehen kann.
Als Denguetrias bezeichnet man Fieber, Ausschlag und Kopf-, Glieder-, Gelenk- oder Muskelschmerzen.
Hämorrhagisches Denguefieber (DHF)
Das hämorrhagische Denguefieber ist ein akutes Schocksyndrom mit Hämorrhagien. Als wahrscheinlichste Ursache wird eine erneute Infektion mit einem anderen Serotypen des Dengue-Virus angesehen.
Ausschließlich bei Menschen mit bereits existierenden Antikörpern gegen einen anderen Serotyp des Virus kann es zu einer immunologischen Überreaktion kommen, in deren Verlauf die Durchlässigkeit (Permeabilität) der Blutgefäßwände größer wird und deshalb unkontrollierte Blutungen auftreten. Die Antikörper können durch eine vorangegangene Erkrankung erworben oder von Müttern auf ihre Kinder übertragen werden. Dies erklärt, warum vor allem Kinder von dieser Variante des Denguefiebers betroffen sind.
Die hämorrhagische Form beginnt wie das normale Denguefieber, verschlechtert sich aber nach zwei bis fünf Tagen dramatisch. Der Blutkreislauf bricht zusammen und es kommt zur Rötung des Gesichtes, zu (inneren) Blutungen, Flüssigkeitsverlust, hirnbedingten (zerebralen) Krampfanfällen, Koma, Zahnfleischbluten, Bluterbrechen, Teerstuhl, einem Anschwellen der Leber und den allgemeinen Zeichen eines Schocks (Tachykardie, Hypotonie, kaltschweißige Haut, Blässe).
Zusätzlich können in dieser Phase dissiminiert Petechien auftreten. Dies sind mikrozirkuläre Einblutungen der Haut, die als rote Punkte auffallen.
Der Krankheitsverlauf ist abhängig vom Schweregrad, dem Therapiebeginn sowie den medizinischen Möglichkeiten einer angemessenen (adäquaten) Schockbehandlung. In ärmeren Regionen mit schlechter medizinischer Versorgung kann die Letalität des hämorrhagischen Denguefiebers bis zu 30 % betragen.
Therapie
Zur Zeit gibt es keine primär wirksamen, antiviralen Medikamente gegen diese Infektionskrankheit, deshalb können lediglich die auftretenden Beschwerden durch eine Behandlung gemildert werden.
Wegen des Blutungsrisikos beim hämorrhagischen Denguefieber wird bei jeder Erkrankung, wo dies nicht auszuschließen ist, von Acetylsalicylsäure-Präparaten (Aspirin und Verwandte) mit ihrer auch gerinnungshemmenden Wirkung abgeraten. Zur Symptomlinderung erscheint Paracetamol als geeigneter, da dieser Wirkstoff eine solche Wirkung nicht besitzt.
Das von IBM gesponserte, gemeinnützige World Community Grid und die University of Texas Medical Branch versuchen gerade gemeinsam ein Medikament gegen Denguefieber zu entwickeln. Sie nutzen dazu die von Freiwilligen zur Verfügung gestellte Rechenleistung normaler PCs.[22]Immunisationsschutz
Die Infektion mit einer von den vier Arten des Krankheitserregers bietet nur einen Immunisationsschutz gegen denselben Serotyp, nicht jedoch gegen die anderen Serotypen des Virus, so dass eine Person bis zu vier mal von Denguefieber befallen werden kann. Auffällig ist, dass nach einer überstandenen Infektion eines Serotyps die Krankheitsfolgen bei einer späteren Infektion mit einem anderen Serotyp meist wesentlich heftiger ausfallen, als bei der Erstinfektion. Ein bislang nicht vorhandener Impfschutz wäre deshalb nur dann sinnvoll, wenn er zugleich gegen alle vier bisher bekannten Serotypen schützen könnte.
Vorbeugung
Der beste Schutz ist besonders tagsüber die Vermeidung von Stichen durch Schutzkleidung, Sprays und Moskitonetze, denn die Mücken sind tagaktiv.
Gegenwärtig gibt es keine Impfung gegen das Denguefieber. Allerdings wird in Thailand an einem tetravalenten Lebendimpfstoff gearbeitet. Die ersten Ergebnisse erscheinen vielversprechend. Man hofft, zwischen 2005 und 2010 durch Massenimpfungen die epidemischen Ausmaße des Denguefiebers einzudämmen. Bis dahin ist ein Schutz gegen das Denguefieber nur durch einen generellen Schutz vor Mücken möglich. Dabei ist neben der Vernichtung der Mücken oder ihrer Brutstätten auch die Nutzung (insektizidgetränkter) Moskitonetze eine sinnvolle Maßnahme. Ein weiteres bedeutendes Forschungszentrum auch für diese Erkrankung ist das Novartis Institute for Tropical Diseases (NITD) in Singapur. Nach Aussagen seines Leiters, Professor Paul Herrling, stehen die Forschungen dort in Bezug auf einen medikamentösen Wirkstoff zur erfolgreichen Behandlung des Denguefiebers noch am Anfang.
Einzelnachweise
- ↑ Medizincontrolling des Universitätsklinikums Münster – DRG-Research Group
- ↑ a b Dengue fever: essential data: http://www.cbwinfo.com/Biological/Pathogens/DENV.html
- ↑ Online Etymology Dictionary
- ↑ Noticias – Más de 3,000 afectados por dengue; FFAA a hospitales
- ↑ promedmail.org: DENGUE/DHF UPDATE 2006 (37)
- ↑ [http://www.clarin.com/diario/2009/04/03/sociedad/s-01890196.htm
- ↑ [http://www.clarin.com/diario/2009/04/22/um/m-01903344.htm
- ↑ [1]
- ↑ D. Fontenille, A.B. Failloux & R. Romi (2007): „Should we expect Chikungunya and Dengue in Southern Europe?“ In: Emerging pests and vector-borne diseases in Europe. Volume 1, herausgegeben von W. Takken & B. G. J. Knols. Wageningen Academic Publishers. ISBN 978-90-8686-053-1 [2] PDF 313 kb
- ↑ L. Rosen, L.E. Rozeboom, B.H. Sweet & A.B. Sabin (1954): „The transmission of dengue by Aedes polynesiensis Marks.“ Am. J. Trop. Med. Hyg. 3: 878-882.
- ↑ I.M. Mackerras (1946): „Transmission of dengue fever by Ae. (Stegomyia) scutellaris Walk. in New Guinea.“ Trans. R. Soc. Trop. Med. Hyg., 40: 294-312.
- ↑ J.E. Freier & L. Rosen (1987): „Vertical transmission of dengue virus by mosquitoes of the Aedes scutellaris group.“ Am. J. Trap. Med. Hyg. 37(3): 640-647.
- ↑ J.E. Freier & L. Rosen (1988): „Vertical transmission of dengue virus by Aedes mediovittatus.“ Am. J. Trop. Med. Hyg. 39(2): 218-222
- ↑ W. Parks W & L. Lloyd (2004): „Planning Social Mobilization and Communication for Dengue Fever Prevention and Control.“ WHO/CDS/WMC/2004.2. WHO, Genf.
- ↑ BBC-Meldung, abgerufen am 2. Januar 2009 (engl.)
- ↑ S. Schaper (2001): „Beitrag zur Verwendung von Mesocyclops thermocyclopoides für die Bekämpfung der Stechmücke Aedes aegypti in Costa Rica“. Dissertation Hannover. ISBN 3831116687
- ↑ B. Kay, V.S. Nam (2005): „New strategy against Aedes aegypti in Vietnam.“ The Lancet 365 (9459): 613-617. DOI:10.1016/S0140-6736(05)17913-6
- ↑ A. Kroeger, A. Lenhart, M. Ochoa et al. (2006): „Effective control of dengue vectors with curtains and water container covers treated with insecticide in Mexico and Venezuela: cluster randomised trials.“ BMJ 332, 1247-1252.
- ↑ A. Rose, M. Geier, A.E. Eiras, M. da Gloria Teixeira, M. das Gracas Vale Barbosa & M.P. Gomes Mourao (2008): „Novel mosquito traps in the fight against urban dengue – from monitoring to control. Introduction to a feasibility study in Manaus, Brazil.“ Proceedings of the XXIII International Congress of Entomology, Durban, South Africa.
- ↑ http://www.bg-sentinel.com/en/World_Bank_Development_Marketplace.html
- ↑ http://www.who.int/csr/resources/publications/dengue/034-47.pdf (Pdf-Datei)
- ↑ World Community Grid: Projekt „Discovering Dengue Drugs – Together“
Literatur
- U. Kuhnle, W. Krahl: „Denguefieber und Hämorrhagisches Denguefieber. Die tödliche Pandemie des 20. Jahrhunderts“. Monatsschrift Kinderheilkunde 147 (1), S. 48–50 (1999), ISSN 0026-9298
- Anonymus: „Denguefieber. Die unbekannte Pandemie“. Pharmazeutische Zeitung 147 (7), S. 52–55 (2002), ISSN 0031-7136
- Anonymus: „Denguefieber rund um die Welt verbreitet“. Pharmazeutische Zeitung 149 (14), S. 50–53 (2003), ISSN 0031-7136
- Deutsches Ärzteblatt; Heft 22; 2005; 102:A 1594–1595
Weblinks
- Denguefieber – Informationen des Robert Koch-Instituts
- Deutsches Grünes Kreuz e. V. – Denguefieber
- Artikel zu Denguefieber bei mediScon
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.


