- Strattera
-
Strukturformel 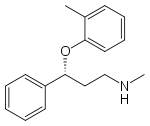
Allgemeines Freiname Atomoxetin Andere Namen Summenformel C17H21NO CAS-Nummer 83015-26-3 PubChem 54841 ATC-Code N06BA09
DrugBank APRD00614 Arzneistoffangaben Wirkstoffklasse Wirkmechanismus Fertigpräparate Strattera® (EU, D, A)
Verschreibungspflichtig: Ja Eigenschaften Molare Masse 255,35 g·mol−1 Aggregatzustand Feststoff [1]
Schmelzpunkt Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: 22-24/25 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 196 mg·kg−1 (Ratte p.o.)
WGK 3 (stark wassergefährdend) [1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Atomoxetin ist ein ursprünglich zur Behandlung von Depressionen entwickelter Arzneistoff, der sich für Depressionen jedoch als unwirksam erwiesen hat und dessen chemische Struktur stark derjenigen von Fluoxetin ähnelt. Im Gegensatz zum SSRI Fluoxetin soll Atomoxetin selektiv die Wiederaufnahme (Re-Uptake) von Noradrenalin aus dem synaptischen Spalt hemmen (NARI).
Atomoxetin wurde im März 2005 in Deutschland für die Indikation ADHS zugelassen und wird unter dem Namen (Strattera®) von der Firma Eli Lilly and Company vermarktet.
Atomoxetin unterliegt in Deutschland im Gegensatz zu den bislang bei ADHS eingesetzten Stimulanzien (insbesondere Methylphenidat) nicht dem Betäubungsmittelgesetz.
Pharmakokinetische Daten:
- Bioverfügbarkeit = 63–94 %
- Proteinbindung = 40 %
- Plasmahalbwertszeit = 5 h
Hinsichtlich der Behandlung von Kindern und Jugendlichen sind prinzipiell ähnliche Vorsichtsmaßnahmen wie bei den Serotonin-Wiederaufnahmehemmern zu beachten. Darüber hinaus liegt seit September 2005 ein Rote-Hand-Brief des Herstellers vor, in dem über ein signifikant erhöhtes Risiko der Begünstigung oder Auslösung von aggressivem Verhalten, Suizidalität und Suizidhandlungen unter Atomoxetin im Vergleich zu Placebo bei Kindern, nicht aber bei Erwachsenen informiert wird.[2] Bei Auftreten von Suizidgedanken unter dem Medikament soll die Einnahme beendet werden. Während der Atomoxetin-Anwendung ist aufmerksam auf Anzeichen für Suizidalität zu achten. Leberschäden sind aufgetreten und haben zu Warnhinweisen durch den Hersteller geführt.Einzelnachweise
- ↑ a b c d Sicherheitsdatenblatt für Atomoxetin-HCl – Sigma-Aldrich 22. Dezember 2007
- ↑ Rote-Hand-Brief vom 29. September 2005: zum erhöhten Suizidrisiko unter Atomoxetin (pdf)
Weblinks
- FDA Label für STRATTERA (atomoxetine hydrochloride) CAPSULES for Oral Use – Stand: Juli 2008 auf der Webseite der Food and Drug Administration FDA
- arznei-telegramm Artikel zur Markteinführung von Strattera®
- Pressemitteilung von Frontal 21 der Dokumentation am 9. Dezember 2008, im ZDF
- Schreiben an Frontal 21 vom 17. November 2008
- Strattera (Wirkstoff: Atomoxetin): Informationen zu Berichten aus der Nebenwirkungsdatenbank des BfArM - Erstellt: 9. Dezember 2008
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.
