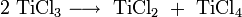- TiCl2
-
Kristallstruktur 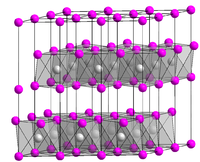
__ Ti2+ __ Cl- Allgemeines Name Titan(II)-chlorid Andere Namen Titandichlorid
Verhältnisformel TiCl2 CAS-Nummer 10049-06-6 PubChem 66228 Kurzbeschreibung schwarzer, selbstentzündlicher Feststoff Eigenschaften Molare Masse 118,79 g/mol Aggregatzustand fest
Dichte 3,13 g/cm3 [1]
Schmelzpunkt Siedepunkt 1500 °C[2]
Löslichkeit Zersetzung in Wasser
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 

Leicht-
entzündlichÄtzend (F) (C) R- und S-Sätze R: 14/15-17-34 S: 16-24-26-36/37/39-45 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Titan(II)-chlorid ist eine chemische Verbindung aus der Gruppe der Chloride.
Inhaltsverzeichnis
Gewinnung und Darstellung
Gewöhnlich wird Titan(II)-chlorid durch thermale Disproportionierung von Titan(III)-chlorid bei 500 °C gewonnen.
Eigenschaften
Titan(II)-chlorid ist ein starkes Reduktionsmittel (reagiert heftig mit Wasser und Sauerstoff) und besitzt eine geschichtete Cadmiumdiiodid Kristallstruktur, wobei das Titan(II) oktaedrisch zu sechs Chloridliganden positioniert ist.[3][4] Es bildet mit Derivate bzw. Komplexverbindungen in der TiCl2(R)2 wobei R ein Chelat (z.B. dppe oder TMEDA) oder ein Salz (z.B. Natriumchlorid) sein kann.
Verwendung
Titan(II)-chlorid kann zur Herstellung von reinem Titan[5] und als Mediator bei organischen Synthesen verwendet werden.
Sicherheitshinweise
Titan(II)-chlorid ist selbstentzündlich (hängt u. a. von der Korngröße ab) und bildet bei Kontakt mit Wasser oder feuchter Luft hochentzündliche Gase in gefährlicher Menge. Sie zersetzt sich in Wasser mit heftiger Reaktion.
Quellen
- ↑ a b c Eintrag zu CAS-Nr. 10049-06-6 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 18.04.2008 (JavaScript erforderlich)
- ↑ Datenblatt bei WebElements (englisch)
- ↑ Gal'perin, E. L.; Sandler, R. A.: "TiCI2". In: Kristallografiya. 7, 1962, S. 217–19.
- ↑ Baenziger, N. C.; Rundle, R. E.: "TiCI2" Acta Crystallographica. 1,, 1948,, S. 274ff. doi:10.1107/S0365110X48000740
- ↑ Buchauszug
Wikimedia Foundation.