- Vitamin K1
-
Strukturformel 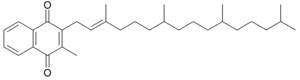
Allgemeines Trivialname Vitamin K1 Andere Namen - Phyllochinon
- Phytomenadion (INN) (Konakion®)
- 2-Methyl-3-phytyl-1,4-naphthochinon
- 2-Methyl-3-(3,7,11,15-tetramethyl- 2-hexadecenyl)- 1,4-naphthalendion
Summenformel C31H46O2 CAS-Nummer 84-80-0 ATC-Code B02BA01
Kurzbeschreibung gelbe Flüssigkeit Vorkommen Kohl, Spinat, Rosenkohl, Kohlsprossen Physiologie Funktion Blutgerinnung, Knochenstoffwechsel, Photosynthese, Vitamin K-Zyklus Täglicher Bedarf etwa 80 µg Folgen bei Mangel Verlängerung der Blutgerinnung, bei Säuglingen Hirnblutungen, Verdauungsstörungen Überdosis nicht bekannt Eigenschaften Molare Masse 450,71 g·mol−1 Aggregatzustand flüssig Dichte 0,97 g·cm−3 Schmelzpunkt −20 °C Siedepunkt 140–145 °C Löslichkeit fettlöslich, auch in Alkohol, Benzol, Chloroform, Ether löslich Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Phyllochinon oder Vitamin K1 gehört zu den fettlöslichen K-Vitaminen, kommt in unterschiedlichen Konzentrationen in den Chloroplasten der Grünpflanzen als normaler Bestandteil des Photosyntheseapparates und zum Teil in deren Früchten vor und spielt im menschlichen Organismus unter anderem bei der Blutgerinnung und beim Knochenstoffwechsel eine wichtige Rolle. In der Photosynthese der Pflanzen ist es in der Elektronenübertragungskette als Kofaktor A1 beteiligt. Das Molekül besteht aus einem Methyl-Naphthochinon mit einer Phytyl-Seitenkette. Es bildet eine Substanz, die bei Raumtemperatur als viskose Flüssigkeit vorliegt.
Inhaltsverzeichnis
Namen
Vitamin K1 ist die triviale Bezeichnung für 2-Methyl-3-phytyl-1,4-naphtochinon (auch α-Phyllochinon). Seinen Ursprung hat der Name Phyllochinon von dem Wort Phyllos, das Blatt. Der Buchstabe K wurde eingesetzt, nach dem der dänische Forscher Henrik Dam um 1935 aus getrockneten Luzerne-Blättern eine fettlösliche Substanz isolierte, die eine ausgleichende Wirkung auf die Blutgerinnung zeigte (Koagulations-Vitamin) und man es der Einfachheit halber dann Vitamin K nannte. Es ist ein Terpenoid.
Beschreibung
Nur mit der Hilfe von Gallensäure kann Vitamin K resorbiert werden. Eine Erhöhung der Resorption wird durch die gleichzeitige Aufnahme von Fetten gesteigert. Vitamin K ist in der Leber an der Herstellung verschiedener Blutgerinnungsfaktoren beteiligt. Weiterhin ist Vitamin K über körpereigene Proteine, beispielsweise das Osteocalcin und über Funktionen innerhalb des Stoffwechsels von Calcium direkt am Knochenaufbau beteiligt. Aufgrund der Hitzestabilität der Vitamin K-Gruppe treten beim Zubereiten, insbesondere beim Garen nur wenig Vitaminverluste auf. Vitamin K ist gleichzeitig auch gegenüber Sauerstoff stabil. Unter Einstrahlung von Licht wird Vitamin K inaktiv und verliert schnell seine Bioverfügbarkeit.
Alle Substanzen mit Phyllochinon-Wirksamkeit (K-Vitamine) leiten sich vom natürlicherweise nicht vorkommenden 2-Methyl-1,4-Naphtochinon (Menadion) ab. Voraussetzungen für die Vitamin-K-Aktivität sind neben dem unsubstituierten, aromatischen Ring eine lipophile Seitenkette (trans-Konfiguration). Optimal sind natürliche Terpenketten mit 20 Kohlenstoffatomen. Seitenketten unter 8 Kohlenstoffatomen führen außer bei Menadion zur Inaktivität.
Es sind bis zu 100 Verbindungen mit Vitamin-K-Wirksamkeit bekannt, von denen aber nur drei von Bedeutung sind.
Aufgabe/Funktion
Blutgerinnung
Die Hauptfunktion von Vitamin K besteht darin, dass es für die Synthese bestimmter Proteine (Prothrombin) notwendig ist, die in der Blutgerinnung eine wichtige Rolle einnehmen[1][2] . Mit diesen Faktoren werden Blutungen gestoppt (Gerinnung). Auch bei der Biosynthese von Proteinen im Knochen, in der Niere, im Plasma und Bindegewebe spielt Vitamin K eine große Rolle. Vitamin K1 ist als fettlösliches Vitamin an die Resorption der Fette gebunden. Die Resorptionsrate beträgt 60–80 Prozent. Vitamin K2 gelangt dagegen durch Diffusion in das Darmgewebe. Die Vitamine K1 und K2 gelangen über das Blut zum Knochenmark, zur Leber und Niere. Hier kann eine Speicherung bis zu 14 Tagen erfolgen. Ausgeschieden werden die Vitamine über die Galle und teilweise über die Nieren. Die biologische Aktivität von Vitamin K ist auf seine Fähigkeit zurückzuführen, zwischen seinen oxidierten (Chinon) und reduzierten (Hydrochinon) Formen im Vitamin K-Zyklus zu wechseln. Die wesentliche Bedeutung von Vitamin K liegt in seinem Beitrag zur posttranslationalen Einführung einer Carboxylgruppe in die γ-Position von Glutamylresten spezifischer Proteine, wodurch sich deren Eigenschaften ändern. Seine wichtigste Funktion ist die Beteiligung an der Synthese verschiedener Blutgerinnungsfaktoren.
Knochenstoffwechsel
Phyllochinon spielt als Vitamin K1 eine wichtige Rolle beim Knochen-Stoffwechsel[3][4].
Photosynthese
Phyllochinon ist im Photosynthese-Reaktionszentrum Photosystem I enthalten, wo es in der Elektronenübertragungskette als sekundärer Elektronen-Akzeptor (Kofaktor A1) beteiligt ist[5].
Vitamin K-Zyklus
Das Peroxid des Vitamin K führt unter Veränderung zum Epoxid des Vitamin K zur Deprotonierung des Proteins (z. B. des Gerinnungsfaktors). Das Protein wird mittels CO2 und Energie aus ATP zum γ-carboxylierten Protein (oder vitamin K-abhängigem Gerinnungsfaktor).
Das Epoxid des Vitamin K wird mittels Epoxid-Reduktase zum Chinon des Vitamin K. Das Chinon des Vitamin K wird mittels Reduktase zum Hydrochinon des Vitamin K. Diese beiden Schritte können durch die Herzinfarkt-Medikamente Dicoumarol, Marcumar und Warfarin inhibiert werden.
Das Hydrochinon des Vitamin K wird zum Peroxid des Vitamin K. Der Zyklus beginnt von vorn.
Vorkommen
Vitamin K1 findet sich in den Lamellarmembranen der Chloroplasten in grünen Pflanzen, während die Vitamin K2 Formen unter anderem von der Darmflora synthetisiert werden. Der aromatische Kern der K-Vitamine wird im sogenannten Shikimisäureweg gebildet. Im Körper ist das Vitamin K im Blutplasma vorhanden und in der Leber, Niere und Milz gespeichert. Vitamin K kommt natürlich vor und wird von Pflanzen und einigen Mikroorganismen synthetisiert. Es kommt in grünem Gemüse (Rosenkohl, Grünkohl, grüne Tomaten, Spinat, Broccoli, Möhrengrün,..) und Kartoffeln, Hagebutten, Salat, Sojabohnen, grünem Tee, in Milch und Milchprodukten und Muskelfleisch vor. Der Gehalt schwankt jahreszeitlich.
Tagesdosis von 65 µg (1 µg = 0,000 001 g = 0,001 mg) ist beispielsweise enthalten in:
- 15 g Schnittlauch
- 25 g Rosenkohl
- 50 g Kalbsleber
- 3 Eiern
- 220 g Speisequark
- 400 g Champignons
- 500 g Erdbeeren
Weiterhin enthalten beispielsweise folgende Nahrungsmittel Vitamin K1 (1 mg = 0,001 g):
- 200 g Rosenkohl 1,14 mg
- 200 g Blumenkohl 0,60 mg
- 200 g Kohlrabi 1,00 mg
- 300 g Vollkornbrot 37 μg (0,037 mg)
- 30 g Müsli 15 μg
Bedarf
Die Festlegung des Vitamin-K-Bedarfs gestaltet sich aufgrund analytischer Probleme bei der Bestimmung dieses Vitamins in Lebensmitteln sowie der Ungewissheit über die Höhe der Synthese durch Bakterien im Darm schwierig. Hinsichtlich des täglichen Bedarfs an Vitamin K besteht eine unterschiedliche Bewertung. Die Deutsche Gesellschaft für Ernährung empfiehlt: 65 µg für Frauen und 80 µg für Männer pro Tag. Da Säuglinge häufig unter einem Vitamin-K-Mangel leiden, weil Muttermilch nur einen geringen Vitamin K-Gehalt hat, wird oft eine Vitamin K-Prophylaxe empfohlen.
Mangelerscheinungen (Hypovitaminose)
Ein Vitamin K-Mangel beim Menschen ist – mit der Ausnahme von Neugeborenen – eher selten, zumal es sich um ein fettlösliches Vitamin handelt und die Speicherreserven des Körpers damit nicht so rasch erschöpft werden wie im Fall der wasserlöslichen Vitamine. Leber- und chronische Magen- und Darmerkrankungen (Diarrhöe) fördern einen Vitamin K-Mangel; übermäßiger Alkoholkonsum kann ein Grund dafür sein. Durch die orale Einnahme von Antibiotika (Wachstumshemmung der Vitamin K liefernden Darmbakterien) kann es aber zur Hemmung der körpereigenen Blutbildung kommen; dies passiert aber nur bei gleichzeitiger Mangelernährung. Weiterhin kommt es auch häufig bei Osteoporose, wo ein erhöhter Verlust von Calcium typisch ist, zu einem Vitamin K-Mangel. Wie auch bei anderen fettlöslichen Vitaminen, kann es bei einer intestinalen Fettresorptionsstörung (beispielsweise bei Gallengangsverschluss) zu Mangelerscheinungen kommen. Kommt es aber zu einem Mangel an Vitamin K, so tritt eine Verlängerung der Blutgerinnung ein. Bei Säuglingen kann es zu Hirnblutungen kommen. Verdauungsstörungen, chronische Lebererkrankungen und Blutungen in verschiedenen Geweben und Organen, wie beispielsweise an der Nasenschleimhaut, im Magen-Darm-Trakt und in der Muskulatur, sind möglich.
Folgen einer Überdosierung (Hypervitaminose)
Da Vitamin K keine toxische Wirkung aufweist (für ein 500faches der empfohlenen Menge sind keine toxischen Wirkungen bekannt), treten kaum negative Wirkungen bei Überdosierungen auf. Nach Injektion von Vitamin K in sehr hohen Dosen können allergische Reaktionen und Veränderungen der Blutzusammensetzung auftreten. Einige Menschen haben einen Gendefekt, bei dem es durch Überdosierung von Vitamin K zu Thrombosen kommen kann. Ein Gentest dafür ist verfügbar.
Antagonisten
Man weiß, dass Vitamin K zur Synthese von Gerinnungsfaktoren (Prothrombin) unerlässlich ist. Die Gegenwart von Vitamin-K-Antagonisten (z.B. Warfarin, Dicumarol) klärte die Wirkungsweise dieses Vitamins erstmalig auf. So führte das in verdorbenem Klee vorhandene Dicumarol zu lebensgefährlichen Blutungen bei Rindern. Warfarin findet auch als Rattengift Verwendung. Mit Dicumarol gefütterte Kühe besitzen ein abnormes Prothrombin, das anders als das normale Prothrombin kein Ca2+ mehr bindet. Dies kommt durch die Änderung einer Aminosäure im Prothrombin zustande.
Als Medikament zur Blutgerinnungshemmung wird häufig Phenprocoumon als Antagonist verwendet.
Geschichte
1929 wurde Vitamin K aus Luzerne isoliert. Im Jahre 1943 erhielten Henrik Dam – für die Entdeckung – und Edward Adelbert Doisy – für die Aufdeckung der chemischen Natur des Vitamins K – den gemeinsamen Nobelpreis für Medizin.
Quellen
- ↑ M. J. Shearer: Vitamin K. In: Lancet 345, 1998, S. 229–234.
- ↑ R. T. Weibert et al.: Correction of Excessive Anticoagulation with Low-Dose Oral Vitamin K. In: Annals of Internal Medicine 126, 1997, S. 959–962.
- ↑ C. Vermeer: Role of Vitamin K in bone metabolism. In: Annu. Rev. Nutr. 15, 1995, S. 1–22.
- ↑ D. Feskanich et al.: Vitamin K intake and hip fractures in women: a prospective study. In: Am. J. Clin. Nutr. 69, 1999, S. 74–79.
- ↑ F. MacMillan et al.: Orientation of the Phylloquinone Electron Acceptor Anion Radical in Photosystem I. In: Biochemistry 36, 1997, S. 9297–9303.
Weblinks
- Fachartikel: Wie gefährlich ist Vitamin K3?
- Informationsquelle über Vitamin K1
- Vitamin-K-Gehalt von Lebensmitteln
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.