- Woodward-cis-Hydroxylierung
-
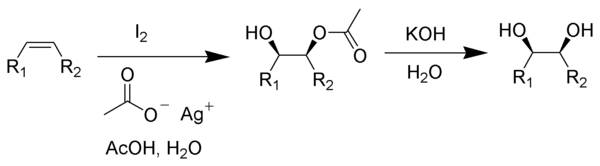
Die Prévost-Woodward-Hydroxylierung (auch: Woodward-cis-Hydroxylierung oder Woodward-Variante) ist eine chemische Reaktion, bei der sich unter milden chemischen Bedingungen zwei Hydroxylgruppen an Alkene addieren lassen können. Im Gegensatz zur Prévost-Hydroxylierung werden bei dieser Reaktion beide Hydroxylgruppen syn zueinander addiert.
Benannt ist diese Reaktion u. a. nach Robert Burns Woodward, der diese Reaktion 1958 im Journal of the American Chemical Society veröffentlichte.
Mechanismus
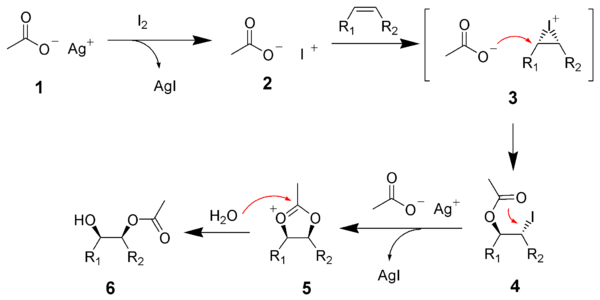
Zuerst wird das zu hydroxylierende Alken in Essigsäure und Wasser mit elementarem Iod und einem Silbercarboxylat (etwa Silberbenzoat oder Silberacetat) im molaren Verhältnis 1:1 versetzt, wobei sich analog zu der Prévost-Hydroxylierung ein β-Iodcarboxylat bildet. Die Addition von Iod und Carboxyloat verläuft anti.
Für die Folgereaktion existieren z. Zt. zwei Erklärungsansätze:
- Die im Molekül neu entstandene Iod-Gruppe wird durch Wasser (besser: Hydroxid-Ion) nukleophil substituiert. Die Substitution wird hierbei durch das Vorhandensein von Wasser und dadurch bedingter Solvatisierung der Ester-Gruppe nicht durch Nachbargruppeneffekte gesteuert. Es erfolgt dadurch eine normale SN2-Reaktion. Diese so entstandene Hydroxyl-Gruppe steht nun syn zu der Carboxylat-Gruppe.
- Durch Nachbargruppeneffekte wird die vorhandene Iod-Gruppe intramolekular durch den Carbonylsauerstoff der Ester-Gruppe substituiert (SN2), wobei intermediär ein Kation entsteht. Nun wird ein Hydroxid-Ion an das positive C-Atom der Ester-Gruppe addiert. Durch Umlagerung bildet sich die Benzoatgruppe zurück und es entsteht eine Hydroxylgruppe in syn-Position.
Beide Ansätze bedürfen einer genaueren Betrachtung, da sie teilweise im Widerspruch zueinander stehen.
Im letzten Schritt wird die Ester-Gruppe hydrolysiert. Da die Hydrolyse die Konfiguration des Moleküls nicht verändert, bleiben die so entstandenen Hydroxylgruppen syn zueinander.
Durch Wechsel der Ausgangssubstanzen (andere Halogene, Thallium(I)-acetat oder -benzoat) kann die chemische Ausbeute erhöht werden.
Anwendung
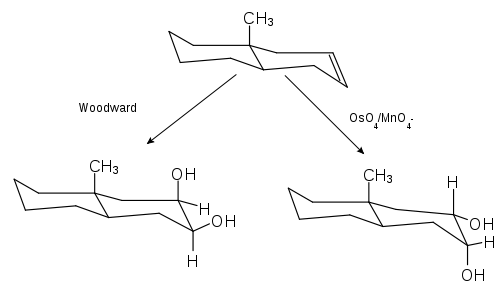
Die Prévost-Woodward-Hydroxylierung eignet sich sehr gut als Alternative zu den üblichen Dihydroxylierungsreaktionen mit Kaliumpermanganat bzw. Osmiumtetroxid, da im Gegensatz zu denen hier das sterisch ungünstigere Produkt entsteht. Es greift hier zuerst das Halogen an der sterisch günstigeren Seite des Alkens an, dann wird das Benzoat an der sterisch ungünstigeren Seite addiert.
Literatur
- Michael B. Smith, Jerry March, March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, 5th Edition, Wiley-Interscience, New York, 2001, 1049-1050
- Woodward, R. B.; Brutcher, F. V. J. Am. Chem. Soc. 1958, 80, 209. (doi:10.1021/ja01534a053)
- http://www.chemieonline.de/campus/namensreaktion.php?action=detail&id=166
Wikimedia Foundation.