- Xenotransplantation
-
Bei einer Xenotransplantation (griechisch ξένος, xénos: Fremder) handelt es sich um die Übertragung von lebens- und funktionstüchtigen Zellen oder Zellverbänden (einschließlich ganzer Organe oder Körperteile) zwischen verschiedenen Spezies.
Hiervon ist die Allotransplantation abzugrenzen, bei der die Übertragung zwischen genetisch verschiedenen Individuen derselben Spezies durchgeführt wird.
Durch die nur begrenzte Verfügbarkeit von Spenderorganen für die Allotransplantation, verspricht die Xenotransplantation eine mögliche Alternative zu werden. Herzklappen von Schweinen werden schon heute als mögliche Alternative zu mechanischen verwendet. Dabei werden die Herzklappen jedoch so bearbeitet, dass sie kein Antigen an der Oberfläche tragen, das als fremd erkannt werden könnte. Jedoch sind bis heute ganze Organ-Xenotransplantationen beim Menschen nicht möglich.
Obwohl Primaten viel näher zum Menschen verwandt sind, werden heute Schweine als die vielversprechendste Möglichkeit für Organtransplantationen gehandelt. Schweineorgane sind physiologisch besser geeignet den Anforderungen an den menschlichen Körper zu genügen. Die erste Herz-Xenotransplantation an einem Menschen mit einem Schimpansenherzen zeigte, dass das Herz zu klein war, um die Blutzirkulation aufrechtzuerhalten (Hardy, Mississippi 1964). Schweineherzen dagegen haben eine ausreichende Funktion der linken Herzkammer, um einen Menschen am Leben zu erhalten und sind zudem noch klein genug, um in den Thorax zu passen.[1]
Inhaltsverzeichnis
Mechanismen der Abstoßungsreaktion[2]
Die Abstoßungsreaktion kann grob in vier verschiedene Zeitabschnitte eingeteilt werden:
- HAR
- AVR
- AHXR
- chronische Abstoßung
Hyperakute Abstoßung (HAR - hyperacute rejection)
Die erste Stufe der Abstoßungsreaktion erfolgt schon innerhalb der ersten 24 Stunden. Hier richten sich schon gebildete Antikörper gegen die Endothelzellen des Implantats. Durch die Anlagerung von diesen IgG Antikörpern kommt es zu Komplementaktivierung, Schwellung des Endothels und mikrovaskulärer Thrombose.
Die hier zum Tragen kommenden Antikörper richten sich gegen die Galα1,3Galβ1,4GlcNAc (αGal) Kohlenhydratseitenketten der Endothelzellen des Schweines. Diese Seitenketten befinden sich auf den Endothelzellen von nicht-primaten Säugetieren als auch Neuweltaffen und sind nicht vorhanden beim Menschen und Altweltaffen. Durch natürliche Infektionen des Gastrointestinaltraktes mit αGal exprimierenden Mikroorganismen bildet der menschliche Körper schon sehr früh Antikörper gegen diese Kohlenhydrate. Um diese Art der Abstoßung abzuwenden, gelang es 2002 ein sogenanntes k. o.-Schwein (αGal -/-) für dieses Kohlenhydrat zu generieren, mit dem die nächsten Phasen der Abstoßung erreicht werden konnten.
Akute Gefäßabstoßung (AVR – acute vascular rejection)
Dieser Abschnitt der Abstoßung, der innerhalb von ein paar Tagen eintritt, ist ähnlich der HAR, jedoch sind hier noch Zellen des angeborenen Immunsystems involviert, wie NK Zellen, Makrophagen und Neutrophile Granulozyten.
Akute humorale Xenotransplantatabstoßung (AHXR – acute humoral xenograft rejection)
In dieser Phase werden neue Antikörper gegen das Xenotransplantat gebildet, die sich nicht gegen αGal richten. Auch hier wird sowohl Komplement aktiviert, als auch das Blutgerinnungssystem.
Chronische Abstoßung
In der letzten experimentell erreichten Phase der Xenotransplantation kommt es zur Entwicklung einer Thrombotischen Mikroangiopathie.
Gefahren und ethische Bedenken
Die größte Befürchtung bei der Anwendung von Xenotransplantaten ist das Risiko des Übertragens von tierischen Pathogenen auf den Wirt und auf die gesamte Menschheit. Es gibt Beobachtungen, dass endogene Schweineretroviren (PERVs – porcine endogenous retrovirus) auf menschliche Zelllinien übertragen werden können.[3] Jedoch gibt es bis heute noch keinen Beweis, dass dies auch in vivo geschehen kann.[4] Es gibt verschiedene ethische Bedenken bei der Xenotransplantation. Im Unterschied zu allen anderen medizinischen Eingriffen wird hier eine so genannte Chimäre gebildet, die lebende Zellen von zwei verschiedenen Spezies enthält.[5] Auch aus religiöser Sicht gibt es unterschiedliche Bedenken. Auf dem XVIII International Congress of the Transplantation Society in Rom 2000 hat Papst Johannes Paul II dem Gebrauch von Schweinen als Organspender zugestimmt.
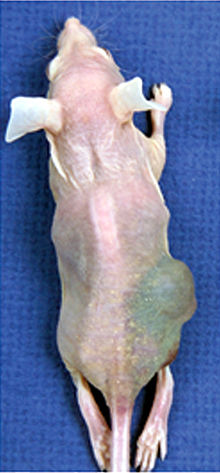
Die Xenotransplantation von menschlichem Gewebe, wie beispielsweise Tumorzellen, auf Versuchstiere – insbesondere Nacktmäuse – (sogenannte Xenografts) ist seit 1972 ein in der präklinischen Forschung etabliertes Verfahren.
Literatur
- Jorge Guerra González: Infection Risk and Limitation of Fundamental Rights by Animal-To-Human Transplantations. EU, Spanish and German Law with Special Consideration of English Law. Verlag Dr. Kovac, Hamburg 2010, ISBN 978-3-8300-4712-4.
Einzelnachweise
- ↑ Allan JS, Rose GA, Choo JK et al. Morphometric analysis of miniature swine hearts as potential human xenografts. Xenotransplantation 2001; 8: 90-93. PMID 11328578
- ↑ B Sprangers et al. Xenotransplantation: Where are we in 2008? Kidney International 2008; 74: 14-21. PMID 18418354
- ↑ Bach FH, Fishman JA, Daniels N et al. Uncertainty in xenotransplantation: individual benefit versus collective risk. Nat Med 1998; 4: 141-144. PMID 9461178
- ↑ Fishman JA, Patience C. Xenotransplantation: infectious risk revisited. Am J Transplant 2004; 4: 1383-1390. PMID 15307825
- ↑ George JF. Xenotransplantation: an ethical dilemma. Curr Opin Cardiol 2006; 21: 138-141. PMID 16470151
Siehe auch
Weblinks

Bitte den Hinweis zu Gesundheitsthemen beachten!
Wikimedia Foundation.