- Ziagen
-
Strukturformel 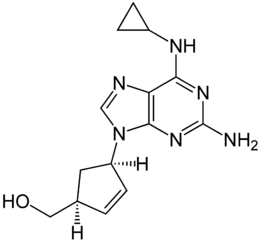
Allgemeines Freiname Abacavir Andere Namen - (1S,4R)-4-[2-Amino- 6-(cyclopropylamino)-9H-purin-9-yl]-2-cyclopenten-1-methanol
- (1S,4R)-4-[2-Amino- 6-(cyclopropylamino)-9H-purin-9-yl]cyclopent-2-en-1-methanol
Summenformel - C14H18N6O (Abacavir)
- (C14H18N6O)2·H2SO4 (2 Abacavir·H2SO4)
CAS-Nummer - 136470-78-5 (Abacavir)
- 188062-50-2 (2 Abacavir·H2SO4)
PubChem 441300 ATC-Code J05AF06
DrugBank DB01048 Arzneistoffangaben Wirkstoffklasse Virustatikum, nukleosidische Reverse-Transkriptase-Inhibitoren
Wirkmechanismus Fertigpräparate Ziagen® (D, A, CH)
Verschreibungspflichtig: Ja Eigenschaften Molare Masse Schmelzpunkt 165 °C (Abacavir) [1]
Sicherheitshinweise Gefahrstoffkennzeichnung
unbekanntR- und S-Sätze R: ? S: ? Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Abacavir (Handelsname Ziagen; Hersteller GlaxoSmithKline) ist ein Arzneistoff zur Behandlung von mit HIV-1 infizierten Patienten im Rahmen einer antiretroviralen Kombinationstherapie. Er gehört zur Gruppe der nukleosidischen Reverse-Trankriptase-Inhibitoren (NRTI).
Eine Besonderheit ist, dass das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) für Abacavir erstmals die Erlaubnis zur Verordnung eines Arzneimittels, an einen vorherigen Gentest bindet. Bei diesem Test wird das Vorhandensein des Genmarkers HLA-B*5701 überprüft. Bei Patienten mit diesem Genmarker kommt es zu teilweise lebensbedrohlichen Überempfindlichkeitsreaktionen.
Inhaltsverzeichnis
Pharmakologie
Abacavir wird zunächst in das Triphosphat umgewandelt. Zusätzlich wird der Basenanteil metabolisiert. Als biologisch aktives Stoffwechselprodukt entsteht Carbovir-triphosphat. Dieser hemmt die reverse Transkriptase. Es wirkt in vitro teilweise synergistisch mit Nukleosiden und Proteaseinhibitoren.
Pharmakokinetik
Die Bioverfügbarkeit liegt > 70 %. Die Eliminationshalbwertzeit wird mit ca. 1,5 Stunden berechnet. Für das aktive Triphosphat wird die intrazelluläre Halbwertzeit mit 3 bis 4 Stunden angegeben. Die Einnahme erfolgt in zwei täglichen Einzeldosen zu 300 mg. Die Resorption ist von den Mahlzeiten unabhängig. Bei regelmäßiger Anwendung sind maximale Spiegel von 3,0 ± 0,9 mg/l angegeben, als AUC-Wert wurde 6,0 ± 1,7 mg/l x h berechnet. Die Konzentration im Liquor entspricht ca. 1/3 der Plasmakonzentrationen. Abacavir wird überwiegend (ca. 85 %) matbolisiert mit dem Urin ausgeschieden. Der Arzneistoff wird nicht durch das Cytochrom P450-System verstoffwechselt. Es besteht kein entsprechendes Interaktionspotential.
Nebenwirkungen
Wichtigste Nebenwirkung ist eine Überempfindlichkeitsreaktion (ca. 5 %). Symptome: Fieber, Exanthem, Abgeschlagenheit und gastrointestinale Symptome. Die Beschwerden treten i.d.R. zwischen der ersten und vierten Behandlungswoche auf. Nach Absetzen des Medikamentes, sind die Beschwerden innerhalb von ein bis zwei Tagen rückläufig. Abacavir darf danach nicht noch einmal verabreicht werden! Eine schwere lebensbedrohliche Überempfindlichkeitsreaktion mit Blutdruckabfall trat gehäuft innerhalb von ein bis zwei Stunden auf. Selten: Laktatazidose, Hepatomegalie.
Abacavir wird über das Enzym Alkohol-Dehydrogenase abgebaut. Plasmakonzentrationen können erhöht sein, wenn gleichzeitig Alkohol konsumiert wird. Wechselwirkungen mit Zidovudin oder Lamivudin sind gering. Interaktionen mit dem Cytochrom P450-System sind unwahrscheinlich.
Resistenzen
Über die Mechanismen der Resistenzentwicklung sind Details bekannt. Veränderungen der Aminosäuren 65, 74, 115 und 184 der reversen Transkriptase sind mit einer Reduktion der Empfindlichkeit assoziiert. Auch ähnliche Nukleoside wie Zalcitabin und Didanosin sind gegen solche Stämme in der Regel weniger wirksam. Um der Resistenzbildung entgegen zu wirken ist die Kombination im Rahmen einer HAART zwingend erforderlich.
Stereoisomerie
Abacavir ist chiral und enthält in 1- und in 4-Position des Cyclopentenylrings zwei stereogene Zentren. Also existieren vier Stereoisomere: Die (1S,4S)-Form, die (1R,4R)-Form, die (1R,4S)-Form und die (1S,4R)-Form. Wegen der unterschiedlichen physiologischen Wirkungen dieser Stereoisomeren, wird als Arzneistoff ausschließlich die (1S,4R)-Form von Abacavir eingesetzt.[2]
Einzelnachweise
- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1, ISBN 978-0-911910-00-1.
- ↑ ROTE LISTE 2008, Verlag Rote Liste Service GmbH, Frankfurt am Main, Seite 31, ISBN 978-3-939192-20-6.
Weblinks
- AIDSMeds.com
- Angaben des Herstellers
- Artikel zum Thema DER ARZNEIMITTELBRIEF: unabhängige Zeitschrift, Schwerpunkt Pharmakotherapie.
Bitte beachte den Hinweis zu Gesundheitsthemen!
Wikimedia Foundation.
