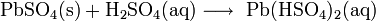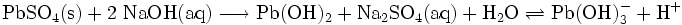- Bleisulfat
-
Strukturformel Pb2+ 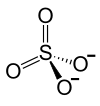
Allgemeines Name Blei(II)-sulfat Andere Namen - Plumbosulfat
- Bleivitriol
Summenformel PbSO4 CAS-Nummer 7446-14-2
15739-80-7 (als Schwefelsäure-Bleisalz)
12202-17-4 (als dreibasisches Bleisulfat PbSO4•3(PbO)Kurzbeschreibung weißer kristalliner Feststoff Eigenschaften Molare Masse 303,26 g/mol Aggregatzustand fest
Dichte 6,2 g/cm3 [1]
Schmelzpunkt 1170 °C[1]
Löslichkeit schlecht löslich in Wasser (0,045 g/l)[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Giftig Umwelt-
gefährlich(T) (N) R- und S-Sätze R: 61-20/22-33-62-50/53 S: 53-45-60-61 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Blei(II)-sulfat (PbSO4), ein weißer kristalliner Feststoff, ist das Blei(II)-Salz der Schwefelsäure.
Inhaltsverzeichnis
Vorkommen
In der Natur findet man Blei(II)-sulfat in Form von rhombischem, diamantglänzendem Anglesit (Vitriolbleierz). In reinem Zustand spricht man auch von "Bleiglas".
Bei der Entladung von Bleiakkumulatoren bildet sich Blei(II)-sulfat:
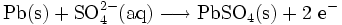
- Am Minuspol des Akkumulators wird Blei in Bleisulfat umgewandelt.
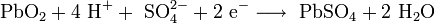
- Am Pluspol entsteht aus Blei(IV)-oxid und Sulfat Bleisulfat.
Darstellung
Das in Wasser weitgehend unlösliche Blei(II)-sulfat entsteht als weißer Niederschlag bei der Reaktion löslicher Blei(II)-salze wie Blei(II)-nitrat oder Blei(II)-acetat mit löslichen Sulfaten wie Natriumsulfat oder Schwefelsäure:
Eigenschaften
Die Bleiverbindung ist ein Feststoff mit einer relativ hohen Dichte von 6,35 g/cm3. In Wasser ist sie nahezu unlöslich, in konzentrierter Schwefelsäure und starken Säuren löst sie sich gut.
Deswegen enthält Schwefelsäure, die nach dem Bleikammerverfahren gewonnen wird, Blei(II)-sulfat, das beim Verdünnen der Säure größtenteils wieder ausfällt.
Konzentrierte Alkalilaugen vermögen Blei(II)-sulfat unter Bildung von Alkalihydroxoplumbiten zu lösen.
Verwendung
Blei(II)-sulfat wurde als weiße Malerfarbe verwendet. Ihr Vorteil liegt darin, dass sie gegen Licht und Luft beständig ist. Nachteilig ist dagegen, dass die Farbe schlechter deckt und trocknet als zum Beispiel Bleiweiß. Schwefelwasserstoff und Bleisulfidbildung führen zu einem Nachdunkeln. Darüber hinaus wird Blei(II)-sulfat für die Herstellung von Leinölfirnis sowie als Beschwerungsmittel verwendet. Blei(II)-sulfat darf wegen seiner Giftigkeit in Deutschland nicht mehr frei verkauft werden.
Das Ausfällen von Blei(II)-sulfat durch Versetzen von Bleisalzlösungen mit verdünnter Schwefelsäure wird in der Analytik zur quantitativen Bestimmung von Blei genutzt.
Quellen
Wikimedia Foundation.

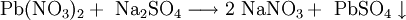
_sulfate.jpg)