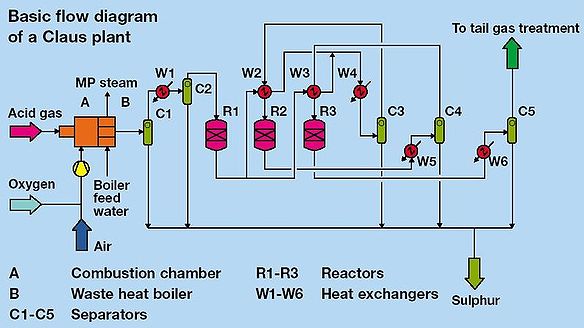
- Claus-Anlage
-
Der Claus-Prozess ist ein Verfahren zur industriellen Herstellung von Schwefel aus Schwefelwasserstoff. Schwefelwasserstoff entsteht beispielsweise bei der Herstellung von Steinkohlenkoks als Bestandteil des Kokereigases oder bei der Entschwefelung von Erdöl in Raffinerien.
Inhaltsverzeichnis
Chemisch-technisches Verfahren
Chemische Reaktion
Der grundlegende chemische Prozess besteht aus zwei Schritten:[1]:
- Ein Drittel des Schwefelwasserstoffs wird zu Schwefeldioxid verbrannt:
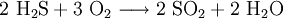 : ΔH = -4147,2 kJ/mol
: ΔH = -4147,2 kJ/mol - Die restlichen 2/3 des Schwefelwasserstoffs reagieren mit dem SO2 zu Schwefel (Komproportionierung):
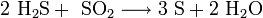 : ΔH = -1165,6 kJ/mol
: ΔH = -1165,6 kJ/mol
Verfahrenstechnik
Das technische Verfahren lässt sich in vier Stufen zerlegen:
- Im Hauptbrenner wird durch substöchiometrisches Verbrennen des H2S mit Luft (auch Luft/Reinsauerstoff-Gemische möglich) die benötigte Menge SO2 erzeugt (Reaktion 1., ca. 1100 °C). Das SO2 reagiert bereits hier zum Großteil mit dem restlichen H2S zu Schwefel (Reaktion 2.). Hinter dem Hauptbrenner wird das Gas abgekühlt (auf ca. 140 °C), so dass der erzeugte flüssige Schwefel abgeschieden werden kann (ca. 60–70 % der erzeugten Schwefelmenge).
- In zwei aufeinanderfolgenden katalytischen Stufen (Bauxit-Katalysator, ca. 250 °C) wird nach Reaktion 2. weiterer Schwefel gewonnen. Die gesamte Ausbeute an Schwefel beträgt für diese prozesstechnische Konstellation 95 % (Schwefelrückhaltungsgrad), denn Reaktion 2. läuft nicht vollständig ab (es existieren auch Claus-Anlagen, bei denen drei katalytische Stufen den Schwefelrückhaltungsgrad auf etwa 97 % anheben können).
- Im Abgas hinter der zweiten katalytischen Stufe befindet sich neben SO2 immer noch H2S, welches entweder in einem thermischen (~900 °C) oder katalytischen (~400 °C) Incinerator verbrannt wird (Reaktion 1.) um Emissionen von H2S zu vermeiden.
Die Einhaltung der Stöchiometrie ist extrem wichtig, da sonst überschüssiges SO2 bzw. H2S (im nachfolgenden Incinerator zu SO2 verbrannt) die Umwelt belastet.
Um den Schwefelrückhaltungsgrad weiter zu steigern, sind diverse Verfahren entwickelt worden, die das Abgas hinter den katalytischen Stufen von Schwefelverbindungen reinigen. Das bekannteste ist das sogenannte SCOT-Verfahren (Shell Claus Offgas Treating).
SCOT-Verfahren
SO2, das im Claus-Verfahren nicht zu Schwefel umgesetzt wurde, wird im SCOT-Verfahren zu H2S hydriert:
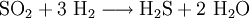 : ΔH = -339,6 kJ/mol
: ΔH = -339,6 kJ/mol
und zusammen mit dem ebenfalls nicht umgesetzten H2S der zweiten katalytischen Stufe über eine Aminwäsche aus dem Abgasstrom entfernt. Das absorbierte H2S wird wieder freigesetzt und zum Einsatz der Clausanlage zurückgeführt (recycled). Das Abgas wird anschließend wegen der - wenn auch geringen - Spuren an H2S ebenfalls incineriert. Ein guter Schwefelrückhaltungsgrad einer Claus/SCOT-Kombination liegt bei 99,8 %.
Regenerative Rauchgasentschwefelung
Bei regenerativen Verfahren zur Rauchgasentschwefelung (z. B. Wellmann-Lord-Verfahren) entsteht SO2, das direkt in eine (vorhandene) Claus-Anlage geleitet werden kann. Hierdurch wird die zusätzliche Investition für die SO2-Aufarbeitung (Hydrierung) gespart. Speziell für Raffinerien ist dies eine interessante Lösung.[2]
Quellenangaben
- ↑ Charles E. Mortimer, Ulrich Müller: Chemie. Das Basiswissen der Chemie. Thieme, Stuttgart 2003, ISBN 3-13-484308-0, S. 411–412.
- ↑ "PCK Schwedt"
Weblinks
- SCOT-Prozess (PDF)
- Schwefelemissionen (PDF)
- Ein Drittel des Schwefelwasserstoffs wird zu Schwefeldioxid verbrannt:
Wikimedia Foundation.