- Entzündbar
-
Dieser Artikel wurde aufgrund von Mängeln auf der Qualitätssicherungsseite der Redaktion Chemie eingetragen. Dies geschieht, um die Qualität der Artikel aus dem Themengebiet Chemie auf ein akzeptables Niveau zu bringen. Dabei können Artikel gelöscht werden, die nicht signifikant verbessert werden können. Hilf mit, die Mängel dieses Artikels zu beseitigen, und beteilige dich an der Diskussion. Eine Verbrennung ist eine Redoxreaktion, die exotherm, d. h. unter Abgabe von Energie in Form von Wärme und Licht abläuft.
Im allgemeinen Sprachgebrauch versteht man unter Verbrennung die Redoxreaktion eines Materials mit Luftsauerstoff. Verbrennungen gibt es aber auch bei Reaktionen ohne Sauerstoff, beispielsweise der Reaktion von Fluor und Wasserstoff zu Fluorwasserstoff.
Inhaltsverzeichnis
Begriffe, Einteilung
Zu unterscheiden sind:
- Verbrennung in Form eines Feuers mit Flammenerscheinung aus glühenden flüchtigen Stoffen; brennen feste Stoffe mit Flamme, so wird diese durch verbrennende gasförmige Pyrolyseprodukte gebildet
- Verbrennung in Form von Glut (ohne glühende flüchtige Stoffe)
- als unvollständige Verbrennung bezeichnet man eine Verbrennung, bei der nicht alle möglichen Bindungen zum Oxidationsmittel entstehen (z. B. die Verbrennung von Kohlenstoff zu Kohlenmonoxyd oder Herstellung von Grillkohle, Schwelbrand, Verkoken)
- langsame und relativ kalte Oxidation, etwa beim Verrosten von Metallen oder in Lebewesen bei der „Verbrennung“, also der Oxidation von Nährstoffen.
Die Verbrennung in einem Feuer kann kontrolliert (Nutzfeuer), zum Beispiel in einem Ofen, einem Dampfkessel (Feuerung), als Lagerfeuer, oder unkontrolliert als Schadfeuer bei einem Brand erfolgen.
Verbrennungen, bei der vorgemischte Systeme mit einer hohen Verbrennungsgeschwindigkeit, nahezu schlagartig und mit enormer Volumenzunahme (der gasförmigen Bestandteile) reagieren, bezeichnet man als Explosionen. Diese werden unter Berücksichtigung der Verbrennungs- und Ausbreitungsgeschwindigkeit unterteilt in
(Siehe auch Abbrandgeschwindigkeit der Pyrotechnik, Brisanz).
Die Einleitung des Brennvorgangs, das Zünden (Zuführen der Aktivierungsenergie), wird verschieden bezeichnet: Während allgemein Verbrennungen entzündet werden, werden insbesondere Feuer, Deflagrationen, u. a. angezündet, Detonationen gezündet (siehe Zünder), Dämpfe und Gase entflammt.
Brände werden in der Brandlehre in fünf verschiedene Brandklassen eingeteilt:
Brandklasse A: Brände fester Stoffe
Brandklasse B: Brände flüssiger oder flüssig werdender Stoffe
Brandklasse C: Brände gasförmiger Stoffe
Brandklasse D: Metallbrände
Brandklasse F: Brände von pflanzlichen Ölen und Fetten in Fettbackgeräten.Verlauf
Bei der Verbrennung reagiert eine Substanz, der Brennstoff, chemisch mit Sauerstoff oder (selten) einem anderen Gas. Der Brennstoff kann fest (beispielsweise Holz, Kohle), flüssig (Benzin, Alkohol), flüssig werdend (Wachs) oder gasförmig (Methangas, Erdgas) sein.
Sobald eine kleine Brennstoffmenge reagiert hat, bringt die dabei freigesetzte Wärme als Aktivierungsenergie weiteren Brennstoff zum Reagieren. Die Verbrennung ist in diesem Sinne eine thermische Kettenreaktion.
Das bei der Verbrennung freigesetzte Licht stammt aus den glühenden Masseteilchen. Außerdem erhöht sich typischerweise die Temperatur sehr stark, was zur Heizung oder Verrichtung von Arbeit genutzt werden kann.
Zurzeit werden in Anlagen zur Wärmeerzeugung meist Kohlenwasserstoffe mit dem Sauerstoff der Luft zur Reaktion gebracht. Es entsteht dabei Abgas, das (neben dem Luftstickstoff) hauptsächlich Kohlenstoffdioxid (CO2) und Wasser (H2O) enthält. Je nach Art der Verbrennungsführung können verschiedene weitere Stoffe im Abgas enthalten sein, z. B. Kohlenmonoxid (CO), Stickoxide (NOx) und unverbrannte Kohlenwasserstoffe. Bei fetter Verbrennung (Kraftstoffüberschuss) von Kohlenwasserstoffen kann außerdem Ruß entstehen.
Voraussetzungen für eine Verbrennung
Vorhanden sein muss:
- Brennbares Material in ausreichender Menge
- Oxidationsmittel, meist Sauerstoff (siehe Sauerstoffindex)
- Das richtige Mengenverhältnis des brennbaren Stoffes mit der Umgebungsluft oder dem reaktiven Gas
- eine geeignete Zündquelle
Ein Katalysator kann die Aktivierungsenergie, die für den Start der chemischen Reaktion erforderlich ist, herabsetzen. Dadurch kann die Verbrennung beschleunigt oder die zur Zündung notwendige Energie herabgesetzt werden.
Verbrennung von Holz und anderen organischen Feststoffen
Die Verbrennung von Holz beginnt mit einer Erhitzung von außen. Enthält das Holz Wasser, dann stoppt die Temperaturerhöhung oberhalb von 100 °C (je nach Siedepunktserhöhung durch gelöste Stoffe). Erst wenn das meiste Wasser verdampft ist, kann sich die Temperatur weiter erhöhen und die Verbrennung beginnen. Für die Verdampfung von Wasser müssen große Wärmemengen zugeführt werden. Weil Holz ungefähr das eigene Gewicht an Wassermengen speichern kann, ist das Anzünden von feuchtem oder nassem Holz langwierig bis unmöglich. Ist das Holz getrocknet, so erhöht sich die Temperatur weiter, bis das Holz ab etwa 150 °C beginnt zu verkohlen. Hierbei verwandelt sich das Holz durch hitzebedingte chemische Zersetzung (Pyrolyse) zum Teil in gasförmige Stoffe, die aus dem Holz austreten und in einer Flamme verbrennen. Die zurückbleibende Holzkohle (Gemisch aus Kohlenstoff und Asche) verglüht anschließend.
Luftzahl
Für die Verbrennung an Luft wird die sogenannte Luftzahl benötigt. Diese ist ein Verhältniswert aus den Anteilen der Umgebungsluft, hauptsächlich also Sauerstoff und Stickstoff:
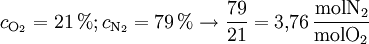
Sauerstoffbedarf
Bezogen auf 1 mol Brennstoff erhält man den zur vollständigen Verbrennung erforderlichen Anteil Sauerstoff νO2 über:
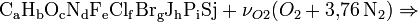
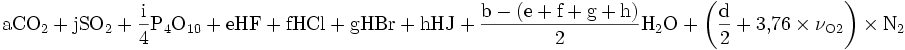
Löst man obige Gleichung nach νO2 auf, so erhält man:
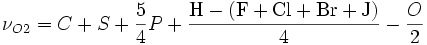 beziehungsweise
beziehungsweise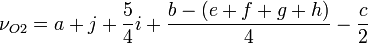 , wobei die Kleinbuchstaben die Anzahl der im Brandstoff enthaltenen Elemente angeben.
, wobei die Kleinbuchstaben die Anzahl der im Brandstoff enthaltenen Elemente angeben.stöchiometrische Konzentrationen
Die für die vollständige Verbrennung rechnerisch nötige Konzentration von Brennstoff erhält man über
![\mathrm {c_{stoech}={100 \over 1+(1+3{,}76)\times\nu_{O 2}}\,[Vol%]}](/pictures/dewiki/57/92eed2bded45e0c9663be975eae37d06.png) beziehungsweise
beziehungsweise![\mathrm {c_{stoech}={Vol% \times 124\times10^{-2} \over (0{,}02405)}}\,[g/m^3]](/pictures/dewiki/52/4a2bbb499c0b86bd77f4256fb3b9051d.png)
Beispiel
Als Beispiel ist hier die vollständige Verbrennung von Propanol (C3H8O) genannt:
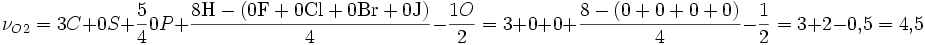
Somit sind zur vollständigen Verbrennung von 1mol Propanol 4,5 mol Sauerstoff nötig. Weiterhin lässt sich die stöchiometrische Konzentration, die für die Verbrennung nötig ist, berechnen:
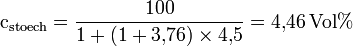 beziehungsweise
beziehungsweise 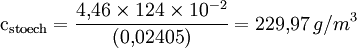
Verbrennungsgeschwindigkeit
Beim brennbaren Material kann es nur zur Oxidation kommen, wenn ein einzelnes Atom oder Molekül des Brennstoffs mit Sauerstoff in direkten Kontakt kommt. Daher sind für die Verbrennungsgeschwindigkeit (Abbrandgeschwindigkeit) die Verfügbarkeit von Sauerstoff und sein inniger Kontakt mit dem Brennmaterial maßgeblich.
Die Versorgung mit Sauerstoff kann man durch stete Zufuhr von Frischluft erreichen, indem man z. B. in ein Holzfeuer bläst. Für Holzfeuer ist der Kamin dabei ein ideales Hilfsmittel. In dem sich verengenden Kaminrohr steigen die erwärmten Abgase schnell auf und erzeugen einen steten Unterdruck um das Feuer. Dieser saugt permanent frische Luft heran. Eine extreme Ausprägung sind der Feuersturm bzw. Waldbrände, die durch Winde, z. B. den Mistral, angefacht werden.
Einige Löschverfahren beruhen darauf, die Sauerstoffzufuhr zu unterbrechen (Löschdecke, Schaum, CO2-Löschanlage …).
Um den innigen Kontakt herzustellen, muss man die Oberfläche des Brennstoffs vergrößern. Ideal ist es dabei, den Brennstoff in ein Gas zu verwandeln. Das geschieht bei der Kerze: Am Boden des Dochts schmilzt Wachs, steigt dann als Flüssigkeit auf und verdampft an der heißen Spitze. Das verdampfte Wachs verbrennt schließlich.
Ein weiteres anschauliches Beispiel ist die Mehlstaubexplosion: Wird etwas Mehl in eine Kerzenflamme geblasen, wird das ansonsten unbrennbare Mehl durch die Zerstäubung brennbar und reagiert heftig. Beim Ottomotor und Dieselmotor erfolgt ebenfalls eine Verdampfung bzw. Zerstäubung. Flüssiger Dieselkraftstoff ist bei Raumtemperatur nicht leicht entflammbar. Erst durch Zerstäubung durch eine Einspritzanlage und schlagartige Erhitzung durch die Verdichtung im Verbrennungsraum zündet er selbst und verbrennt. Über allen Flüssigkeiten steht in Abhängigkeit von der Stoffeigenschaft spezifischer Dampfdruck und den Umgebungsfaktoren Druck und Temperatur eine Dampfwolke. Handelt es sich um eine brennbare Flüssigkeit ist diese Dampfschicht in einem bestimmten Bereich (zwischen unterer und oberer Explosionsgrenze) entzündlich. Benzin z.B. hat einen niedrigen spezifischen Dampfdruck und ist daher relativ leicht flüchtig, bildet also auch schon bei niedrigen Temperaturen eine brennbare Dampfschicht über seiner Oberfläche aus.
In einigen chemischen Verbindungen sind das „Oxidationsmittel“ (Sauerstoff) und das zu oxidierende „Material“ in demselben Molekül untergebracht, so z. B. in vielen Sprengstoffen. Das „Nitroglyzerin“ mit der Summenformel C3H5N3O9 enthält pro Molekül 9 Sauerstoffatome (in drei Nitrat- bzw. [Ester|Salpetersäureester]]-Gruppen) und damit mehr als genug, um die im Molekül enthaltenen Kohlen- und Wasserstoffatome vollständig zu Kohlendioxid und Wasser zu oxidieren. Die instabile Verbindung zerfällt explosionsartig schon bei leichten Erschütterungen; die gasförmigen Oxidationsprodukte bilden blitzartig ein Vielfaches des ursprünglichen Volumens und dadurch extrem hohen Druck, worauf die Wirkung dieses Sprengstoffs und aller anderen beruht.
Auch die Treibsätze von Feststoffraketen bringen den Sauerstoff selbst mit, weil es ihn im Vakuum des Weltalls nicht gibt.
Literatur
- J. Warnatz, U. Maas, R. W. Dibble, Verbrennung, 3. Aufl., Springer: Berlin etc. 2001 ISBN 3-540-42128-9
- Rodewald, Brandlehre, 6. Aufl., W. Kohlhammer GmbH, Stuttgart 2007, ISBN 978-3-17-019129-7
- Drysdale, An Introduction to Fire Dynamics Second Edition 1998, John Wiley & Sons, Ltd, The Atrium, Southern Gate, Chichester West Sussex PO19 8SQ, England, ISBN 978-0-471-97291-4
Weblinks
Wikimedia Foundation.


