- Ergotalkaloid
-
Als Mutterkornalkaloide (Ergotalkaloide, Secalealkaloide) werden verschiedene organische Verbindungen bezeichnet, die aus dem Mutterkorn, dem Sklerotium des Pilzes Claviceps purpurea, gewonnen werden können. Darüber hinaus können Mutterkornalkaloide auch von anderen Pilzen der Abteilung Schlauchpilze und von höheren Pflanzen der Familie der Windengewächse produziert werden.
Im Mittelalter waren Vergiftungen aufgrund von Mutterkornalkaloiden ein größeres Problem. Näheres dazu siehe unter Mutterkorn. Heute dienen einige Mutterkornalkaloide als Grundlage für unterschiedliche Pharmazeutika und als Bausteine für verschiedene synthetische Drogen.
Inhaltsverzeichnis
Molekülstruktur
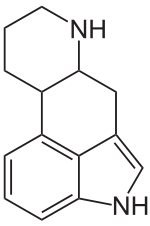
Charakteristisch für die chemische Struktur der Mutterkornalkaloide ist das tetrazyklische Ergolin. Die in der Natur gefundenen Mutterkornalkaloide können in vier Gruppen unterteilt werden: Lysergsäuren, einfache Lysergsäureamide, Ergopeptine und Clavine. Der Gehalt im Mutterkorn liegt zwischen etwa 0,2–1 % der Trockenmasse.
Lysergsäuren
Lysergsäuren, wie z. B. Lysergsäure und Paspalsäure, sind Endprodukte oder einfache Zwischenprodukte in der Biosynthese höherer Mutterkornalkaloide.
Einfache Lysergsäureamide
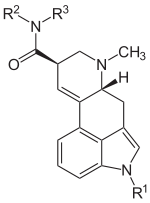
Einfache Lysergsäureamide, wie z. B. Ergometrin, werden durch den Mutterkornpilz durch Kondensation von Lysergsäure und einer Aminosäure (z. B. Alanin) gebildet. Andere einfache Lysergsäureamide, wie z. B. Ergin (Lysergsäureamid), sind Abbauprodukte höherer Mutterkornalkaloide.
Name Substituent R1 Substituent R2 Substituent R3 Ergin H H H Ergometrin H CH(CH3)CH2OH H Methergin H CH(CH2CH3)CH2OH H Methysergid CH3 CH(CH2CH3)CH2OH H LSD H CH2CH3 CH2CH3 Ergopeptine
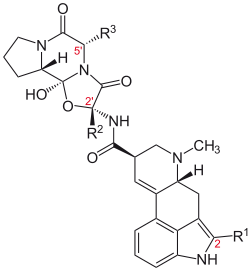
Ergopeptine sind die formenreichste Gruppe der Mutterkornalkaloide. Sie sind Kondensationsprodukte aus der Lysergsäure und einem in der Regel trizyklischen Tripeptid. Der bekannteste Vertreter ist Ergotamin, das Hauptalkaloid des Mutterkorns. Des weiteren konnten die Ergopeptine Ergocornin, Ergocristin, α-Ergokryptin, β-Ergokryptin, Ergovalin, α-Ergosin und β-Ergosin als Inhaltsstoffe des Mutterkorns identifiziert werden. Ergovalin ist ein Hauptalkaloid der endophytisch in Weidegräsern wachsenden Neotyphodium- und Epichloë-Arten und von veterinär-toxikologischer Bedeutung (Fescue toxicosis). 9,10-Dihydroergopeptine sind in der Natur sehr selten und konnten bisher nur in Sphacelia sorghi nachgewiesen werden. Partialsynthetisch gewonnene Dihydroergopeptine, wie z. B. Dihydroergotamin und Dihydroergotoxin, besitzen dem gegenüber eine therapeutische Bedeutung.
Ergopeptin Substituent R2 (Pos. 2′) Substituent R3 (Pos. 5′) Ergotamin CH3 CH2C6H5 Ergovalin CH3 CH(CH3)2 α-Ergosin CH3 CH2CH(CH3)2 β-Ergosin CH3 CH(CH3)(C2H5) Ergocristin CH(CH3)2 CH2C6H5 Ergocornin CH(CH3)2 CH(CH3)2 α-Ergokryptin CH(CH3)2 CH2CH(CH3)2 β-Ergokryptin CH(CH3)2 CH(CH3)(C2H5) Clavine
Clavine, wie z. B. Lysergol, leiten sich im Gegensatz zu allen übrigen natürlich vorkommenden Ergolinen nicht von der Lysergsäure ab, sondern von dessen Vorstufen mit einer niedrigeren Oxidationsstufe (z. B. Alkohole).
Das Mutterkorn enthält die Clavine Agroclavin, Elymoclavin, Molliclavin, Lysergin, Lysergol, Lysergen, Setoclavin, Isosetoclavin, Penniclavin, Isopenniclavin, Festuclavin, Pyroclavin, Costaclavin und Fumigaclavin A u. B. Ebenso können sogenannte Secoergoline ohne vollständige Ergolinstruktur, wie z. B. Chanoclavin, nachgewiesen werden. Sie sind biogenetische Vorstufen der Clavine.
Isoergoline
Isoergoline (Suffix: -inin, z. B. Ergotaminin) unterscheiden sich stereochemisch von Ergolinen durch einen α-ständigen Substituenten in Position 8 des Ergolingrundgerüstes. Isoergoline entstehen aus Ergolinen durch Isomerisierungsreaktionen in wässriger Lösung. Sie sind meist Abbauprodukte oder Aufarbeitungsartefakte bei der Isolierung von Mutterkornalkaloiden. Sie besitzen in der Regel eine geringere pharmakologische Aktivität. Dem gegenüber stellen einige partialsynthetische Isoergoline, wie z. B. Lisurid und Tergurid, hochpotente Arzneistoffe in der Therapie der Parkinson-Krankheit dar.
Partialsynthetische Modifikationen
Basierend auf den natürlich vorkommenden Mutterkornalkaloiden wurden zahlreiche modifizierte Ergoline entwickelt. Das früher verwendete Migräneprophylaktikum Methysergid leitet sich vom einfachen Lysergsäureamid Ergometrin ab. Das ebenfalls in der Migränetherapie verwendete Dihydroergotamin wird durch Hydrierung aus Ergotamin gewonnen. Die Parkinsontherapeutika Pergolid und Lisurid können ausgehend von Clavinen bzw. von Lysergsäure gewonnen werden.
Entdeckung
Der Franzose Charles Tanret extrahierte 1875 aus Mutterkorn eine – allerdings ziemlich verunreinigte – Substanz, die er Ergotinin nannte. Ebenso wie das Ergotoxin, welche 1907 entdeckt wurde, ist es eine Mischsubstanz. Erst Arthur Stoll isolierte 1918 das Ergotamin, das erste reine Ergotalkaloid.
Mit dieser Entdeckung konnte die Lysergsäure als den Mutterkornalkaloiden zugrundeliegende Basisstruktur identizifiert werden. Die übrigen Alkaloide des Mutterkorns wurden in den folgenden 25 Jahren entdeckt:
- Ergotamin-Gruppe: Ergotamin / Ergotaminin (1918), Ergosin / Ergosinin (1936)
- Ergometrin-Gruppe: Ergometrin (Ergobasin, Ergonovin) / Ergometrinin (1935)
- Ergotoxin-Gruppe: Ergokristin / Ergokristinin (1935), Ergokryptin / Ergokryptinin (1937), Ergocornin / Ergocorninin (1943), Ergostin / Ergostinin (1943)
Besondere Verdienste um die Erforschung der Mutterkornalkaloide hat sich der schweizer Chemiker Albert Hofmann erworben, dessen Forschungen 1943 auch zur zufälligen Entdeckung des Halluzinogens LSD (Lysergsäurediethylamid) führte.
Medizinische Verwendung
Wegen ihrer pharmakodynamischen Wirkungen sind einige Mutterkornalkaloide in der Medizin u. a. zur Behandlung von Migräne, peripheren Durchblutungsstörungen, der Parkinson-Krankheit und des Restless-Legs-Syndroms relevant bzw. werden als Wehenmittel und Antihypertensiva eingesetzt. Auch in der Tiermedizin finden sie Anwendung.
Pharmakologische Eigenschaften
Die Wirkungen der Mutterkornalkaloide sind vielfältig. Sie können die Dopamin-Rezeptoren stimulieren und die Ausschüttung von Prolaktin und Somatotropin hemmen. Sie sind partielle Agonisten an den Serotonin-Rezeptoren. Auf die Uterusmuskulatur haben sie eine kontrahierende Wirkung (v. a. Ergometrin). Besonders natürlichem Ergotamin ist eine vasokonstriktorische Wirkung eigen. Die hydrierten Ergotamine blockieren die α-Adrenorezeptoren, was unter bestimmten Umständen kontrahierte Gefäße erweitern kann.
Indikation und Präparate
- Bromocriptin (z. B. Pravidel®, Bromocrel®): Parkinson-Krankheit, Akromegalie, Hyperprolaktinämie, Restless-Legs-Syndrom, Lakatationshemmung / Scheinträchtigkeit (Hund)
- Cabergolin (Cabaseril®, Galastop®): Parkinson-Krankheit, Restless-Legs-Syndrom, Scheinträchtigkeit bei Hunden
- Dihydroergotamin (z. B. Ergomimet®): Orthostatische Dysregulation, Krampfadern (Varizen), Hypotonie, Migräne (auch zur Prophylaxe)
- Dihydroergocryptin (Almirid®, Cripar®): Parkinson-Krankheit)
- Dihydroergotoxin (z. B. Hydergin®, Sponsin®, Orphol®): Durchblutungsstörungen, arterielle Hypertonie, Demenz, Migräne
- Ergometrin/Methylergometrin (Methergin®): Lakatationshemmung, Blutstillung (besonders im Uterus)
- Ergotamin (Ergo-Kranit®): Migräne, arterielle Hypertonie, Durchblutungsstörungen, Arrhythmie, Emetikum (i.v.)
- Lisurid (Dopergin®): Parkinson-Krankheit, Akromegalie, Hyperprolaktinämie, Lakatationshemmung, Restless-Legs-Syndrom
- Pergolid (Parkotil®): Parkinson-Krankheit, Restless-Legs-Syndrom
Rechtliches
Das deutsche Grundstoffüberwachungsgesetz schränkt die Abgabe von Ergotamin ein: es könnte nämlich als Basis zur Herstellung von LSD, einem in Deutschland verbotenen Betäubungsmittel, verwendet werden. Zusammen mit Ergometrin fällt es auch unter das „Übereinkommen der Vereinten Nationen vom 20. Dezember 1988 gegen den unerlaubten Verkehr mit Suchtstoffen und psychotropen Stoffen (Suchtstoffübereinkommen)“.
Literatur
- Albert Hofmann: Die Mutterkornalkaloide. Vom Mutterkorn zum LSD. Die Chemie der Mutterkornalkaloide. Nachtschatten, o.O. 2000 (Nachdr. v. 1964), ISBN 3-907080-64-5
- Otto Kraupp, Fred Lembeck (Hrsg.): Mutterkornalkaloide heute. Therapeutische Konsequenzen einer chemisch-pharmakologischen Differenzierung im Lichte neuer Forschungsergebnisse. Thieme, Stuttgart 1982, ISBN 3-13-621001-8
- Claudia Arntz: Molekularbiologische Untersuchungen zur Alkaloidsynthese bei Claviceps. Cramer, Berlin u.a. 1999
- Julia Groß: Untersuchungen zum Vorkommen von Ergolinen in höheren Pflanzen der Familie der Convolvulaceae und in endophytischen Pilzen. Diss. Bonn 2004.
Siehe auch
Weblinks
Wikimedia Foundation.