- Feshbach-Resonanz
-
Eine Feshbach-Resonanz ist ein Effekt aus der physikalischen Streutheorie, die nach dem amerikanischen Physiker Herman Feshbach benannt ist. Sie tritt auf, wenn sich ein gebundener Zustand (Molekülzustand) zwischen zwei Atomen in einem Streupotential befindet, das energetisch nur wenig oberhalb der Energiesumme der einlaufenden Teilchen liegt. In diesem Falle können die beiden Atome diesen gebundenen Zustand einnehmen. Infolgedessen „spüren“ sie das Potential für längere Zeit und die Änderung ihrer Wellenfunktion nimmt zu. Dadurch ändert sich die Streulänge des Systems.
Feshbach-Resonanzen können künstlich herbeigeführt werden: Im Falle der magnetischen Feshbach-Resonanz bedient man sich des Zeeman-Effektes, um die Streupotentiale so zueinander zu verschieben, dass diese Resonanz auftritt. Bei der optischen Feshbach-Resonanz hingegen koppelt man die Atome mit dem Molekülzustand, indem man Laserlicht mit dem exakten Energieabstand einstrahlt. Mit beiden Methoden lässt sich so die Streulänge nahezu beliebig ändern.
Die Molekülzustände werden normalerweise nicht tatsächlich besetzt: Dies ist unmöglich, da dabei ja Energie gewonnen oder verloren würde. Nur wenn die Energie des Molekülzustandes genau mit der Energiesumme der einlaufenden Atome zusammenfällt, gilt Energieerhaltung und die Atome können Moleküle bilden. Bei einer magnetischen Feshbach-Resonanz kann man diesen Fall künstlich herbeiführen und so gezielt Moleküle erzeugen. Man braucht nur das Magnetfeld so einzustellen, dass sich Moleküle bilden. Dann kann man das Molekülpotential absenken, und die Moleküle bleiben bestehen.
Ultrakalte Atome und Moleküle
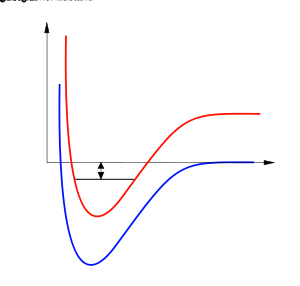
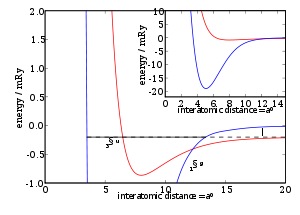 Das Bild stellt die Streupotentiale dar (als Beispiel wird Li-6 verwendet). Das rote Potential (Triplet) ist nach unten verschoben, zum Beispiel mit Hilfe eines Magnetfeldes, und die Dissoziationsenergie stimmt mit dem gebundenen Zustand im blauen Potential (Singulett) überein. Das kleine Bild gibt eine Übersicht. (Die Verschiebung und die Bindungsenergieen sind hier stark übertrieben dargestellt, die Potentiale dagegen korrekt)
Das Bild stellt die Streupotentiale dar (als Beispiel wird Li-6 verwendet). Das rote Potential (Triplet) ist nach unten verschoben, zum Beispiel mit Hilfe eines Magnetfeldes, und die Dissoziationsenergie stimmt mit dem gebundenen Zustand im blauen Potential (Singulett) überein. Das kleine Bild gibt eine Übersicht. (Die Verschiebung und die Bindungsenergieen sind hier stark übertrieben dargestellt, die Potentiale dagegen korrekt)
Die wichtigsten Anwendungen der Feshbach-Resonanz dürften im Bereich der ultrakalten Atome liegen (10−7 Kelvin und weniger). Sie sind hier als Forschungsobjekt beliebt, aber auch gefürchtet, führen sie doch insbesondere bei Bosonen zu starken Verlusten, da sich beim Durchstimmen der Magnetfelder die Streulänge plötzlich ändert, die Atome dadurch stoßen können und man durch Stoßprozesse die Atome aus der Falle verliert.
Bei Fermionen wird genau dies begrüßt: Die Feshbach-Resonanz ermöglicht nicht nur eine Wechselwirkung, sondern sogar eine, die sich wie oben beschrieben nach Belieben verändern lässt. Mit Fermionen konnte man daher auch erstmalig, wie oben erwähnt, gezielt Moleküle erzeugen. Da diese wiederum als Fermionenpaare Bosonen darstellen, konnte man diese in Form eines Bose-Einstein-Kondensates (in der Fachliteratur: BEC) kondensieren.
Aber nicht nur das: liegt der Molekülzustand energetisch niedriger als die Energiesumme der einlaufenden Atome (der Wechselwirkungsoperator im Hamiltonian muss negativ sein), ist die Wechselwirkung anziehend. Existiert zwischen Fermionen eine anziehende Wechselwirkung, so ist eine der Voraussetzungen der BCS-Theorie erfüllt. So konnte man einen BCS-Zustand aus ultrakalten Atomen erzeugen, der dem Elektronen-Grundzustand eines Supraleiters gleicht. Man erhält auf diese Weise durch die Feshbach-Resonanz einen so genannte BEC-BCS-Übergang, ein gegenwärtig (2007) sehr aktuelles Forschungsgebiet.
Literatur
- Herman Feshbach: Ann. Phys. (N. Y.) 5, 357 (1958) doi:10.1016/0003-4916(58)90007-1
- Ugo Fano: Nuovo Cimento 156, 12 (1935)
- Ugo Fano: Phys. Rev. 124, 1866 (1961) doi:10.1103/PhysRev.124.1866
- Per-Olov Löwdin: Studies in Perturbation Theory. IV. Solution of Eigenvalue Problem by Projection Operator Formalism. J. Math. Phys. 3, 969-982 (1962) doi:10.1063/1.1724312
- Claude Bloch: Nucl. Phys. 6, 329 (1958) doi:10.1016/0029-5582(58)90116-0
Wikimedia Foundation.