- Geranial
-
Strukturformel 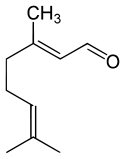
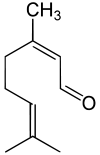
links Geranial (Citral A), rechts Neral (Citral B)Allgemeines Name Citral Andere Namen - 3,7-Dimethylocta-2,6-dienal
- (E)-3,7-Dimethylocta-2,6-dienal (Geranial)
- (Z)-3,7-Dimethylocta-2,6-dienal (Neral)
Summenformel C10H16O CAS-Nummer 5392-40-5 PubChem 8843 Kurzbeschreibung schwach gelbliche Flüssigkeit mit zitronenähnlichem Geruch Eigenschaften Molare Masse 152,24 g·mol−1 Aggregatzustand flüssig
Dichte 0,89 g·cm–3 [1]
Schmelzpunkt Siedepunkt 225 °C [1]
Dampfdruck Löslichkeit unlöslich in Wasser (420 mg/l bei 20 °C[1]), löslich in Ethanol
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 
Reizend (Xi) R- und S-Sätze R: 38-43 S: (2)-24/25-37 LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Citral ist das Gemisch aus den Stereoisomeren Geranial (Citral A) und Neral (Citral B). Geranial ist als Duftstoff u. a. in Tomaten zu geringen Anteilen als Abbauprodukt von Lycopen zu finden. Citral ist Hauptbestandteil vom Lemongrasöl. Es ist Alarmpheromon der Blattschneiderameise.
Inhaltsverzeichnis
Eigenschaften
Die CAS-Nummer des Citral lautet 5392-40-5, die des Nerals 106-26-3[6] und die des Geranials 141-27-5[7]. Die IUPAC Bezeichnung für Citral lautet 3,7-Dimethylocta-2,6-dienal. Es handelt sich um acyclische Monoterpen-Aldehyde. Citral ist eine schwach gelbliche Flüssigkeit mit intensiv-frischem Zitronenduft. Das Gemisch siedet bei 228 °C, in Wasser ist es nahezu unlöslich. Citral wirkt in reiner Form sowie im Gemisch in Konzentrationen ab 1 % reizend auf die Haut.[1]
Verwendung
Citral wird als Duft- und Aromastoff verwendet. Gemäß der 7. Ergänzung der EU Kosmetikrichtline 76/768/EEC muss es aufgrund allergenen Potenzials als kosmetischer Inhaltsstoff deklariert werden.
Reaktionen
Neral und Geranial lassen sich durch Dehydrierung aus Nerol und Geraniol herstellen. Citral reagiert mit Aceton im alkalischen Milieu (zum Beispiel Bariumhydroxid) zuerst unter Wasserabgabe zum Pseudoionon. Dieses kann dann unter Anwesenheit von Säuren und höheren Temperaturen in das Isomer Ionon überführt werden.[8][9]
Im alkalischen Milieu kann es auch in Ethanal und 2-Methylhept-2-en-6-on zerfallen (Retro-Aldol-Reaktion).
Quellen
- ↑ a b c d e f Eintrag zu Citral in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 22. Juli 2008 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 5392-40-5 im European chemical Substances Information System ESIS
- ↑ Biochemical Journal. Vol. 34, Pg. 1196, 1940.
- ↑ a b Citral bei ChemIDplus
- ↑ Food and Cosmetics Toxicology. Vol. 2, Pg. 327, 1964.
- ↑ PubChem 643779 (Neral)
- ↑ PubChem 638011 (Geranial)
- ↑ NODA, C., ALT, G. P., WERNECK, R. M. et al.: In Aldol Condensation of Citral with Acetone on Basic Solid Catalysts Braz. J. Chem. Eng. 1998, 15 doi:10.1590/S0104-66321998000200004 [1]
- ↑ A. Russell, R.L. Kenyon: In Pseudoionone Organic Syntheses Coll. Vol. 3, 747 [2]
Wikimedia Foundation.
