- Glykosaminoglykan
-
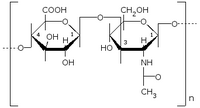
Glykosaminoglykane (GAG) oder Mucopolysaccharide sind linear aus sich wiederholenden Disacchariden aufgebaute, saure Polysaccharide.[1] Die einzelnen Disaccharid-Einheiten bestehen dabei aus Estern einer Uronsäure (meist Glucuronsäure, seltener Iduronsäure, Uronsäure der Idose), die 1-3-glykosidisch mit einem Aminozucker wie N-Acetylglucosamin verbunden sind. Die Disaccharid-Einheiten der Ketten selbst sind 1-4-glykosidisch verknüpft.[2] Teilweise sind die Glykosaminoglykane auch mit Schwefelsäure oder Essigsäure weiter verestert.
Mucupolysaccharide sind Bestandteile vieler biologischer Makromoleküle, etwa der kovalent an Proteine gebundenen Proteoglykane. Sie bilden das Gerüst vieler faserbildener Stoffe und besitzen durch ihre Fähigkeit, Wasser aufzunehmen, eine hohe Elastizität.
Je nach der Zusammensetzung der Disaccharideinheiten unterscheidet man verschiedene Untergruppen der Glykosaminoglykane:
Inhaltsverzeichnis
Hyaluronsäure (HA)
- → Hauptartikel: Hyaluronsäure
Hyaluronsäure besteht aus β-(1→4)-glykosidisch miteinander verknüpften Glukuronyl-β-(1→3)-N-Acetylglukosamin-Disaccharideinheiten, wobei bis zu 100.000 aufeinander folgen können. Die Zuckereinheiten sind unsulfatiert. Hyaluronsäure liegt als amphipathische Helix vor und ist als einziges Glykosaminoglykan nicht an ein Proteinzentralfilament gebunden. Ein Hyaluronsäuremolekül kann durch Hydratisierung eine bis zu 10.000mal größere Raumbeanspruchung besitzen als das Volumen des Moleküls selbst, so dass sich schon bei niedrigen Konzentrationen ein viskoses Gel bildet. Damit dient es als biologisches Schmiermittel. Hyaluronsäure kommt im Knorpel, in der Gelenkschmiere, in der Nabelschnur sowie im Glaskörper des Auges vor. In den Fibroblasten wird die Hyaluronsäure aus D-Glucose synthetisiert.[2]
Heparin/Heparansulfat (HS)
- → Hauptartikel: Heparin, Heparinsulfat
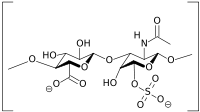
Heparin besteht aus D-Glukuronsäure, die β-(1→4)-glykosidisch, bzw. L-Iduronsäure, die α-(1→4)-glykosidisch mit einem Glukosamin verknüpft ist. Die Bindung zwischen den verschiedenen Disacchariden ist α-(1→4)-glykosidisch. Die Aminofunktion des Glukosamins trägt häufig eine Acetylgruppe oder einer Sulfatgruppe. Zusätzlich sind O-Sulfatgruppen vorhanden. Heparansulfat ist strukturell mit dem Heparin verwandt, nur besitzt es weniger N- und O-Sulfatreste und mehr N-Acetylgruppen.
Chondroitinsulfat/Dermatansulfat (CS/DS)
- → Hauptartikel: Chondroitin
Chondroitinsulfat oder Chondritinsulfat besteht aus β-(1→4)-glykosidisch verknüpften Glukuronyl-β-(1→3)-N-Acetylgalaktosamin-Disacchariden, wobei D-Glukuronsäure teilweise in L-Iduronsäure umgewandelt wird. Wenn mehr als 10 % des Uronats als Iduronat vorliegen, spricht man von Dermatansulfat. Der Grad der Sulfatierung von Chondroitinsulfat und Dermatansulfat beträgt etwa ein Sulfatrest pro Disaccharid. Das Sulfat in Chondroitinsulfat liegt als 4-Sulfat oder 6-Sulfat vor. Beim Dermatansulfat kann aufgrund Epimerisierung an C5 auch Glucuronat vorkommen.
Die Molare Masse liegt zwischen 10 und 50 kDa.
Chondroitinsulfat kommt im Bindegewebe (besonders im Knorpel und in Synovia), Dermatansulfat ebenfalls im Bindegewebe (vorwiegend in der Haut) vor.[2]
Keratansulfat (KS)
Die Disaccharideinheiten von Keratansulfat sind β-(1→3) verknüpfte Galaktosyl-β-(1→4)-N-Acetylglukosaminreste. Beide Zucker können eine Sulfatierung am C6-Atom aufweisen. Pro Einheit treten 0,8-1,5 Sulfatgruppen auf. Keratansulfat ist in Knorpel, Cornea und Bandscheiben (Disci) vorhanden.[2]
Einzelnachweise
Wikimedia Foundation.