- Hexamethylensulfid
-
Strukturformel 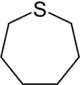
Allgemeines Name Thiepan Andere Namen Hexamethylensulfid
Summenformel C7H12S CAS-Nummer 4753-80-4 Eigenschaften Molare Masse 116,22 g·mol−1 Dichte 0,99 g·cm–3 (20 °C) [1]
Siedepunkt Sicherheitshinweise Gefahrstoffkennzeichnung [2] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Thiepan, auch Hexamethylensulfid genannt, ist der einfachste schwefelhaltige gesättigte siebengliedrige Heterocyclus.
Inhaltsverzeichnis
Darstellung
Die Darstellung von Thiepan kann durch die Reaktion von 1,6-Dibromhexan mit Natriumsulfid[3] oder 1,6-Diiodhexan mit Kaliumsulfid[4] erfolgen.
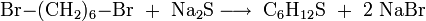
Eigenschaften
Thiepan siedet bei 173–174 °C und besitzt eine Dichte von 0,99 g/cm3.
Reaktionen
Die möglichen Reaktionen beschränken sich weitgehend auf Reaktionen am Schwefelatom und dessen α-Position, dem Kohlenstoff neben dem Schwefel. So kann Thiepan mit Kaliumpermanganat zu Sulfonen[5] oder mit Wasserstoffperoxid zu Sulfoxiden oxidiert werden.[6]
An α-Kohlenstoff können auch Abgangsgruppen eingeführt werden. So liefert die Reaktion mit N-Chlorsuccinimid 2-Chlorthiepan.[7] Dies ermöglicht weitere Reaktionen mit Nukleophilen. Hierzu können beispielsweise Grignard-Reagenzien[8] zur Einführung organischer Reste verwendet werden.
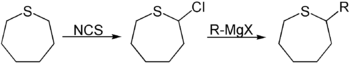 Sequenz aus Chlorierung mit N-Chlorsuccinimid und Grignard-Reaktion. R = organischer Rest, X = Halogenid
Sequenz aus Chlorierung mit N-Chlorsuccinimid und Grignard-Reaktion. R = organischer Rest, X = HalogenidQuellen
- ↑ a b Mueller in: Monatsh. Chem. 1953, 84, 1206–1214.
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ A. Singh, A. Mehrotra, S. L. Regen: High Yield Medium Ring Synthesis of Thiacycloalkanes, in: Synth. Commun. 1981, 11, 409–412.
- ↑ J. v. Braun: Über cyclische Sulfide, in: Chem. Ber. 1910, 43, 3220–3226.
- ↑ G. W. Gokel, H. M. Gerdes, D. M. Dishong in: Journal of Organic Chemistry 1980, 45, 18, 3634–3639.
- ↑ R. L. Crumbie, D. D. Ridley in: Aust. J. Chem. 1981, 34, 5 , 1027–1035.
- ↑ H. J. Gais in: Angew. Chem. 1977, 89, 3, 201–202.
- ↑ H. Sashida, T. Tsuchiya in: Heterocycles 1982, 19, 11, 2147–2150.
Wikimedia Foundation.
