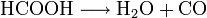- Kohlenstoffmonooxid
-
Strukturformel 
Allgemeines Name Kohlenstoffmonoxid Andere Namen - Kohlenmonoxid
- Kohlenstoffmonooxid
Summenformel CO CAS-Nummer 630-08-0 PubChem 281 Kurzbeschreibung farb- und geruchloses Gas Eigenschaften Molare Masse 28,01 g·mol−1 Aggregatzustand gasförmig
Dichte 1,2506 kg·m−3 (0 °C)[1]
Schmelzpunkt −205,07 °C[1]
Siedepunkt −191,55 °C[1]
Löslichkeit 30 mg·l−1 in Wasser (20 °C)[1]
Sicherheitshinweise Gefahrstoffkennzeichnung aus RL 67/548/EWG, Anh. I [2] 

Hoch-
entzündlichGiftig (F+) (T) R- und S-Sätze R: 61-12-23-48/23 S: 53-45 MAK LD50 WGK 1 (schwach wassergefährdend)[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Kohlenstoffmonoxid (auch Kohlenstoffmonooxid, gebräuchlicher Kurzname: Kohlenmonoxid) ist eine chemische Verbindung aus Kohlenstoff und Sauerstoff und ist damit neben Kohlenstoffdioxid, Kohlenstofftrioxid und Kohlenstoffsuboxid eines der Oxide des Kohlenstoffs
Kohlenstoffmonoxid ist ein farb-, geruch- und geschmackloses giftiges Gas. Es entsteht bei der unvollständigen Oxidation von kohlenstoffhaltigen Substanzen. Dies erfolgt zum Beispiel beim Verbrennen dieser Stoffe, wenn nicht genügend Sauerstoff zur Verfügung steht oder die Verbrennung bei hohen Temperaturen stattfindet (siehe auch: Boudouard-Gleichgewicht). Kohlenstoffmonoxid selbst ist brennbar und verbrennt mit blauer Flamme zusammen mit Sauerstoff zu Kohlenstoffdioxid.
Inhaltsverzeichnis
Name
In der deutschen Norm DIN 32640 „Chemische Elemente und einfache anorganische Verbindungen – Namen und Symbole“ vom Dezember 1986 werden nur die Schreibweisen „Kohlenstoffmonooxid“ und „Carbonmonooxid“ mit „oo“ empfohlen, weil nach den IUPAC-Regeln für die Nomenklatur der anorganischen Chemie Endvokale vorangestellter griechischer Zahlwörter nicht weggelassen werden.
Dagegen werden in der Ausgabe der IUPAC-Nomenklatur von 1990 nur die Schreibweisen „Kohlenstoffmonoxid“ und „Carbonmonoxid“ genannt, zur Verwendung der multiplikativen Präfixe heißt es: „Die abschließenden Vokale der multiplikativen Präfixe werden nicht weggelassen, es sei denn, es liegen zwingende sprachliche Gründe vor. Monoxid ist eine derartige Ausnahme“.[3]
Eigenschaften
Physikalische Eigenschaften

Der Bindungsabstand zwischen Kohlenstoff- und Sauerstoffatom beträgt in der Festphase 106 und in der Gasphase 112,8 pm.[4]Zündtemperatur 605 °C[1] Kritische Temperatur −140,2 °C[1] Kritischer Druck 35,0 bar[1] ΔfH0g −110,53 kJ/mol Die Molekülstruktur kann am besten mit der Molekülorbitaltheorie beschrieben werden. Die im Vergleich zu organischen Carbonylverbindungen etwa 10 pm kürzere C-O-Bindung weist auf eine partielle Dreifachbindung hin.[5] Das Molekül hat ein geringes Dipolmoment (0,12 D) und wird oft wie folgt dargestellt (Mesomerie):
 Mesomere Grenzstrukturen. Zu beachten ist, dass die Oktettregel in den beiden rechten Strukturformeln nicht eingehalten wird.
Mesomere Grenzstrukturen. Zu beachten ist, dass die Oktettregel in den beiden rechten Strukturformeln nicht eingehalten wird.Die ungewöhnliche Stabilität hat ähnliche Gründe wie beim sehr inerten, isoelektronischen Distickstoffmolekül (N2): Die CO-Dissoziationsenergie beträgt 1070,3 kJ/mol.[4]
Chemische Eigenschaften
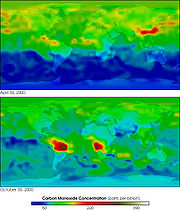
Die Bildung von Kohlenstoffmonoxid aus den Elementen ist zwar exotherm, allerdings steht Kohlenstoffmonoxid in einem Disportionierungsgleichgewicht mit Kohlenstoff und Kohlenstoffdioxid. Weil sich dieses Gleichgewicht bei Raumtemperatur nur fast unmessbar langsam einstellt, lässt sich CO trotz der ungünstigen Gleichgewichtslage isolieren – CO ist metastabil. Bei höheren Temperaturen verschiebt sich das Gleichgewicht zugunsten des Kohlenstoffmonoxids (Prinzip von LeChatelier). Dies wird beispielsweise bei der Eisenherstellung (Hochofenprozess) genutzt, wo das gasförmige Kohlenstoffmonoxid ein viel effektiveres Reduktionsmittel darstellt als das feste Koks. Die Halbwertszeit von Kohlenstoffmonoxid in der Atmosphäre beträgt etwa ein bis vier Monate, abhängig von der Lufttemperatur und Anwesenheit anderer Gase.[6]
Kohlenstoffmonoxid ist ein gutes und preiswertes Reduktionsmittel und wird in dieser Funktion vielfältig verwendet. Die Oxidationskraft von CO ist hingegen nur schwach ausgeprägt.
Kohlenstoffmonoxid ist ein in der Organometallchemie häufig verwendeter Ligand, die Chemie Metallcarbonyle ist daher gut erforscht. Kohlenstoffmonoxid zählt zu den Starkfeld-Liganden und ist isoelektronisch zum Distickstoff (N2) sowie zu den Ionen Cyanid (CN−) und Nitrosyl (NO+). Durch Ausprägung von sich synergetisch verstärkenden Hin- und Rückbindungen entsteht eine starke Metall-Ligand-Bindung. CO ist ein starker σ-Donator und π-Akzeptor.
Kohlenstoffmonoxid besitzt mit 1073 kJ/mol die stärkste Bindung eines ungeladenen Moleküls.
Toxizität
Kohlenstoffmonoxid ist ein gefährliches Atemgift. Wenn es z. B. über die Lunge in den Blutkreislauf gelangt ist, koordiniert es an das zentrale Eisenatom des Hämoglobins und behindert so den Sauerstofftransport im Blut, was zum Tod durch Erstickung führen kann. Kohlenstoffmonoxid bindet etwa 325-mal stärker an den roten Blutfarbstoff Hämoglobin als Sauerstoff, bei einem Kohlenstoffmonoxidanteil von 0,1 Prozent in der Atemluft wird also etwa die Hälfte der roten Blutkörperchen deaktiviert. Die Giftwirkung des CO wird durch die Proteinumgebung des Häms im Hämoglobin gemindert, so bindet CO an ein ungehindertes Häm etwa 26.000-mal stärker als Sauerstoff. Als Ursache wird angenommen, dass in der Enzymtasche zu wenig Platz ist, um die vom CO bevorzugte lineare Fe-C-O-Geometrie zu erlauben, die vom Disauerstoff bevorzugte gewinkelte Koordination wird dagegen nicht behindert.[7] Bei einem Atemluftanteil von über einem Prozent tritt der Tod binnen ein bis zwei Minuten ein.[8][9] Die Eliminationshalbwertszeit des Kohlenstoffmonoxid aus dem Blut beträgt 2 bis 6,5 Stunden,[1] abhängig von der aufgenommenen Menge an CO und der Ventilationsrate des betroffenen Menschen.
Durch die Bindung des CO an Hämoglobin werden Pulsoxymeter getäuscht und geben fälschlich hohe Sauerstoffsättigungsraten an. Die äußerlichen Anzeichen einer Kohlenmonoxidvergiftung sind kirschrote Schleimhäute. Nach neueren Untersuchungen mit hohen Fallzahlen (231 Patienten) ist dieses klinische Zeichen insbesondere bei leichteren Vergiftungsformen selten anzutreffen.[10] Die Farbe ist ein Resultat der tiefroten Hämoglobin-Kohlenstoffmonoxid-Charge-Transfer-Komplexe. Ferner können die nach dem Tod bei der Leiche auftretenden Totenflecke (Livores) durch eben diesen Mechanismus typischerweise ebenfalls leuchtend rot gefärbt sein und somit einen Hinweis auf eine Kohlenmonoxidvergiftung geben.
Kohlenmonoxid ist ein Photosynthesegift und schädigt auch das Chlorophyll der Pflanzen.
Der prozentuale Anteil des im Blut mit Kohlenstoffmonoxid belegten Hämoglobins wird auch als COHb abgekürzt (Kohlenmonoxid- Hämoglobin).
Wirkungen verschiedener Dosen
- Für gesunde Erwachsene besteht nach älteren Studien auch bei Dauerbelastung von acht Stunden täglich bei Konzentrationen bis 115 ppm keine Gefahr; es entstehen lediglich Konzentrationen von 4 % COHb, bei Nichtrauchern und 7,6 % bei Rauchern. Neuere Studien belegen jedoch, dass bei Risikogruppen mit Herz-Kreislauf-Erkrankungen schon Belastungen ab 2,7 % Krankheitssymptome verstärken können.[1]
- Bei höheren chronischen Belastungen über 150 bis 300 ppm entstehen Schwindelgefühle, Schläfrigkeit, Übelkeit und Erbrechen.
- Akut tödlich wirkende Mengen des Gases (LD50)[1]: siehe Infobox (oben).
Schwerhörigkeit wird bei CO-Belastung um bis zu 50 % verstärkt.[11][12]
Rettung bei Kohlenmonoxid-Intoxikationen
Kohlenmonoxid in hoher Konzentration reagiert stark exotherm mit Luft, wenn sich ein Zündfunke findet. Schon ein Funke im Lichtschalter oder der Türglocke kann daher eine Explosion auslösen. Für den Helfer bedeutet das, dass höchste Vorsicht geboten ist – Eigensicherung hat absoluten Vorrang. Insbesondere sollte auch die Gefahr einer eigenen Vergiftung berücksichtigt werden. Umluftunabhängiger Atemschutz ist in der Regel zur Rettung, welche in den meisten Fällen durch die Feuerwehr erfolgt, notwendig.
Patienten mit einer Kohlenmonoxid-Vergiftung werden vom Rettungsdienst und Notarzt im Allgemeinen intubiert und mit positiv endexpiratorischem Druck (PEEP) und 100 % Sauerstoff beatmet. Durch das deutlich erhöhte Sauerstoffangebot wird das Kohlenmonoxid vom Hämoglobin verdrängt. Auch eine hyperbare Oxygenierung kann erwogen werden.[13][14]
Biologische Bedeutung
Beim Menschen beträgt der prozentuale Anteil des im Blut mit Kohlenstoffmonoxid belegten Hämoglobins COHb im venösen Blut zwischen 0,7 bis 1,1 %, wovon etwa 0,5 % endogen produziert werden. Ein erhöhter CO-Spiegel in den Zellen führt zur bis zu 1000-fach verstärkten Ausschüttung des Glycoproteins Erythropoetin (EPO).[15]
Das Enzym Hämoxygenase baut Häm-Verbindungen, die vorwiegend aus Hämoglobin stammen, unter Freisetzung von Kohlenstoffmonoxid ab. Dieses Enzym sowie eine Guanylatcyclase, welche von CO reguliert wird, konnten im Geruchszentrum des menschlichen Gehirns und im Bulbus olfactorius nachgewiesen werden. Demnach könnte Kohlenstoffmonoxid als gasförmiger Botenstoff für den Geruchssinn dienen. Die aktivierte Guanylatcyclase setzt dann den sekundären Botenstoff cGMP frei.[16] Neben Kohlenstoffmonoxid, cGMP und cAMP wird auch Stickstoffmonoxid als Second Messenger betrachtet.[17] Sowohl Stickstoff- als auch Kohlenstoffmonoxid können als extrem niedermolekulare, wasserlösliche Gase sehr schnell und relativ unbehindert Biomembranen durchdringen und dienen deshalb als Neurotransmitter bei der Übertragung von Informationen aus dem primären oder sensorischen in das sekundäre oder Langzeitgedächtnis durch das limbische System.[18][19]
Kohlenstoffmonoxid besitzt bei chronischer Darmentzündung eine entzündungshemmende Wirkung, was auch die vorher rätselhafte Tatsache erklärt, dass Raucher wesentlich seltener an Colitis ulcerosa erkranken als Nichtraucher.[20][21] Auch nach Lungentransplantationen verhinderte eine inhalative, gering dosierte Gabe von Kohlenstoffmonoxid einen Schaden durch Ischämie oder Reperfusion.[15] Werden Nieren, die zur Transplantation vorgesehen sind, in einer Lösung aufbewahrt, die Kohlenstoffmonoxid in geringer Konzentration enthält, wird der ansonsten zu beobachtende Anstieg an freiem Häm und Abfall an Cytochrom P450 gehemmt, und so eine zellschädigende Lipidperoxidation vermindert.[22] Günstige Wirkungen von Kohlenstoffmonoxid wurden zudem beschrieben in Tiermodellen von septischem Schock, Darmverschluss (Ileus) und Arteriosklerose.[23] Bei Frauen mit Schwangerschaftshypertonie und Schwangerschaftsvergiftung (Präeklampsie) ist die Kohlenstoffmonoxidkonzentration in der Ausatemluft vermindert.[24] Raucherinnen haben ein vermindertes Risiko, an Präeklampsie zu erkranken.[25] Medikamente, welche kontrollierte Mengen an Kohlenstoffmonoxid transportieren und freisetzen können, befinden sich in der Entwicklung.[26]
Herstellung
Kohlenstoffmonoxid kann aus zahlreichen Edukten wie z. B. Erdgas, Biogas, Leichtbenzin, Schwerölen, Kohle und Biomasse hergestellt werden, wobei zunächst Synthesegas, eine Mischung von Kohlenstoffmonoxid mit Wasserstoff erzeugt wird, welche dann gereinigt und aufbereitet wird (Synthesegas, Fischer-Tropsch-Synthese). Es entweicht zudem in großen Mengen als Luftschadstoff über Abgas-Emissionen.
Großtechnisch (z. B. aus Koks) kann Kohlenstoffmonoxid unter Einfluss von Energie (Verbrennung) wie folgt hergestellt werden:
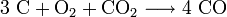
- Kohlenstoff verbrennt mit Sauerstoff bei Anwesenheit von Kohlenstoffdioxid zu Kohlenstoffmonoxid.
Dabei wird das Kohlenstoffdioxid eingesetzt, um ein Verbrennen des Kohlenstoffs zu Kohlenstoffdioxid zu verhindern:
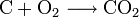
- Bei der Anwesenheit von ausreichend Sauerstoff verbrennt Kohlenstoff zu Kohlenstoffdioxid.
Im Labor ist CO durch Zersetzung von Ameisensäure herstellbar:
Der Zerfall wird durch die wasserentziehende Wirkung konzentrierter Schwefelsäure bewirkt, die der Ameisensäure zugetropft wird.
Entsorgung
Da Kohlenstoffmonoxid sehr giftig ist, müssen überschüssige Mengen mit speziellen Absorbern aufgefangen oder mit einer Abflammvorrichtung abgeflammt werden. Besondere Vorsicht gilt bei CO-Luft-Gemischen, da sie sehr explosiv reagieren können.
Zusätzlich besteht die Möglichkeit Kohlenstoffmonoxid mit Kupfer(II)-oxid oder Hopcalite katalytisch zu Kohlenstoffdioxid umzusetzen.
Verwendung
Reines Kohlenstoffmonoxid wird vor allem für folgende Anwendungen eingesetzt:
- Herstellung von Ameisensäure über Methylformiat
- Herstellung von Natriumformiat über Natriumhydroxid
- Umsetzung mit Methanol zu Essigsäure
- Umsetzung mit Chlor zu Phosgen
- Carbonylierungsreaktionen in der organischen Synthese
- Reduktionsmittel für z. B. Eisenerz
- Zum Binden von Kohlenstofffasern in einer reinen Kohlenstoffmatrix für die Herstellung von CFK
 CO-Wächter in einer Tiefgarage
CO-Wächter in einer TiefgarageNachweis
Im Handel gibt es heute elektronische Sensoren, die den Nachweis von Kohlenstoffmonoxid im Bereich von 50–1000 ppm in der Raumluft gestatten. Bei elektronischen Sensoren sollte gleichzeitig aber kein Wasserstoffgas vorhanden sein, da sonst die Nachweisgenauigkeit deutlich beeinflusst wird. Als präzises Nachweisreagenz dient auch Diiodpentoxid I2O5, das in einem U-Rohr bei höheren Temperaturen (ca. 80–160 °C) in Gegenwart von Kohlenstoffmonoxid quantitativ zu elementarem Iod I2 reduziert wird, bei gleichzeitiger Bildung von Kohlenstoffdioxid CO2. Durch Rück-Titration des Iods mit Thiosulfat S2O32− (Iodometrie) lässt sich der CO-Gehalt des Gases dann bestimmen. Ditte erforschte schon im Jahr 1870 dieses Verfahren mit Diiodpentoxid. Wasserstoff – auch in höheren Konzentrationen – stört dabei nur sehr minimal die Nachweisgenauigkeit dieser Methode. Durch gleichzeitige quantitative Bestimmung des umgesetzten Kohlenstoffdioxids (Bestimmung durch Leitfähigkeit oder durch Fällung einer Bariumhydroxidlösung) ist die Bestimmung sehr genau.
Quellenangaben
- ↑ a b c d e f g h i j k l m n o p q r Eintrag zu CAS-Nr. 630-08-0 in der GESTIS-Stoffdatenbank des BGIA, abgerufen am 12. Dezember 2007 (JavaScript erforderlich)
- ↑ Eintrag zu CAS-Nr. 630-08-0 im European chemical Substances Information System ESIS
- ↑ IUPAC: Nomenklatur der Anorganischen Chemie. Deutsche Ausgabe der Empfehlungen 1990. VCH, Weinheim 1994, ISBN 3-527-25713-6, S. 76.
- ↑ a b Nils Wiberg, Egon Wiberg und Arnold Fr. Holleman: Lehrbuch der Anorganischen Chemie. Gruyter Verlag; 102., stark umgearb. u. verb. Auflage 2007; ISBN 978-3-11-017770-1; S. 898
- ↑ J.E. Huheey, E.A. Keiter, R.L. Keiter : Anorganische Chemie: Prinzipien von Struktur und Reaktivität, 2003, Walter de Gruyter, ISBN 3-11-017903-2
- ↑ Dr. Peter Bützer: Autokatalysator
- ↑ James Collman et al: Nature of O2 and CO Binding to Metalloporphyrins and Heme Proteins, 1976
- ↑ Oxide des Kohlenstoffs-Kohlenstoffmonoxid
- ↑ Hu & Speizer: Environmental and occupational hazards. Carbon Monoxide. In: Harrison’s Principles of Internal Medicine, McGraw-Hill, New York City, 14th edition Seite 2533
- ↑ Cevik AA et al. Interrelation between the PSS, CO-Hb levels and in-hospital clinical course of CO poisoning. Int J Clin Pract 2006; 60: 1558–1564 PMID 16918999
- ↑ Kohlenmonoxid
- ↑ Markus Fritz: Klipp und klar, 100 x Umwelt. Bibliographisches Institut AG, Mannheim 1977, ISBN 3-411-01706-6 Seite 18
- ↑ Weaver et al.: Carbon monoxide poisoning: risk factors for cognitive sequelae and the role of hyperbaric oxygen. Am J Respir Crit Care Med. 2007;176(5):491-7. PMID 17496229
- ↑ Weaver et al. Hyperbaric oxygen for acute carbon monoxide poisoning. N Engl J Med. 2002 Oct 3;347(14):1057–1067. PMID 12362006
- ↑ a b C.S. Gebhard: Untersuchungen zur Regulation der Kohlenmonoxid-bedingten Stimulation der Erythropoetinsekretion bei der Ratte, Dissertation 2007, Eberhard Karls Universität Tübingen
- ↑ Wissenschaft-Online-Lexika: Eintrag zu Kohlenmonoxid im Lexikon der Neurologie
- ↑ P. Weydt: Rezeptorvermittelte Kalziumsignale in kultivierten humanen Gliomzellen, 2000, Tectum Verlag, ISBN 3-8288-8137-8
- ↑ R.F. Schmidt, F. Lang: Physiologie des Menschen: Lernen und Gedächtnis, Springer-Verlag, ISBN 978-3-540-32908-4
- ↑ P. A. Berg: Chronisches Müdigkeits- und Fibromyalgiesyndrom, 2003, Springer-Verlag, ISBN 3-540-44194-8
- ↑ Das „Gute“ am Kohlenmonoxid - Immunologie: Entzündungshemmende Wirkung im Darm, Abendblatt vom 24. Dezember 2005
- ↑ "Journal of Experimental Medicine". 2005, Vol. 202, S. 1703-17139
- ↑ Nakao A et al.: „Ex vivo carbon monoxide prevents cytochrome P450 degradation and ischemia/reperfusion injury of kidney grafts..“ Kidney Int 2008; 74: S. 1009–1016 Abstract
- ↑ Nakao A et al.: „Protective effect of carbon monoxide in transplantation..“ J Cell Mol Med 2006; 10: S. 650–671 Abstract Artikel
- ↑ Baum M et al.: „End-tidal carbon monoxide measurements in women with pregnancy-induced hypertension and preeclampsia..“ Am J Obstet Gynecol. 2000; Oct;183(4): S. 900-3 Abstract
- ↑ Bainbridge SA et al.: „Direct placental effects of cigarette smoke protect women from pre-eclampsia: the specific roles of carbon monoxide and antioxidant systems in the placenta..“ Med Hypotheses. 2005; 64(1): S. 17-27 Abstract
- ↑ Foresti R et al.: „Use of carbon monoxide as a therapeutic agent: promises and challenges..“ Intensive Care Med 2008; 34: S. 649–658 Abstract
Weblinks
- Über die Vergiftung durch Kohlenoxydgas – Innsbrucker Nachrichten 29.1.1872
- Kohlenmonooxid bei seilnacht.com
- Verbotene Färbung von Fischfilets mit Kohlenstoffmonoxid
Sicherheitsdatenblätter
Sicherheitsdatenblätter für Kohlenstoffmonoxid verschiedener Hersteller in alphabetischer Reihenfolge:
Literatur
- Hans Beyer, Wolfgang Walter: Lehrbuch der Organischen Chemie. S. Hirzel Verlag, Stuttgart – Leipzig 1998, 23. überarb. und aktualisierte Auflage, ISBN 3-7776-0808-4
Wikimedia Foundation.