- L-Penicillamin
-
Strukturformel 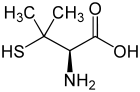
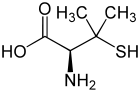
L-Penicillamin (links) bzw. D-Penicillamin (rechts)Allgemeines Freiname Penicillamin Andere Namen - 2-Amino-3-mercapto-3-methyl-buttersäure
- D-Penicillamin: 3-mercapto-D-valin
(S)-Penicillamin: (S)-3,3-Dimethyl-cystein
Summenformel C5H11NO2S CAS-Nummer 52-67-5 PubChem 5852 ATC-Code M01CC01
DrugBank DB00859 Kurzbeschreibung weißes bis fast weißes, kristallines Pulver [1] Arzneistoffangaben Wirkstoffklasse Fertigpräparate - Metalcaptase® (D)
- Artamin® (A)
- Mercaptyl® (CH)
Verschreibungspflichtig: ja Eigenschaften Molare Masse 149,21 g·mol−1 Schmelzpunkt 202−206 °C [2]
Löslichkeit leicht löslich in Wasser, schwer löslich in Ethanol 96 % [1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1]
Xn
Gesundheits-
schädlichR- und S-Sätze R: 36/37/38-63 S: 36/37/39 Bitte beachten Sie die eingeschränkte Gültigkeit der Gefahrstoffkennzeichnung bei Arzneimitteln LD50 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Penicillamin ist eine nicht-proteinogene α-Aminosäure. Es existieren von Penicillamin zwei Enantiomere: D- und L-Penicillamin. Die D-Variante wird als Medikament bei der Wilsonschen Krankheit eingesetzt. Außerdem kann D-Penicillamin bei Schwermetalvergiftungen mit Blei, Cadmium oder Quecksilber angewendet werden oder bei Rheuma. Die L-Variante ist dagegen giftig, da der Körper diese Variante des Penicillamins nicht von anderen proteinogenen Aminosäuren unterscheiden kann.
Inhaltsverzeichnis
Vorkommen
D-Penicillamin ist ein Vorstoff des Penicillins. In Schimmelpilzarten, die Penicillin auf natürlichem Wege herstellen können, ist es ein daher ein Zwischenprodukt des natürlichen Stoffwechsels.
Gewinnung und Darstellung
Der Ausgangsstoff für aus Penicillin synthetisch hergestelltes D-Penicillamin ist die Aminosäure Valin. Alternativ wird D-Penicillamin in einer dreizehnstufigen Synthese aus Isobutyraldehyd, Ammoniak und Schwefel hergestellt, mit der Asinger-Reaktion als Schlüsselschritt[3].
Medizinische Bedeutung
D-Penicillamin kann als Medikamentenwirkstoff eingesetzt werden bei
- Morbus Wilson/hepatolentikuläre Degeneration: D-Penicillamin bildet aufgrund seiner molekularen Struktur leicht Chelatkomplexe. Die Thiol-Gruppe besitzt eine hohe Affinität zu Kupfer, dadurch kann das krankheitsbedingt überschüssige Kupfer an das Molekül gebunden und über den Urin aus dem Körper ausgeschieden werden.
- Schwermetall-Vergiftungen: Schwermetalle können irreversibel an Enzyme binden und diese in ihrer Funktion hemmen oder sie vollständig deaktivieren. Hier wird ebenfalls die chelatbildende Eigenschaft von D-Penicillamin ausgenutzt. Das Molekül wirkt wie ein Staubsauger für Schwermetalle im Körper.
- Cystin-Harnsteine: Cystin-Harnsteine entstehen, wenn sich übermäßig Cystin und Homocystin unter Bildung einer Disulfidbrücke zusammenballt. Die Thiol-Gruppe des D-Penicillamin vermag diese Disulfidbindungen zu spalten und somit die Harnsteine aufzulösen.
Unerwünschte Wirkungen von Penicillamin (Auswahl, gelegentlich bis häufig):
- Teratogenität: Bei gebährfähigen Frauen ist auf eine wirksame Schwangerschaftsverhütung zu achten.
- Hauterscheinungen (häufig, 1 % bis 10 %)
- Nierenschädigung (häufig)
- Knochenmarkschädigungen (häufig)
- Myasthenisches Syndrom (gelegentlich, 0,1 % bis 1 %)
Einzelnachweise
- ↑ a b c d Safety Data Sheet for PENICILLAMINE CRS – European Pharmacopoeia (Ph. Eur.) 16. Februar 2009
- ↑ The Merck Index. An Encyclopaedia of Chemicals, Drugs and Biologicals. 14. Auflage, 2006, S. 1223, ISBN 978-0-911910-00-1.
- ↑ Wolfgang M. Weigert, Heribert Offermanns und Paul Scherberich: D-Penicillamin - Production and Properties, Angewandte Chemie-International Edition 14, 330–336 (1975).
Weblinks
Wikimedia Foundation.
