- Lepirudin
-
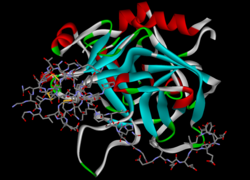
Hirudin-1 (Hirudo medicinalis), Lepirudin Modell von Hirudin (Stäbchen) im Komplex mit Thrombin (Bänder) nach PDB 4HTC Vorhandene Strukturdaten: s. UniProt Größe 65 Aminosäuren Bezeichner Externe IDs UniProt: P01050 CAS-Nummer: 120993-53-5 Arzneistoffangaben ATC-Code B01AE02 DrugBank DB00001 Wirkstoffklasse Fibrinolytikum Handelsnamen Refludan®
Inhibitorklassifikation MEROPS I14.001 Vorkommen Übergeordnetes Taxon Hirudo medicinalis Hirudin ist ein Polypeptid aus dem medizinischen Blutegel (Hirudo medicinalis) mit antikoagulatorischen Eigenschaften (Blutgerinnungshemmung).
1884 entdeckte der britische Physiologe John Berry Haycraft, dass Blutegel beim Blutsaugen einen Stoff mit stark gerinnungshemmender Wirkung absondern[1], den Jakobi 1904 Hirudin nannte.[2] Die Substanz wurde 1955 erstmals durch Extraktion aus Blutegelköpfen isoliert.[3]
Die Primärstruktur des HV-1 (Hirudin Variant-1) besteht aus 65 Aminosäuren.[4][5]
Die medizinische Verwendung von Hirudin geschieht entweder durch direktes Ansetzen lebender Egel am Patienten oder mittels gentechnisch hergestellter Substanzen.
Hirudin bindet sich an die Fibrinogenbindestelle von Thrombin und hemmt über einen Ausläufer das aktive Zentrum, wodurch dessen Wirkung blockiert wird. Es kommt vor allem bei Patienten mit Heparininduzierter Thrombozytopenie Typ II (HIT II) zum Einsatz.
Hirudin ist in der Lage, die Plazenta-Schranke zum ungeborenen Kind zu überwinden sowie in die Muttermilch zu gelangen.
Eine Steuerung der Therapie mit Hirudin ist über die Bestimmung der PTT möglich. Da es kein spezifisches Antidot gibt, ist im Falle einer Überdosierung eine Hämofiltration oder Hämodialyse erforderlich.
Quellen
- ↑ Haycraft, J.B. (1884): Über die Einwirkung eines Sekretes des officinellen Blutegels auf die Gerinnbarkeit des Blutes. In: Arch. Exp. Pathol. Pharmakol. Bd. 18, S. 209–217.
- ↑ Forth, W., Henschler, D. (2001): Allgemeine und spezielle Pharmakologie und Toxikologie 8. Auflage, S. 568.
- ↑ Fritz Markwardt (1955): Untersuchungen über Hirudin. In: Naturwissenschaften. Bd. 42, S. 537-538. doi:10.1007/BF00630151
- ↑ Dodt, J. et al. (1984): The complete amino acid sequence of hirudin, a thrombin specific inhibitor Application of colour carboxymethylation. In: FEBS Lett. Bd. 165, S. 180-184. doi:10.1016/0014-5793(84)80165-9
- ↑ UniProt P01050
Literatur
- Nowak, G. & Schrör, K. (2007): Hirudin - the long and stony way from an anticoagulant peptide in the saliva of medicinal leech to a recombinant drug and beyond. A historical piece. In: Thromb. Haemost. Bd. 98, S. 116-119. PMID 17598001 doi:10.1160/TH07-05-0364 PDF
Siehe auch
Wikimedia Foundation.