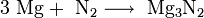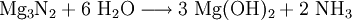- Mg3N2
-
Kristallstruktur Keine Kristallstruktur vorhanden Allgemeines Name Magnesiumnitrid Verhältnisformel Mg3N2 CAS-Nummer 12057-71-5 Kurzbeschreibung gelbes Pulver Eigenschaften Molare Masse 100,95 g·mol−1 Aggregatzustand fest
Dichte 2,712 g·cm−3[1]
Schmelzpunkt 800 °C (Zersetzung)[1]
Löslichkeit reagiert mit Wasser[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 

Reizend Leicht-
entzündlich(Xi) (F) R- und S-Sätze R: 11-29-36/37/38 S: 7/8-26-33-37-43-60 Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Magnesiumnitrid ist eine chemische Verbindung aus den Elementen Magnesium und Stickstoff. Es besitzt die Formel Mg3N2 und gehört zur Stoffgruppe der Nitride. Es entsteht als gelber Feststoff zum Beispiel beim Erhitzen von metallischem Magnesium auf ca. 600 °C unter Stickstoffatmosphäre.
Bei der Verbrennung von Magnesiummetall an Luft entsteht es neben Magnesiumoxid (MgO) und lässt dieses gelblich erscheinen. Mit Wasser hydrolysiert Magnesiumnitrid zu Magnesiumhydroxid und Ammoniak.
Im historischen Serpek-Verfahren wurde diese Reaktion (neben der Hydrolyse von AlN) zur Ammoniaksynthese eingesetzt (siehe Haber-Bosch-Verfahren).
Quellen
Wikimedia Foundation.