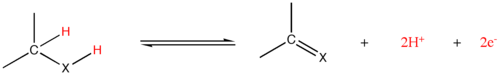- Monooxygenasen
-
Oxidoreduktasen sind Enzyme der ersten Enzymklasse laut der systematischen Nomenklatur der Enzymkommission der International Union of Biochemistry (IUB) und katalysieren Redoxreaktionen. Der systematische Name ist Donor:Acceptor Oxidoreduktases. Unterschieden wird zwischen Monooxygenasen, Dioxygenasen, Oxidasen, Dehydrogenasen, Reduktasen und Peroxygenasen.
Inhaltsverzeichnis
Reaktionen
Katalyse der folgenden Redoxreaktionen
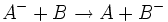
- Oxygenierung und/oder
- Addition oder Entfernung eines Reduktionsäquivalents
Oxygenasen
Siehe den Hauptartikel Oxygenasen
Oxygenasen übertragen ein oder mehrere Sauerstoffatome auf ihr Substrat, wobei oft auch Ringöffnungen am aromatischen Molekül stattfinden. Meist wird NADP/NADPH verbraucht.
Oxidasen
Als Oxidasen bezeichnet man Enzyme, welche die bei der Oxidation eines Substrates freiwerdenden Elektronen auf Sauerstoff (O2) übertragen. Dabei dient der Sauerstoff als Elektronenakzeptor und wird – bei Aufnahme von zwei Elektronen – zu Wasser (H2O) oder – bei Aufnahme von vier Elektronen – zu Wasserstoffperoxid (H2O2) reduziert.
Oxidasen verbrauchen kein NADH bzw NADPH und sind oft abhängig von FAD
- Aminosäureoxidasen
- Monoaminooxidasen (MAO)
- Alkoholoxidasen
Dehydrogenasen
Dehydrogenasen verbrauchen bzw. bilden NADH, NADPH oder FADH2
- Alkoholdehydrogenasen
- Aldehyddehydrogenasen
- Aminosäurendehydrogenasen
- CO-Dehydrogenasen
- Falls NAD-Kofaktor, dann X=O oder NH
- Falls Flavine bzw. 1e- Akzeptoren, dann X=O, NH oder CHR
Hydrogenasen
Hydrogenasen kommen z.B.in methanogenen Bakterien als Ni2+-haltige Enzyme vor und benötigen den Kofaktor F420. Diese Enzyme katalysieren die Reduktion von Kohlenstoffdioxid (CO2) zu Methan mittels Wasserstoffmolekülen (H2) als Reduktionsmittel.
Allgemeine Beispiele
Wikimedia Foundation.