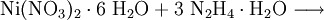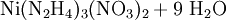- Nickelnitrat
-
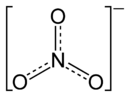
Strukturformel 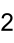

Allgemeines Name Nickel(II)-nitrat Andere Namen - Nickelnitrat
- Nickelnitrat-Hexahydrat
Summenformel Ni(NO3)2 CAS-Nummer 13138-45-9 (wasserfrei)
13478-00-7 (Hexahydrat)Kurzbeschreibung grüne, zerfliessende, wasserlösliche, hygroskopische Kristalle[1] Eigenschaften Molare Masse 182,72 g/mol (wasserfrei)
290,83 g/mol (Hexahydrat)Aggregatzustand fest
Dichte 2,05 g/cm3[1]
Schmelzpunkt 56,7 °C[1]
Siedepunkt 136,7 °C[1]
Löslichkeit sehr gut löslich in Wasser (940 g/l bei 20 °C)[1], löslich in Alkohol
Sicherheitshinweise Gefahrstoffkennzeichnung [1] 

Giftig Brand-
fördernd(T) (O) R- und S-Sätze R: 45-8-22-43 S: 53-24-27-28-37/39-45 MAK Für krebserzeugende Stoffe wird generell kein MAK-Wert vergeben
LD50 1620 mg/kg (oral, Ratte)[1]
WGK 3 (stark wassergefährdend)[1] Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Nickel(II)-nitrat ist eine chemische Verbindung des Metalls Nickel aus der Gruppe der Nitrate. Sie kommt gewöhnlich in Form ihres Hexahydrates Ni(NO3)2 · 6 H2O vor, weshalb sich alle Angaben aus der Tabelle auf dieses beziehen.
Inhaltsverzeichnis
Eigenschaften
Nickel(II)-nitrat ist ein starkes Oxidationsmittel und kommt in verschiedenen Hydratformen vor. Am häufigsten ist Hexahydrat (Ni(NO3)2 · 6 H2O). Beim langsamen Erhitzen des Nickel(II)-nitrat Hexahydrats bildet sich ab 45 °C das Tetrahydrat ((Ni(NO3)2 · 4 H2O)), ab 80 Grad C das Dihydrat (Ni(NO3)2 · 2 H2O), bei 120 bis 145 °C basisches Nickelnitrat. Beim abkühlen kann sich Nonahydrat bilden (Ni(NO3)2 · 9 H2O). Oberhalb von 200 °C beginnt sich Nickelnitrat zu Nickel(II)-oxid zu zersetzen. Beim raschen Erhitzen erfolgt zwischen 310 und 340 °C Zersetzung zu Nickel(II)-oxid, Stickoxiden und Sauerstoff.
Durch Reaktion von Nickelnitrat-Hexahydrat mit Hydrazinhydrat kann Nickelhydrazinnitrat gewonnen werden.
Durch Reaktion von Nickelnitrat mit Natriumhydroxid entsteht Nickel(II)-hydroxid.
Verwendung
Nickel(II)-nitrat verwendet man in der Keramikindustrie (als braunes Pigment), in der Färberei als Beizmittel, zum elektrolytischen Vernickeln, zum Gewinnen von Nickel(II)-oxid und zum Herstellen von reinem Katalysatornickel.
Sicherheitshinweise
Nickel(II)-nitrat wirkt brandfördernd und ist als krebserzeugend eingestuft.
Quellen
Wikimedia Foundation.