- Phenylglycin
-
Strukturformel 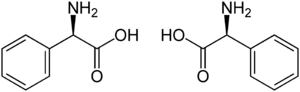
D-Phenylglycin (links) und L-Phenylglycin (rechts)
Allgemeines Name α-Phenylglycin Andere Namen - (R)-2-amino-2-phenylessigsäure
- D-(–)-Phenylglycin
- D-2-Phenylglycin
- (S)-2-amino-2-phenylessigsäure
- L-(–)-Phenylglycin
- L-2-Phenylglycin
Summenformel C8H9NO2 CAS-Nummer - 875-74-1 (D-Phenylglycin)
- 2935-35-5 (L-Phenylglycin)
- 2835-06-5 (DL-Phenylglycin)
PubChem 70134 Kurzbeschreibung weißes kristallines Pulver[1] Eigenschaften Molare Masse 151,16 g·mol−1 Aggregatzustand fest
Schmelzpunkt Löslichkeit schlecht in Wasser (3 g·l−1 bei 20 °C)[2]
Sicherheitshinweise Gefahrstoffkennzeichnung [1] keine Gefahrensymbole R- und S-Sätze R: keine R-Sätze S: keine S-Sätze Soweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. D-Phenylglycin [Synonym:(R)-Phenylglycin] ist eine ökonomisch bedeutende, in der Natur nicht vorkommende, nicht-proteinogene α-Aminocarbonsäure. Sie ist in der Seitenkette mehrerer semisynthetischer β-Lactam-Antibiotika als Teilstruktur enthalten, etwa im Ampicillin. Die enantiomere Aminosäure L-Phenylglycin [Synonym:(S)-α-Phenylglycin] besitzt nur untergeordnete Bedeutung.
Inhaltsverzeichnis
Darstellung
D-Phenylglycin kann durch Spaltung des Racemats DL-Phenylglycin mit Hilfe von D-Campher-10-sulfonsäure, in der Gegenwart von Essigsäure und Salicylaldehyd erhalten werden. Die Ausbeute bei diesem Verfahren beträgt 68 % bei einer optischen Reinheit von 95,9 %.[3]
Die enzymatische Darstellung von D-Phenylglycin aus Phenylpyruvat gelang 2006.[4] Phenylpyruvat ist ein direkter Vorläufer des L-Phenylalanins. Daher wurde für die Darstellung ein E. coli-Stamms eingesetzt, der auf die Produktion von L-Phenylalanin auf Basis von Glucose optimiert war. Die Umwandlung des Phenylpyruvats erfolgte über Mandelat und Phenylglyoxylat in drei Stufen. Diese wurden durch drei Enzyme (Hydroxymandelat-Synthase (HmaS), Hydroxymandelat-Oxidase (Hmo) und die stereoinvertierende Hydroxyphenylglycin-Aminotransferase (HpgAT)) katalysiert. Die diese Enzyme kodierenden Gene stammten aus Amycolatopsis orientalis, Streptomyces coelicolor und Pseudomonas putida.
Eigenschaften
α-Phenylglycin ist ein farbloser Feststoff, der sich bei 305 °C zersetzt. Der Drehwert α einer 1-molaren Lösung in 1-molarer Salzsäure beträgt bei 20 °C und einer Wellenlänge von 589 nm –155°.[5]
Verwendung
D-Phenylglycin ist ein wichtiger Seitenketten-Baustein für die halbsynthetische Gewinnung von β-Lactam-Antibiotika, wie Cefalexin oder Ampicillin.[4]
Literatur
- ↑ a b c Sicherheitsdatenblatt Alfa-Aesar.
- ↑ Sicherheitsdatenblatt Acros.
- ↑ Bull. Chim. Soc. Jap. 1983, 56, 3744–3747; beschrieben in Patentschrift WO 1995023805.
- ↑ a b Müller, U. et al.: "Metabolic engineering of the E. coli L-phenylalanine pathway for the production of D-phenylglycine (D-Phg)", Metab Eng. 2006, May 8(3), 196–208; PMID 16466681.
- ↑ Sicherheitsdatenblatt Aldrich.
Wikimedia Foundation.
