- PuF3
-
Kristallstruktur 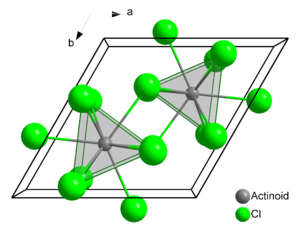
Kristallsystem hexagonal Raumgruppe 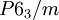
Gitterkonstanten a = pm
c = pmKoordinationszahlen Pu[9], F[3] Allgemeines Name Plutonium(III)-fluorid Andere Namen Plutoniumtrifluorid
Verhältnisformel PuF3 CAS-Nummer 13842-83-6 PubChem 139624 Kurzbeschreibung violette Kristalle[1] Eigenschaften Molare Masse 301,059 g/mol Aggregatzustand fest
Dichte 9,3 g/cm3[1]
Schmelzpunkt 1396 °C[2]
Siedepunkt Zersetzung bei 2000 °C[1]
Sicherheitshinweise Gefahrstoffkennzeichnung [3] keine Einstufung verfügbar R- und S-Sätze R: siehe oben S: siehe oben Radioaktivität 
RadioaktivSoweit möglich und gebräuchlich, werden SI-Einheiten verwendet. Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen. Plutonium(III)-fluorid (PuF3) ist eine Ionenverbindung bestehend aus Pu3+- und F−-Ionen und bildet violette Kristalle. Es kristallisiert im hexagonalen Kristallsystem in der Raumgruppe P63/m und zwei Formeleinheiten pro Elementarzelle. Seine Kristallstruktur ist isotyp mit Uran(III)-chlorid. In der Struktur werden die Plutoniumatome von je neun Fluoratomen umgeben, als Koordinationspolyeder ergibt sich dabei ein dreifach überkapptes, trigonales Prisma.[1] Der Schmelzpunkt der Verbindung liegt bei 1396 °C.[2]
Verwendung
Um Plutonium zur Wiederaufbereitung durch Ausfällung aus Lösungen abtrennen zu können, wurde eine Methode zur Ausfällung als Plutonium(III)-fluorid entwickelt, um eine Alternative zur bisherigen Plutoniumperoxidmethode zu haben.[4] Eine Studie des Los Alamos National Laboratory aus dem Jahr 1957 berichtet, dass diese Methode gegenüber dem bisherigen Verfahren weniger effektiv sei,[5] während eine neuere Studie, die vom US-Office of Scientific and Technical Information in Auftrag gegeben wurde, diese als eine eher effektivere Methode darstellt.[6]
Einzelnachweise
- ↑ a b c d Plutonium(III)-fluorid bei www.webelements.com.
- ↑ a b David R. Lide: Handbook of Chemistry and Physics, 87, S. 113, CRC Press 1998, ISBN 0-8493-0594-2(Zugriff am 20. Juni 2008)
- ↑ In Bezug auf ihre Gefährlichkeit wurde die Substanz von der EU noch nicht eingestuft, eine verlässliche und zitierfähige Quelle hierzu wurde noch nicht gefunden.
- ↑ C. K. Gupta: Hydrometallurgy in Extraction Processes, 2, S. 206-208, CRC Press 1990, ISBN 0-8493-6805-7(Zugriff am 20. Juni 2008)
- ↑ R. S. Winchester: Aqueous Decontamination of Plutonium from Fission Product Elements, S. 9-10, Los Alamos Scientific Laboratory of the University of California 1957(Zugriff am 20. Juni 2008)
- ↑ L. L. Martella: Laboratory-scale evaluations of alternative plutonium precipitation methods. United States Office of Scientific and Technical Information(Zugriff am 20. Juni 2008)
Literatur
- Arnold F. Holleman, Nils Wiberg: Lehrbuch der Anorganischen Chemie, 102. Auflage, de Gruyter, Berlin 2007, ISBN 978-3-11-017770-1.
- Norman N. Greenwood, Alan Earnshaw: Chemie der Elemente, 1. Auflage, Wiley-VCH, Weinheim 1988, ISBN 3-527-26169-9.
Wikimedia Foundation.
