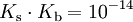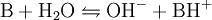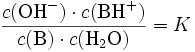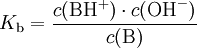Basestärke — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PK-Wert — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKS-Wert — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKa — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKa-Wert — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKs — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKs-Wert — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
PKs-Werte — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
Säurenkonstante — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia
Säurestärke — Die Säurekonstante Ks ist eine Stoffkonstante und gibt Aufschluss darüber, in welchem Maße ein Stoff in einer Gleichgewichtsreaktion mit Wasser unter Protolyse reagiert: . Dabei steht HA für eine Brønsted Säure (nach Brønsted), die ein Proton H+… … Deutsch Wikipedia